Lire l'article complet

La lettre de l’hépato-gastroentérologue - n° 2 - vol. V - mars-avril 2002 85
OBSERVATION DIALOGUÉE
Pseudo-achalasie : vraie tumeur
●S. Lecleire, G. Savoye*
ous rapportons l’observation d’un homme de
67ans, hospitalisé dans le service de gastroentéro-
logie pour une aphagie brutale. L’histoire clinique
remontait à plusieurs mois et comportait une altération de l’état
général avec une perte de 10 kg associée à une dysphagie mixte,
prédominant pour les solides, et évoluant depuis quelques
semaines. L’aphagie s’était installée brutalement la veille de l’hos-
pitalisation et chaque prise alimentaire était suivie précocement
de vomissements. Les antécédents de ce malade étaient dominés
par un diabète non insulino-dépendant et non compliqué, traité
par sulfamides et biguanides, et un éthylo-tabagisme non sevré.
À l’admission aux urgences, l’examen clinique était parfaitement
normal. Les examens biologiques usuels étaient sans particula-
rité (numération formule sanguine, ionogramme sanguin, hémo-
stase, transaminases, bilirubinémie, phosphatases alcalines, fonc-
tion rénale), exceptée une élévation modérée de la γ-glutamyl-
transférase à deux fois la normale.
Une fibroscopie œsogastroduodénale était pratiquée en première
intention et mettait en évidence un volumineux corps étranger
alimentaire bloqué juste au-dessus du cardia. À ce niveau, il était
noté une petite ulcération superficielle linéaire de 5 mm. L’ex-
traction instrumentale du corps étranger impacté était effectuée
et l’ulcération œsophagienne biopsiée. Il n’était pas noté de res-
saut au passage de l’endoscope, une fois l’extraction réalisée.
Quant à l’examen anatomopathologique, il permettait de conclure
à une ulcération œsophagienne aiguë sans anomalie suspecte de
malignité.
Dans ce contexte, une manométrie œsophagienne était réalisée
afin d’explorer la dysphagie et l’épisode d’aphagie qui restaient
inexpliqués après l’endoscopie. Cet examen retrouvait, au niveau
du corps de l’œsophage, des troubles nets de la propagation des
ondes péristaltiques: 45% des déglutitions de liquides et 85%
des déglutitions de solides (10 g de poulet) n’étaient pas suivies
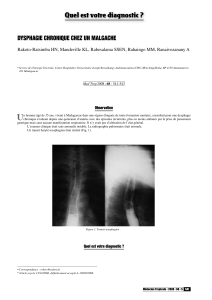
de contractions propagées (figure 1). Une sensation de blocage
survenait à la neuvième bouchée de solides. Cette sensation s’es-
tompait finalement après la prise d’un verre d’eau. On notait une
absence de relaxation du sphincter inférieur de l’œsophage en
réponse aux déglutitions de liquides pour seulement une déglu-
tition sur quatre. Ces troubles moteurs, quoique suggérant une
achalasie débutante, restaient donc aspécifiques. Le diagnostic
évoqué à ce stade était celui d’une pseudo-achalasie devant l’as-
sociation d’une altération de l’état général, de troubles de pro-
pagation des contractions œsophagiennes aspécifiques survenant
chez un éthylotabagique de plus de 60 ans. Ce doute diagnos-
tique motivait la réalisation d’un scanner abdomino-thoracique
et d’une échoendoscopie.
La tomodensitométrie thoraco-abdominale retrouvait une masse
tissulaire mesurée à 6 cm de grand axe sur 3,7 cm, débutant au
contact de l'extrémité inférieure de l’œsophage et du cardia joux-
tant le pilier gauche du diaphragme (figure 2),associée à une
lame d’épanchement pleural homolatéral. Les parenchymes hépa-
tique et pulmonaire étaient normaux.
Le repérage endoscopique retrouvait une muqueuse œsopha-
gienne normale avec notamment une cicatrisation de l’ulcération
linéaire, décrite lors de l’épisode d’impaction alimentaire.
L’échoendoscopie œsophagienne objectivait une volumineuse
formation tissulaire, homogène, développée dans la région car-
diale, en dehors de la partie antérieure et gauche de l’œsophage,
sur une hémi-circonférence. La lésion débutait à 32 cm des
N
* Département d’hépato-gastroentérologie et de nutrition,
hôpital C. Nicolle, Rouen.
Figure 1. Tracé de manométrie objectivant un défaut de propagation
des contractions œsophagiennes secondaires à une déglutition de 10 ml
de liquide.

La lettre de l’hépato-gastroentérologue - n° 2 - vol. V - mars-avril 2002
86
arcades dentaires et infiltrait la musculeuse de la face latérale
gauche de l’œsophage. Elle était en contact avec le pilier dia-
phragmatique gauche et mesurait 5,5 cm de diamètre. Il n’exis-
tait, pas plus qu’à la TDM, de ganglion suspect ou d’ascite.
En vue d’une décision opératoire, un transit œsophagien pré-
opératoire était réalisé et mettait en évidence une discrète perte
du péristaltisme à l’origine d’une hypotonie des deux tiers infé-
rieurs de l’œsophage, une rigidité anormale segmentaire de l’œ-
sophage abdominal et un élargissement de l’espace inter-phré-
nico-gastrique.
Le patient était opéré et le chirurgien constatait en peropératoire
une volumineuse lésion dans la région du cardia, envahissant net-
tement le pilier gauche du muscle diaphragmatique et débordant
largement sur la coupole gauche. S’y associaient de nombreuses
granulations péritonéales, localisées sur le corps gastrique et sur
de multiples anses grêliques. La palpation hépatique permettait de
percevoir des formations intraparenchymateuses évoquant forte-
ment des métastases méconnues jusque-là par l’imagerie préopé-
ratoire. De multiples prélèvements étaient réalisés sur la masse
cardiale et au sein du parenchyme hépatique pour un examen
extemporané. Cet examen affirmait la nature maligne de toutes les
lésions prélevées, sans pouvoir en déterminer l’origine exacte ou
le type histologique précis. L’exérèse projetée n’était donc pas réa-
lisée et une jéjunostomie était mise en place dans le même temps
opératoire. L’examen histologique définitif retrouvait une proli-
fération tumorale, constituée de lobules de taille variable, séparés
par de larges travées de stroma fibreux, richement vascularisé.
L’étude immuno-histochimique objectivait un seul marqueur
positif, la synaptophysine, associée aux lésions neuroendocrines.
Tous les marqueurs épithéliaux et conjonctifs étaient, quant à eux,
négatifs.
Le diagnostic final retenu était celui d’une tumeur neuroendo-
crine à grandes cellules avec diffusion métastatique. La mise en
œuvre d’une nutrition entérale en site jéjunal, en complément à
une alimentation mixée, permettait une rapide reprise de poids.
La recherche d’une sécrétion neuroendocrine en excès s’avérait
négative, et initialement une surveillance simple était mise en
place. L’examen tomodensitométrique de contrôle, réalisé à trois
mois de l’intervention, notait une stabilité lésionnelle, et il était
décidé de poursuivre la surveillance et de ne réserver chimiothé-
rapie et traitement par analogues de la somatostatine qu’à une
progression tumorale patente ou à l’apparition d’une symptoma-
tologie invalidante.
DISCUSSION
C’est le plus souvent au niveau du cardia que se produisent les
impactions alimentaires. La brutalité d’installation de ces acci-
dents conduit rapidement le malade à consulter. Les symptômes
classiques du blocage cardial sont une dysphagie aiguë avec,
éventuellement, une aphagie complète. On peut noter une hyper-
salivation, associée parfois à des troubles respiratoires à type de
toux. Ces signes imposent une extraction endoscopique dont les
modalités pratiques de délai (immédiate ou dans les 24 heures),
de sédation (sous anesthésie ou non), de techniques utilisées
(pinces diverses, poussée ou non) sont adaptées aux signes cli-
niques, au malade, à la taille et aux caractéristiques du bolus res-
ponsable de l’obstruction (alimentaire ou non). L’urgence pas-
sée, après l’extraction, une endoscopie de contrôle doit toujours
être réalisée afin de rechercher un facteur favorisant, dont les plus
fréquemment en cause sont les sténoses œsophagiennes orga-
niques et, par ordre de fréquence, les lésions tumorales suivies
des lésions peptiques. L’absence d’une telle lésion, ce qui était le
cas dans notre observation, doit faire évoquer la possibilité d’un
obstacle fonctionnel. D’authentiques achalasies ont en effet été
révélées par des accidents d’impaction alimentaires. Ces cir-
constances particulières de diagnostic d’achalasie sont essentiel-
lement décrites chez des enfants ou des adultes jeunes. Des
troubles non spécifiques peuvent être mis en évidence devant un
accident d’impaction alimentaire. Ce malade présentait un trouble
du péristaltisme œsophagien notable (45% des déglutitions de
liquides et 85% des déglutitions de solides non propagées) mais,
OBSERVATION DIALOGUÉE
Figure 2. Coupe tomodensitométrique objectivant une volumineuse for-
mation tumorale développée au contact du pilier du diaphragme gauche
au temps artériel (figure 2a) et au temps portal (figure 2b).
a
b

La lettre de l’hépato-gastroentérologue - n° 2 - vol. V - mars-avril 2002 87
qui du fait de la persistance de certaines propagations et de relaxa-
tions transitoires du sphincter inférieur conservées dans 75% des
déglutitions, ne permettait pas de retenir le diagnostic d’achala-
sie. En revanche, l’association de ces troubles manométriques au
contexte clinique d’un sujet âgé de plus de 55ans, présentant une
dysphagie progressive et une altération de l’état général, fait évo-
quer une pseudo-achalasie.
Cette entité clinique peut être très délicate à distinguer de l’acha-
lasie primitive, que ce soit en termes de clinique, d’endoscopie
ou de manométrie. Cependant, certains signes cliniques doivent
faire évoquer le diagnostic de pseudo-achalasie plutôt que celui
d’achalasie primitive : un âge de début des troubles supérieur à
55 ans, une perte de poids supérieure à 10% du poids originel,
mais surtout une vitesse d’amaigrissement rapide, et une dys-
phagie évoluant depuis moins d’un an (1,2). Ces caractéristiques
étaient retrouvées dans notre observation. De même, une fibro-
scopie œsogastroduodénale macroscopiquement normale, mais
au cours de laquelle la jonction œsogastrique n’est franchie que
difficilement (3),doit inciter à la prudence dans ce contexte cli-
nique et à la réalisation de profondes biopsies cardiales, même
si celles-ci restent le plus souvent négatives. Il n’existe pas de
critère manométrique fiable pour distinguer une pseudo-achala-
sie d’une achalasie. Même un tracé typique avec un apéristal-
tisme œsophagien et une altération des relaxations du SIO en
réponse aux déglutitions ne permet pas d’écarter le diagnostic de
pseudo-achalasie. De plus, le contexte de survenue des troubles
doit conduire à la poursuite des investigations.
L’exploration d’un malade présentant un tableau de pseudo-acha-
lasie comporte la réalisation d’un examen tomodensitométrique
abdomino-thoracique. Le scanner peut aider au diagnostic en
montrant un épaississement de la paroi œsophagienne dont le
caractère asymétrique ou supérieur à 10 mm est évocateur d’in-
filtrat tumoral. Le diagnostic peut être plus aisé comme dans notre
observation où une masse para-œsophagienne, responsable de la
symptomatologie, est reconnue (4). La réalisation de cet examen
permet également d’orienter vers les possibilités d’exérèse, même
si notre observation en est un contre-exemple.
L’échoendoscopie œsophagienne et cardiale a une sensibilité plus
élevée que l’examen tomodensitométrique dans cette indication,
mais nécessite une anesthésie générale. Dans notre cas, elle met-
tait en évidence l’infiltration de la musculeuse œsophagienne.
Elle permet également un bilan préopératoire précis et une clas-
sification standardisée de la lésion tumorale.
Les étiologies des pseudo-achalasies sont dominées par les
adénocarcinomes du cardia, qui représentent plus de 50% des
causes de pseudo-achalasie. Ces lésions peuvent infiltrer la région
cardiale sans avoir un développement endoluminal évident en
endoscopie. Les carcinomes épidermoïdes sont plus rarement en
cause. Ce type de cancer de l’œsophage a, en effet, un dévelop-
pement endoluminal qui échappe rarement à l’examen endosco-
pique. Il ne faut pas hésiter à réaliser de nouvelles biopsies au
cours d’un second examen endoscopique si la première série est
négative, et la rétrovision pour l’étude de la région cardiale doit
être réalisée soigneusement. Des causes exceptionnelles de
pseudo-achalasie ont été décrites, comme des envahissements par
une tumeur primitive bronchique ou un cancer ORL, une tumeur
mésenchymateuse œsophagienne ou encore un pseudo-kyste pan-
créatique. Une exploration chirurgicale diagnostique, si l’endo-
scopie, la tomodensitométrie et l’échoendoscopie se sont révé-
lées insuffisantes, est recommandée ; son utilisation en pratique
reste exceptionnelle dans cette situation clinique (3). Dans notre
observation, la pseudo-achalasie était due à une tumeur neu-
roendocrine à grandes cellules. Ces lésions sont très rares, leur
potentiel évolutif semble lent, et la stratégie de leur traitement,
comme de leur suivi, n’est pas codifiée.
Le mécanisme physiopathologique qui rend compte des troubles
moteurs œsophagiens n’est pas non plus bien élucidé. En effet,
si une hyperpression ou des relaxations incomplètes du SIO peu-
vent trouver leur cause dans une masse para-œsophagienne, l’ab-
sence de propagation des ondes péristaltiques est plus difficile à
expliquer. Dans notre observation, l’échoendoscopie a permis de
mettre en évidence une infiltration pariétale œsophagienne attei-
gnant la musculeuse et remontant sur l’œsophage thoracique. On
évoque un rôle possible de l’infiltration des plexus myentériques
pour expliquer la cause de la dysphagie dans les pseudo-achala-
sies. Ces données ont même conduit certains auteurs à proposer
avec un succès symptomatique la toxine botulinique en traite-
ment palliatif de la dysphagie chez un malade atteint de pseudo-
achalasie par envahissement tumoral locorégional (5). En dehors
de cette observation anecdotique, le traitement de ces pseudo-
achalasies reste un traitement étiologique, s’il est réalisable au
moment du diagnostic. Dans notre observation, la résection chi-
rurgicale projetée n’a pu être effectuée, et l’histologie définitive
de la lésion a conduit à proposer une surveillance simple jusqu’à
ce jour. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1.
Kharilas PJ, Kishk SM, Helm JF et al. Comparison of pseudoachalasia and
achalasia. Am J Mad 1987 ; 82 : 439-46.
2.
Tracey JP, Traube M. Difficulties in the diagnosis of pseudoachalasia. Am J
Gastroenterol 1994 ; 89 : 2014-8.
3.
Moonka R, Patti MG, Feo CV et al. Clinical presentation and evaluation of
malignant pseudoachalasia. J Gastrointest Surg 1999 ; 3 : 456-61.
4.
Carter M, Deckmann RC, Smith RC et al. Differentiation of achalasia from
pseudoachalasia by computed tomography. Am J Gastroenterol 1997 ; 92 : 624-8.
5.
Vallera RA, Brazer SR. Botulimun toxin for suspected pseudoachalasia. Am J
Gastroenterol 1995 ; 90 : 1319-21.
OBSERVATION DIALOGUÉE
1
/
3
100%