But de ce tp La calorimétrie a pour but de mesurer la quantité de

I. But de ce tp
La calorimétrie a pour but de mesurer la quantité de chaleur (énergie
thermique) absorbée ou cédée par un corps. Les mesures sont basées sur
des échanges thermiques par relevé de la température en fonction du
temps. Le but de cette expérience est de:
1- Déterminer la capacité calorifique du calorimètre
2- Déterminer la chaleur massique du cuivre, du fer et de
l’aluminium
II. Partie théorique
III. La chaleur est un transfert d'énergie qui a lieu suite à une
différence de température entre deux corps. La chaleur Q
m est
IV.
V. où c est la chaleur spécifique.
VI.
VII. Chaleurs spécifiques ( 20°C et 1atm)
substance
c( J/kg•K)
Aluminium
900
Cuivre
385
Acier/Fer
450
Plomb
130
Laiton
370
Étain(Sn)
220
Zinc
380
Mercure
140
Eau
4190

Glace (-10°C)
2100
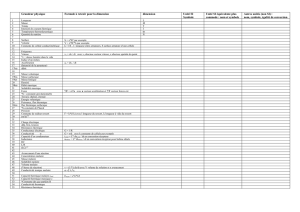
La capacité calorifique C d’une substance est définie par :
C =
dT
Q
variation de température. C s’exprime en cal/deg (J/K en
S.I.).
La chaleur massique, ou capacité calorifique massique,
ou capacité calorifique spécifique c de la substance est
définie par :
c =
m
C
m est la masse de la substance; c s’exprime en cal/g.deg.
(J/Kg.K en S.I.).
La chaleur molaire est la capacité calorifique d’une mole
de la substance, elle est donnée par:
c =
n
C
n est le nombre de moles, n =
M
m
avec M la masse molaire; c
s’exprime en cal/mol.deg. (J/mol.K en S.I.).
En principe, il est nécessaire de distinguer la chaleur
spécifique (ou molaire) cV (respectivement CV) mesurée à
volume constant et la chaleur spécifique (ou molaire) cP
(respectivement CP) mesurée à pression constante.
En effet, suivant la première loi de la
thermodynamique, on a :
dU variation d’énergie interne, P la pression et dV la
variation du volume de la substance.

A pression constante, une dilatation de la substance est
possible (c’est à dire dV > 0); donc la quantité de chaleur
correspondant à un dT donné sera plus grande qu’à volume
constant. On a donc toujours cP > cV. La différence est surtout
marquée pour les gaz, où, dans le cas des gaz parfaits:
cP – cV = R
cP et cV sont les capacités calorifiques molaires et R la
constante des gaz,
R = 1,986 Cal/mole.deg. =
8,314J/mole.deg.
Dans le cas d’un solide, la variation du volume est
négligeable, on peut donc écrire :
CP = CV =
V
T
U
= C
1
/
3
100%