chimie

CHIMIE
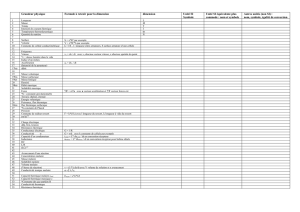
1. Notions de base
• Notions de mole
• Masses atomique et moléculaire relatives
• Nombre d'Avogadro
• Masse volumique et densité
• Symboles chimiques
• Unités du SI et autres unités usuelles
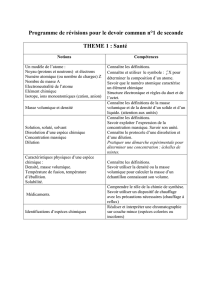
2. Etats de la matière et composition des mélanges
• Corps purs, mélanges, phases
• Propriétés caractéristiques des solides, des liquides et des gaz
• Lois des gaz idéaux
• Molarité
• Pourcentage molaire et massique
• Fraction molaire
• Electrolytes forts et faibles, notion de dissociation
3. Structure de la matière
• Notions d’atome, de molécule et d'élément
• Constitution et organisation de l'atome
• Notion d'ion
• Configuration électronique de la coque valentielle et règle de l'octet
• Constitution du noyau, nombre de masse et nombre atomique
• Tableau de Mendeleïev : notion de famille et de période
• Mise en relation des propriétés des atomes avec leur place dans le tableau périodique
• Les oxydes acides et basiques et les sels
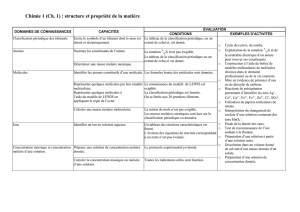
4. La réaction chimique : aspect qualitatif
4.1 Nomenclature chimique générale et organique
• Nomenclature comprenant le symbolisme
• Composés chimiques usuels et la dénomination des fonctions inorganiques et organiques
• Principales Propriétés des fonctions chimiques principales
4.2 notions d'oxydo-réduction
• Equilibre des réactions simples en oxydo-réduction
• Prédiction et interprétation des réactions (données physico-chimiques)

4.3 Acide-base
• Équilibre des réactions simples en acido-basicité
• Prédiction et interprétation des réactions (données physico-chimiques)
5. la réaction chimique : aspect quantitatif
5.1 La réaction chimique
• Établissement d'un bilan massique et molaire à partir d'une réaction à compléter
• Problèmes de gravimétrie et de volumétrie avec mise en œuvre de quantités
quelconques de réactifs (réactif limitant) ; taux de conversion et rendement
5.2. La thermodynamique & l'équilibre chimique
• Notion d'équilibre chimique
• Principe de Le Chatelier
• Constante d'équilibre
1
/
2
100%