effets des perchlorate exposition via l`eau d`a des connaissances sc

4#4
EFFETS DES PERCHLORATES SUR LA SANTÉ ET
EXPOSITION VIA L’EAU D’ALIMENTATION PUBLIQUE :
DES CONNAISSANCES SCIENTIFIQUES INCOMPLÈTES
QUI OUVRENT SUR LA PROBLÉMATIQUE
DES APPORTS EN IODE
En octobre 2012, les préfectures et l’Agence
Régionale de Santé du Nord Pas-de-Calais
ont émis des restrictions d’usage de l’eau
d’alimentation publique dans plusieurs
communes en raison d’une concentration
élevée en ions perchlorates. Cet article dresse
un panorama des connaissances entourant
cette décision.
En Aquitaine et Midi-Pyrénées, les ions
perchlorates ont été mis en évidence dans des
ressources en eau utilisées pour l’alimentation
publique et situées à proximité d’installations
industrielles susceptibles d’en rejeter. La
Lyonnaise de Eaux, qui gérait ces ressources,
a décidé de rechercher les perchlorates dans
plusieurs captages situés en région Nord Pas-
de-Calais. Ces recherches ont abouti à la mise
en évidence de perchlorates dans plusieurs
ressources alimentant la métropole lilloise
Que sont les perchlorates,
où les trouve-t-on et pourquoi
sont-ils utilisés ?
Sous forme solide, les perchlorates se présentent
sous forme de sels dont les plus courants sont
les perchlorates d’ammonium, de potassium et
de sodium. Ils sont naturellement présents en
grande quantité dans quelques rares endroits
comme celui du désert de l’Atacama au Chili.
A cet endroit, ils y sont associés à de grandes
quantités de nitrates qui ont amené ces roches
sédimentaires à être utilisées comme engrais
(salpêtre chilien), notamment aux Etats-Unis.
Dans l’eau, ces sels se dissolvent complètement
et sont à l’origine de la présence de perchlorate
DOSSIER
500
COMMUNES CONCERNÉES
PAR DES RESTRICTIONS
D’EAU DANS LE NORD - PAS
DE CALAIS
+ DE

5
#4
EFFETS DES PERCHLORATES SUR LA SANTÉ ET
EXPOSITION VIA L’EAU D’ALIMENTATION PUBLIQUE :
DES CONNAISSANCES SCIENTIFIQUES INCOMPLÈTES
QUI OUVRENT SUR LA PROBLÉMATIQUE
DES APPORTS EN IODE
sous forme d’anion ClO4-. Celui-ci migre facilement
vers les aquifères où l’on considère qu’il reste très
stable. Il possède des propriétés oxydantes fortes (1).
Le perchlorate d’ammonium peut par ailleurs être
synthétisé et utilisé dans de multiples applications
industrielles mettant en jeu ses propriétés explosives
et détonantes, en particulier dans les milieux militaire
et aérospatial. Il constitue par exemple 70 % du
propergol utilisé comme carburant pour les fusées. Il
est aussi présent dans les dispositifs pyrotechniques,
la poudre de certaines munitions et dans les systèmes
de déclenchement des « airbags ».
Lors de la 1ère guerre mondiale, le perchlorate
d’ammonium fut employé dans 2 types d’obus
de tranchées : le crapouillot français et le minen
allemand, qui n’ont constitué qu’un faible
pourcentage des explosifs tirés. Environ 120 tonnes
de munitions sont encore récupérées chaque
année en région Nord Pas-de-Calais. Le taux de
munitions n’ayant pas explosé durant la guerre 14-
18 est d’environ 30 %.
Effets sur la santé - Toxicité
MÉTABOLISATION
Après ingestion, les ions perchlorates sont
rapidement absorbés au niveau du tractus gastro-
intestinal d’où ils se distribuent dans tout l’organisme
et plus particulièrement au niveau de la thyroïde.
Leur demi-vie sanguine est de l’ordre de 6 à 12h.
Ils sont éliminés dans les urines (ou le lait maternel)
dans lesquelles ils sont couramment mesurés (2).
EFFETS SUR L’ORGANISME
A ce jour, aucune étude scientique n’a pu mettre
en évidence d’effet mutagène ou reprotoxique. Le
principal effet d’intérêt des perchlorates est d’être un
inhibiteur compétitif du passage des ions iodures vers
les cellules de la thyroïde (3). Ils agissent au niveau
d’une protéine membranaire, le symporteur sodium-
iode qui permet à l’iode de pénétrer activement,
contre le gradient de concentration défavorable
à un passage passif (4). L’effet inhibiteur a été
montré dans plusieurs études, dont celle de Greer
en 2002 (5) réalisée chez des volontaires sains avec
l’utilisation d’iode radiomarqué en concentrations
plus élevées que celles rencontrées en expositions
environnementales.
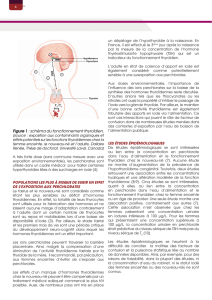
Cet effet biologique est précurseur d’une éventuelle
baisse, selon la dose d’exposition, de la synthèse
des hormones thyroïdiennes T4 (thyroxine) et T3
(triiodothyronine) (gure 1) par les thyrocytes
(cellules de la thyroïde). Ainsi, l’effet suspecté d’une
exposition aux ions perchlorates est une diminution
de l’activité de la thyroïde, pouvant aller jusqu’à
l’hypothyroïdisme. Les hormones thyroïdiennes
ont de multiples fonctions dans le corps humain
et leurs récepteurs sont présents sur tous les tissus.
Elles contribuent, entre autres, au développement
neurologique, à la régulation thermique, à la
régulation de l’activité cardiaque, à la croissance
et au développement osseux (4). Dans l’étude de
Greer, si l’inhibition du passage de l’iode a bien été
mise en évidence, en revanche, aucune diminution
parallèle des hormones thyroïdiennes n’a été
observée.
C. HEYMAN, CELLULE DE L’INSTITUT DE VEILLE SANITAIRE EN RÉGIONS NORD PAS-DE-CALAIS PICARDIE
C. RAOUL, AGENCE RÉGIONALE DE SANTÉ NORD PAS-DE-CALAIS
G. BINET, AGENCE RÉGIONALE DE SANTÉ NORD PAS-DE-CALAIS
P. CHAUD, CELLULE DE L’INSTITUT DE VEILLE SANITAIRE EN RÉGIONS NORD PAS-DE-CALAIS PICARDIE

6#4
Figure 1 : schéma du fonctionnement thyroïdien,
(source : exposition aux contaminants organiques et
effets potentiels sur les fonctions thyroïdiennes chez la
femme enceinte, le nouveau-né et l’adulte, Dallaire
Renée, Thèse de doctorat, Université Laval, Canada)
A très forte dose (sans commune mesure avec une
exposition environnementale), les perchlorates sont
utilisés dans un cadre médical pour traiter certaines
hyperthyroïdies liées à des surcharges en iode (4).
POPULATIONS LES PLUS À RISQUE DE SUBIR UN EFFET
DE L’EXPOSITION AUX PERCHLORATES
Le fœtus et le nouveau-né sont considérés comme
étant les plus sensibles au décit d’hormones
thyroïdiennes. En effet, la totalité de leurs thyrocytes
sont utilisés pour la fabrication des hormones et ne
laissent aucune marge d’adaptation contrairement
à l’adulte dont un certain nombre de thyrocytes
sont au repos et mobilisables lors d’une baisse de
disponibilité d’iode (3). Par ailleurs, le stade fœtal
et les premiers mois de vie sont une période critique
du développement neuro-cognitif dans lequel les
hormones thyroïdiennes ont un effet important.
Les ions perchlorates peuvent traverser la barrière
placentaire. Ainsi, malgré la compensation d’une
diminution de l’activité thyroïdienne fœtale par la
thyroïde de la mère, il recommandé, par précaution,
aux femmes enceintes d’éviter de s’exposer aux
perchlorates.
Les effets d’un manque d’hormones thyroïdiennes
chez le nouveau-né peuvent être compensés par un
traitement médical adéquat commencé le plus tôt
possible. Aussi, de nombreux pays ont mis en place
un dépistage de l’hypothyroïdie à la naissance. En
France, il est effectué le 3ème jour après la naissance
par la mesure de la concentration de l’hormone
thyréostimulante hypophysaire (TSH) qui est un
indicateur du fonctionnement thyroïdien.
L’adulte en état de carence d’apport en iode est
également considéré comme potentiellement
sensible à une surexposition aux perchlorates.
Aux doses environnementales, l’importance de
l’inuence des ions perchlorates sur la baisse de la
synthèse des hormones thyroïdiennes reste discutée.
D’autres anions tels que les thiocyanates ou les
nitrates ont aussi la propriété d’inhiber le passage de
l’iode vers la glande thyroïde. Par ailleurs, le maintien
d’une bonne activité thyroïdienne est également
tributaire des apports en iode via l’alimentation. Ce
sont ces interactions qui jouent le rôle de facteur de
confusion dans de nombreuses études menées dans
des contextes d’exposition par l’eau de boisson de
l’alimentation publique.
LES ÉTUDES ÉPIDÉMIOLOGIQUES
Dix études épidémiologiques se sont intéressées
au lien entre la concentration en perchlorate
dans l’eau d’alimentation et le fonctionnement
thyroïdien chez le nouveau-né (7). Aucune étude
ne montre d’augmentation de la prévalence de
l’hypothyroïdisme congénital. Toutefois, deux études
retrouvent une association entre les concentrations
hydriques et une altération modérée de la fonction
thyroïdienne (8;9). Cinq études se sont intéressées,
quant à elles, au lien entre la concentration
en perchlorate dans l’eau d’alimentation et le
fonctionnement thyroïdien chez la femme enceinte
ou en âge de procréer. Une seule étude montre une
association positive, contrairement aux autres (7).
Cette association n’est observée que chez les
femmes présentant une concentration urinaire
en iodures inférieure à 100 µg/L. Pour les femmes
qui présentaient une concentration supérieure à
100 µg/L, la concentration urinaire en perchlorate
était prédictive du niveau sérique de TSH mais pas du
niveau sérique de T4 (10).
Les études épidémiologiques se heurtent à la
difculté de concilier la maîtrise des facteurs de
confusion et la puissance statistique liée au nombre
de données disponibles. Ainsi, par exemple, pour des
raisons de faisabilité, dans la plupart des études, ni
la consommation d’eau du robinet, ni le statut iodé
des femmes enceintes ou des nouveau-nés ne sont
connus.

7
#4
Statut iodé de la population
Dans une étude récente (12), une baisse modérée
mais signicative de la concentration en thyroxine
(T4 libre et totale) a été observée lorsque les
concentrations urinaires en perchlorate et en
thiocyanate étaient élevées, en même temps que
les concentrations en iode étaient basses. Comme
déjà mentionné, les effets possibles des perchlorates
aux doses environnementales sont à considérer à
l’aune des apports en iode et de l’exposition aux
autres inhibiteurs de la captation d’iode. Un apport
optimal en iode est susceptible de contrebalancer
l’effet des perchlorates.
EN POPULATION GÉNÉRALE
Les données d’iodurie sont disponibles pour 2006-
2007 dans l’aire géographique Nord - Picardie -
Normandie (13). La médiane de l’iodurie est de
146 µg/L (IC 95 % [128-156]) et le 20ème percentile
est de 68 µg/L (IC 95 % [62-83]). Au vu des critères de
l’OMS, le statut nutritionnel en iode est globalement
satisfaisant. Cette situation s’est améliorée au regard
des chiffres de 1999 qui montraient la persistance
d’une décience modérée en iode pour une partie
plus conséquente de la population.
CHEZ LES JEUNES ENFANTS ET LES FEMMES ENCEINTES
OU QUI ALLAITENT
Chez les jeunes enfants de 10 jours à 6 ans, une étude
menée en 2000-2001 dans la région lilloise a fait état
d’une médiane de 196 µg/L et d’un pourcentage
d’enfant carencé (iodurie inférieure à 50 µg/L) de
7 % (14). En 2005, pour des enfants de moins de 1
an, la médiane était de 328 µg/L et le pourcentage
d’enfants carencés de 11 % (15).
Pour les femmes enceintes ou qui allaitent, l’OMS (16)
recommande des apports en iode de plus de 250 µg/j
alors qu’ils ne sont que de 150 µg/j habituellement pour
les adultes. Une iodurie de moins de 150 µg/L et de
moins de 100 µg/L est considérée comme insufsante
respectivement pour les femmes enceintes et
pour celles qui allaitent. Il n’existe pas de données
d’iodurie chez les femmes enceintes dans le nord de
la France. Néanmoins, dans le sud de la France (17),
dans une zone où l’iodurie en population générale
est proche de celle du Nord, le pourcentage de
femmes enceintes dont l’iodurie, mesurée en 2007-
08, est insufsante, c’est-à-dire inférieure à 150 µg/L,
est de 66 % ; la médiane d’iodurie étant de 116 µg/L.
Les apports iodés sont souvent insufsants pendant
la grossesse comme cela a été déjà plusieurs fois
dénoté en Europe de l’ouest.
SOURCES D’IODE
L’iode est principalement apporté par l’alimentation.
Le lait est le principal contributeur en France, du
fait de l’enrichissement des fourrages en iode et
de l’utilisation de produits de désinfection iodés.
Les aliments les plus riches sont cependant les
produits de la mer, crustacés, poissons et algues (la
consommation de ces dernières explique l’iodurie
souvent élevée dans certains pays, comme le
Japon). L’enrichissement du sel en iode tel que
recommandé en France contribue à lutter contre la
décience en iode. Pour les femmes enceintes, une
supplémentation par compléments alimentaires est
recommandée (18).

8#4
Relation dose - effet
Les organismes (OMS, EPA, OEHHA, Ineris) qui se sont
attachés à proposer une dose journalière admissible
ont retenu l’inhibition de la capture de l’iode par la
thyroïde comme effet sanitaire critique. L’étude de
Greer est la seule étude prise systématiquement en
compte par les différents organismes (3). Elle présente
toutefois certaines limites : (i) elle repose sur un faible
nombre de personnes, (ii) elle est de relative courte
durée (14j), (iii) les adultes sains de l’étude ne sont
pas représentatifs du fœtus ou du nouveau-né, (iv)
les apports en ions perchlorates par voie alimentaire
non hydrique n’ont pas été pris en compte et (v)
elle ne donne pas d’information sur le statut iodé
(concentrations sériques ou urinaire en ions iodures)
des participants. De cette étude, la plupart des
organismes (EPA, Anses, Ineris, OEHHA,…) déduisent
une dose journalière admissible de 0,7 µg/ kg pc/j (3)
alors que l’OMS retient 10 µg/kg pc/j (11), sur la base
d’une interprétation différente de la gravité de l’effet
critique retenu.
Exposition globale aux perchlorates
L’exposition globale aux perchlorates provient à la
fois de l’apport hydrique et des apports alimentaires
non hydriques. Aucune donnée n’est disponible
en France sur les concentrations existantes dans
l’alimentation. Aux Etats-Unis, les ions perchlorates
ont été détectés dans de nombreux aliments. Pour
les enfants, les produits laitiers seraient la principale
source d’exposition aux perchlorates alors que
chez les adultes ce serait les légumes. L’Anses (3)
a considéré que la part de l’eau dans les apports
alimentaires quotidiens en perchlorates était de 60 %
pour les adultes et de 100 % pour les nourrissons, nourris
exclusivement au sein ou avec des laits maternisés.
Pour l’OMS, les estimations des apports provenant
de l’eau bue et des aliments sont comprises entre
0,1 µg/kg pc/j et 0,7 µg/kg pc/j, soit des niveaux
inférieurs à 10 µg/kg pc/j. Elle considère ainsi que
l’exposition alimentaire ne constitue pas un problème
de santé (11).
Valeur limite dans l’eau potable
Pour dénir les seuils proposés, l’Anses a fait
l’hypothèse d’une consommation quotidienne
d’eau de 0,75 L pour les nourrissons et de 2 L pour
les adultes. A partir des données de poids corporels
xés conventionnellement à 5 kg pour les nourrissons
et à 60 kg pour les adultes, l’Anses a ainsi déterminé
la concentration maximale admissible dans l’eau de
14,7 (arrondi à 15 µg/L) pour les adultes et de 4,7 µg/L
(arrondi à 4 µg/L pour être plus protecteur) pour les
nourrissons.
Aucune limite n’est indiquée dans la réglementation
européenne pour les perchlorates dans l’eau
potable. En revanche, aux Etats-Unis, bien qu’il
n’existe pas encore de limite fédérale, la procédure
d’élaboration est en cours. La valeur de 15 µg/L est
proposée au niveau fédéral mais certains organismes
(OEHHA, Mass Dep) et quelques Etats ont retenu des
valeurs plus faibles (3).
Situation de l’eau d’alimentation publique
Dans l’eau d’alimentation publique en région
Nord Pas-de-Calais, les ions perchlorates ne sont
pas détectés dans de nombreuses communes
(concentration inférieure aux seuils de détection de
l’ordre du 1µg/L). Le maximum observé est de 77 µg/L.
Plus de cinq cents communes ont été initialement
et sont toujours, pour la plupart, concernées par
une restriction de l’usage de l’eau du robinet pour
les personnes sensibles. Au total, environ 9000
femmes et 5 000 nourrissons seraient potentiellement
concernés par cette restriction d’usage. La carte des
concentrations en perchlorate montre une similitude
visuelle, imparfaite mais frappante, avec celle des
zones de combats de la 1ère guerre mondiale dans
la région (voir cartes 1 et 2 ci- contre). L’utilisation de
munitions perchloratées n’a pas été majeure mais
est avérée (voir plus haut) et constitue la meilleure
explication de la cartographie des pollutions par les
perchlorates.
D’autres sources anciennes et localisées ont pu
également contribuer à la contamination des
sols et, par lixiviation, des aquifères. La disparition
des ressources contaminées en perchlorate en
remontant de l’ancien bassin minier vers la région
lilloise s’explique, non pas par l’arrêt du front de
guerre, mais par la géologie du sous-sol. La nappe
de la craie devient progressivement captive en
s’enfonçant sous les couches géologiques du tertiaire
dont certaines sont argileuses. Le milieu devient alors
fortement réducteur (phénomène de dénitrication
naturel).
 6
6
 7
7
 8
8
1
/
8
100%