Absorption entérocytaire et passage vers le
publicité

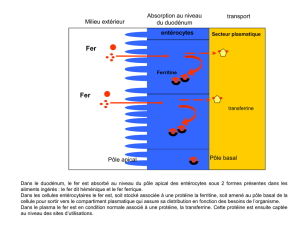
Absorption entérocytaire et passage vers le plasma Fer héminique Fe3+ Dcytb Fe2+ Pôle apical HCP DMT1 Dégradation de l’hème recyclage du fer entérocyte ferritine haephastine Ferroportine Pôle basal Fe3+ Fe2+ Secteur plasmatique Au pôle apical des entérocytes l’hème (issue se lie à son récepteur HCP (Hème Carrier Protein) puis va être dégradé par une enzyme l’hème oxygénase, libérant ainsi le fer qui s’associe alors à la ferritine ou est utilisé pour les besoins cellulaires. Par ailleurs le fer ferrique (Fe3+) présent dans l’alimentation d’origine végétale est réduit en fer ferreux (Fe2+) par une enzymes Dcytb et entre dans la cellule en utilisant un transporteur d’ion divalent DMT1. Vraisemblablement des processus d’endocytose participent au transport du fer dans la cellule. Le fer sera alors soit stocké fixé à la ferritine soit envoyé à la membrane basale de l’entérocyte et pris en charge par une autre protéine de transport, la ferroportine. C’est elle qui permet la sortie du fer de la cellule vers le compartiment plasmatique. Le fer ferreux étant très réactif il sera oxydé en fer ferrique par l’héphastine et pris en charge par la transferrine. Absorption entérocytaire et passage vers le plasma Fer héminique Fe3+ Dcytb HCP Fe2+ Pôle apical DMT1 Dégradation de l’hème recyclage du fer entérocyte ferritine haephastine Ferroportine Pôle basal holotransferrine Fe3+ Fe2+ apotransferrine Secteur plasmatique La transferrine est en condition normale le transporteur du fer dans le plasma. C’est une protéine synthétisée par le foie. On parle d’apotransferrine (transferrine sans molécule de fer associée) et d’holotransferrine lorsqu’elle est associée au fer. Cette dernière est captée par des récepteurs à la transferrine (TFR1 et TFR2) en fonction des besoins des différents organes et tissus.