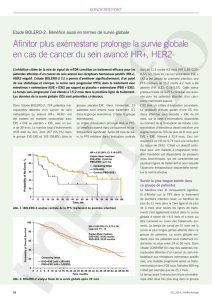
Afinitor® et l`exémestane doublent la survie sans progression

22 03
_ 2013 _ info@onkologie
RAPPORT SPÉCIAL
Suppression de la résistance endocrine
Afi nitor
® et l’exémestane doublent
la survie sans progression
En raison de l’absence d’options thérapeutiques
spécifi ques pour les patientes endocrinorésis-
tantes, ce sont surtout d’autres traitements en-
docrines comme le fulvestrant, un antagoniste
des récepteurs aux œstrogènes qui, contraire-
ment au tamoxifène, ne présente pas d’activité
agoniste, ou exémestane, un inhibiteur stéroï-
dien de l’aromatase, qui sont utilisés. L’effi ca-
cité clinique de ces traitements, examinée au
cours de plusieurs études, est apparue simi-
laire. Au cours de deux 2 études, l’effi cacité cli-
nique du fulvestrant et de l’exémestane a été
testée auprès de patientes souffrant de pro-
gression sous traitement par des NSAI. Chez
ces patientes post-ménopausées avec un can-
cer du sein HR positif et résistant à un traite-
ment par NSAI, le fulvestrant est apparu aussi
effi cace que l’exémestane au cours de l’étude
EFFECT(4), avec une survie sans progression
moyenne de 3,7 mois dans les deux groupes.
Au cours de l’étude SoFEA, le fulvestrant en
association avec l’anastrozole est apparu aussi
effi cace que le fulvestrant seul, ou l’exémestane
(durée jusqu’à la progression: 4,4 mois contre
4,8 mois contre 3,4 mois) (5). En revanche,
dans l’étude CONFIRM, au cours de laquelle
deux dosages différents de fulvestrant (250 mg
Une partie non négligeable des patientes avec cancer du sein au stade précoce souffrent
de récidive. Pour ces patientes avec cancer du sein avancé positif pour les récepteurs hor-
monaux (HR+), le traitement endocrine représente la pierre angulaire de la thérapie. Chez
les patientes post-ménopausées, les inhibiteurs de l’aromatase non stéroïdiens (NSAI)
comme le létrozole et l’anastrozole sont les médicaments de choix pour le traitement de
première intention. Les inhibiteurs de l’aromatase se sont révélés supérieurs au tamoxifène
en termes de taux de réponse et de durée jusqu’à la progression. Néanmoins, une large
majorité de patientes avec cancer du sein HR+ avancé souffrent de progression sous trai-
tement par des inhibiteurs de l’aromatase. Quelles sont les options thérapeutiques à la dis-
position des patientes ayant développé une résistance au traitement par un NSAI? (1–3).
contre 500 mg) ont été comparés, seulement
42,5% des patientes avaient reçu un inhibiteur
de l’aromatase en tant que dernier traitement
antérieur. Bien que toute la population de pa-
tientes de l’étude ayant reçu 500 mg ait profi té
d’une différence d’un mois au niveau de la sur-
vie sans progression (5,5 contre 6,5 mois; HR =
0,80; IC à 95%: 0,68 à 0,94; P=0,006), une dif-
férence importante a été notée en fonction du
traitement antérieur. L’analyse des sous-groupes
montre que ces différences signifi catives sont
observées seulement chez les patientes prétrai-
tées par un médicament anti-œstrogénique et
non chez celles ayant suivi un traitement anté-
rieur par un inhibiteur de l’aromatase (6).
La survie globale n’a pas été signifi cative-
ment différente sur le plan statistique entre les
deux groupes. Il a été montré au cours d’études
que des interactions étroites entre la voie de
signalisation par les œstrogènes et la voie de
signalisation PI3K-mTOR ainsi que son hyper-
activation représentent des mécanismes im-
portants pour l’apparition de la résistance
endocrine. Une stratégie thérapeutique pre-
nant les deux voies de signalisation en compte
semble donc être une approche prometteuse
pour les patientes.
L’évérolimus est un inhibiteur allostérique
de mTOR et peut donc prévenir l’activation oes-
trogénodépendante du récepteur aux œstro-
gènes par mTOR (fi g. 1). Les premières études
précliniques ont confi rmé que le blocage de
ce circuit important de résistance endocrine
conduit à la suppression de cette dernière par
l’évérolimus et donc au renforcement de l’effi -
cacité du traitement endocrine (7).
Étude BOLERO: amélioration
hautement signifi cative
de la survie sans progression
La réussite clinique de la stratégie de suppres-
sion de la résistance endocrine par le blocage
de mTOR a été démontrée par deux études
de phase II (8,9), suivies par une étude de
phase III appelée BOLERO-2 (Breast cancer
trials of OraL EveROlimus-2) (10). Au cours
de cette dernière, l’effi cacité et la sécurité
de l’évérolimus en association avec l’exémes-
tane ont été comparées avec celles du traite-
ment par exémestane seul chez des femmes
post-ménopausées avec cancer du sein mé-
tastatique positif pour les récepteurs aux œs-
trogènes (ER-positif) et HER2-négatif ou local
avancé avec récidive ou progression sous un
traitement antérieur par létrozole ou anastro-
zole (10). Les patientes avaient reçu à 74%
ou 75% un NSAI comme dernier traitement
antérieur et 21% des patientes n’avaient reçu
encore aucun traitement contre leur mala-
die en progression. Seulement 54% ou 53%
des patientes avaient reçu plus de trois traite-
ments antérieurs, y compris des traitements
d’appoint. 16% des patientes avaient été trai-
tées par le fulvestrant, 47% avaient reçu éga-
lement du tamoxifène et seulement 26% des
patientes avaient déjà suivi une chimiothéra-
pie contre leur maladie en progression.
Le cri-
Fig. 2: PFS après évaluation centrale dans BOLERO-2 (10)
Fig. 1: Représentation schématique du double mécanisme d’action

info@onkologie
_ 03 _ 2013 23
RAPPORT SPÉCIAL
tère primaire était la survie sans progression
(PFS). Les résultats concernant la PFS sous
évérolimus + exémestane contre l’exémes-
tane seul sont représentés dans la fi gure 2.
Le critère primaire (PFS) a été atteint au
cours de cette étude. Selon l’évaluation cen-
trale, la PFS a été de 11 mois pour l’évérolimus
plus exémestane contre 4,1 mois sous pla-
cebo plus exémestane (HR 0,38; 0,27–0,47,
p<0,001). La réduction du risque de progres-
sion a donc été de 62%. Ces résultats signi-
fi ent pour les patientes une multiplication par
plus de 2 de la PFS sous le traitement par évé-
rolimus et presque un an de survie sans pro-
gression. Les résultats ont été homogènes
et signifi catifs avec une réduction du risque
presque identique dans tous les sous-groupes.
Concernant la qualité de vie en relation
avec la santé, le traitement associé par évé-
rolimus et exémestane a également donné de
meilleurs résultats par rapport au monotraite-
ment par exémestane au cours de BOLERO-2.
La durée moyenne jusqu’à une aggravation
défi nitive (Time to Defi nite Deterioration, TDD)
a été de 8,3 mois sous l’association évérolimus
plus exémestane contre 5,8 mois sous place-
bo plus exémestane (HR 0,74, p=0,0084)
(11). Ces observations suggèrent que l’aug-
mentation claire de l’effi cacité clinique a amé-
lioré la qualité de vie en relation avec la santé
dans le groupe sous EVE + EXE en dépit de
l’incidence accrue des toxicités de grade 3
ou 4 observées dans ce groupe. Le tableau 1
donne une vue d’ensemble des résultats des
différents traitements.
Sécurité du traitement
par l’évérolimus
La plupart des effets indésirables ont été légers
et de grade 1 ou 2. Le profi l de sécurité est com-
patible avec les autres indications d’Afi nitor®.
On a observé surtout des stomatites, des diar-
rhées, une fatigue et des éruptions cutanées.
Le tableau 2 donne une vue d’ensemble des ef-
fets indésirables les plus fréquents.
Le taux d’interruptions à cause des ef-
fets indésirables associés à Afi nitor® a été
de 10% (11). Outre la pneumonie non infec-
tieuse, la stomatite est également un effet de
classe: il a en effet pu être démontré que les
ulcères étaient plutôt similaires aux aphtes et
qu’ils différaient de la mucosite induite par
la chimiothérapie. Ils sont moins profonds
et guérissent plus rapidement (12). Afi n de
les minimiser, une bonne hygiène buccale et
le renoncement aux plats/boissons épicés,
acides, durs et chauds sont recommandés.
Les stratégies de gestion du traitement telles
qu’une bonne information des patientes sont
bénéfi ques pour la réussite optimale de la
thérapie (13).
Conclusion
L’évérolimus en association avec un inhibi-
teur de l’aromatase prolonge signifi cativement
la survie sans progression de presque un an
des patientes avec cancer du sein HR+ avan-
cé ayant souffert d’une progression ou d’une
récidive sous traitement par un inhibiteur de
l’aromatase. Avec cette multiplication de la sur-
vie sans progression par plus de deux par rap-
port au monotraitement endocrine, la qualité de
vie a été conservée en dépit de l’augmentation
partielle de l’incidence des effets indésirables.
Les résultats de cette étude posent un véritable
jalon dans le traitement des patientes avec can-
cer du sein HR+, ce qui devrait être envisagé
comme un changement de paradigme (13).
Références:
1. Bonneterre J et al Anastrozole is superior to tamoxi-
fen as fi rst-line therapy in hormone receptor posi-
tive advanced breast carcinoma: Results from two
randomized trials designed for combined analysis.
Cancer 2001; 92: 2247-2258
2. Mouridsen H et al. Phase III study of letrozole ver-
sus tamoxifen as fi rst-line therapy of advanced
breast cancer in post-menopausal women: Analysis
of survival and update of effi cacy from the Interna-
tional Letrozole Breast Cancer Group. J Clin Oncol
2003;21: 2101-2109
3. Paridaens R et al. Mature results of a randomized
phase II multicentre study of exemestane versus ta-
moxifen as fi rst-line hormone therapy for postme-
nopausal women with metastatic breast cancer.
Ann Oncol 2003;14:1391-1398
4. Ghia S et al. Double-blind, randomized placebo
controlled trial of fulvestrant compared with exeme-
stane after prior nonsteroidal aromatase inhibitor
therapy in postmenopausal women with hormone
receptor-positive, advanced breast cancer: results
from EFFECT. J Clin Oncol 2008; 26:1664-1670
5. Dodwell A et al. Combining fulvestrant (Faslodex_)
with Continued oestrogen suppression in endocri-
ne-sensitive advanced breast cancer: the SoFEA
TrialClinical Oncology (2008) 20: 321e324
6. Di Leo A et al. Results of the CONFIRM Phase III
trial comparing fulvestrant 250mg with fulvestrant
500mg in postmenopausal women with estrogen
receptor-positive advanced breast cancer. J Clin
Oncol 2010;28:4594-4600
7. Boulay A et al. Dual inhibition of mTOR and estro-
gen receptor signalling in vitro induces cell death in
models of breast cancer. Clin Cancer Res 2005; 11:
5319-5328
8. Baselga J et al Phase II randomized study of neo-
adjuvant everolimus plus letrozole compared with
placebo plus letrozole in patients with estrogen-po-
sitive breast cancer. J Clin Oncol 2009; 27: 2630-
2637
9. Bachelot T et al. Randomized phase II trial of eve-
rolimus in combination with tamoxifen in patients
with hormone receptor-positive human epidermal
growth factor receptor 2-negative metastatic breast
cancer with prior exposure to aromatase inhibitor: a
GINECO study. J Clin Oncol 2012;30:2718-2724
10. Baselga J et al. Everolimus in postmenopausal hor-
mone receptor-positive advanced breast cancer.
N Engl J Med 2012; 366:520-529
11. Burris HA et al. Health-related quality of life of pa-
tients with advanced breast cancer treated with
everolimus plus exemestane versus placebo plus
exemestane in the phase 3, randomized, cont-
rolled, BOLERO-2 trial. Cancer 2013; doi: 10.1002/
cncr.28010. [Epub ahead of print]
12. Sonis S et al. Preliminary characterization of lesi-
ons associated with inhibitor of mammalian tar-
get of Rapamycin in cancer patients. Cancer
20120;116:210-215
13. Gnant M. The role of mammalian target of rapamy-
cin (mTOR) inhibition in the treatment of advanced
breast cancer. Curr Oncol Rep 2013;15:14-23
IMPRESSUM
Rapport: Prof. Dr Dr h.c. Walter F. Riesen
Rédaction: Christian Heid
Avec le soutien de Novartis Pharma Schweiz AG, Rotkreuz
© Aerzteverlag medinfo AG, Erlenbach
Médicament contre comparateur Durée jusqu’à la
progression (mois)
Etude
Fulvestrant + anastrozole contre fulvestrant 4,4 vs 4,8 SoFEA (5)
Fulvestrant contre exémestane 4,8 contre 3,4 SoFea
Fulvestrant contre exémestane 3,7 contre 3,7 EFECT (4)
Evérolimus contre exémestane 11 contre 4,1* BOLERO-2 (10)
*Survie sans progression (PFS)
Tab. 1: Durée jusqu’à la progression ou survie sans progression dans diverses études
sur le cancer du sein HR+ avancé
Tab. 2: BOLERO-2 – Effets indésirables les plus fréquents (incidence 25%) sous Afi nitor®
plus exémestane (10)
Effets indésirables Afi nitor® + exémestane Exémestane + placebo
Tous les grades (%) Grades 3/4(%) Tous les grades (%) Grades 3/4(%)
Stomatite 56 8/0 11 1/0
Diarrhée 30 2/<1 16 1/0
Fatigue 33 3/< 1 26 1/0
Hyperglycémie* 13 4/<1 2 <1/0
Diminution de l’appétit 29 1/0 10 0/0
Eruptions cutanées 36 1/0 6 0/0
Pneumonie non infectieuse*
12 3/0 0 0/0
Toux 22 1/0 11 0/0
Diminution du poids 19 1/0 5 0/0
*Effet indésirable cliniquement important avec une incidence < 25%
1
/
2
100%