AE_B08_preparation derive chlore - leprof

Page 1 sur 1
Les dérivés chlorés sont, entre autres, très utilisés comme
intermédiaires de synthèse et solvants. Ils doivent être
synthétisés industriellement. Comment préparer un
dérivé chloré?
Présentation
Le 2-méthylpropan-2-ol réagit avec l'acide chlorhydrique
pour donner du 2-chloro-2-méthylpropane et de l'eau.
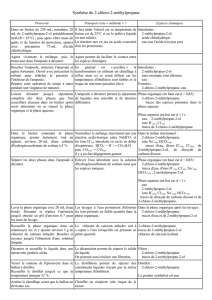
Spectre infrarouge du 2-méthylpropan-2-ol.
1- Repérer la (les) bande(s) d'absorption caractéristique(s) du réactif sur le spectre d'absorption.
Les molécules de 2-méthylpropan-2-ol sont-elles liées par des liaisons hydrogène?
2- Écrire l'équation de la réaction. Comment est modifiée la structure au cours de la réaction?
Manipulation
- Observer les pictogrammes des réactifs utilisés. Rechercher les risques que peut présenter leur
utilisation et s'organiser en conséquence.
- Dans un erlenmeyer contenant un barreau aimanté, introduire, à l'éprouvette graduée et avec
précaution, 30 mL de solution concentrée d'acide chlorhydrique (11 mol.L-1), puis 15,0 mL de
2-méthylpropan-2-ol.
- Adapter un condenseur à air à l'erlenmeyer et placer l'ensemble sur un agitateur magnétique en
fixant l'erlenmeyer à un support vertical. Agiter pendant 20 minutes.
- Retirer le barreau aimanté, puis transvaser avec précaution le mélange dans une ampoule à décanter.
Identifier la phase aqueuse et l'évacuer.
- Ajouter à la phase organique 25 mL de solution concentrée d'hydrogénocarbonate de sodium,
Na+(aq) + HCO3-(aq). Lorsque le dégagement de dioxyde de carbone cesse, boucher l'ampoule, la
retourner en maintenant bien le bouchon et ouvrir le robinet pour dégazer. Agiter alors doucement. A la
fin du dégagement gazeux, refermer l'ampoule, la replacer sur son support, la déboucher, puis évacuer
la phase aqueuse.
- Ajouter à la phase organique 10 mL d'eau distillée, agiter comme précédemment, laisser
décanter, puis évacuer la phase aqueuse. Éliminer l'eau de l'extrémité inférieure de l'ampoule à décanter
avec du papier absorbant.
- Introduire deux spatules de sulfate de magnésium anhydre MgSO4(s) dans un erlenmeyer sec.
- Recueillir la phase organique, boucher et agiter pendant 5 minutes. Faire vérifier la qualité du séchage
par le professeur.
- Filtrer le mélange en récupérant le filtrat dans un erlenmeyer sec pesé au préalable. Adapter un
bouchon.
Exploitation
- Décrire par des schémas et de façon succincte le mode opératoire de la synthèse
L'ion hydrogénocarbonate réagit avec les ions hydrogène H+(aq) pour donner du dioxyde de carbone et
de l'eau. Écrire l'équation de la réaction.
Le sulfate de magnésium anhydre permet de sécher la phase organique grâce à la réaction d'équation :
MgSO4 (s) + 7 H2O(l) —> MgSO4,7 H2O(s) En quoi consiste le séchage de cette phase?
Quelles techniques permettraient de vérifier la nature du produit obtenu?
Déterminer le rendement de la synthèse.
En utilisant un des trois termes, « addition », « substitution » ou « élimination », rédiger une phrase
décrivant la nature de la réaction de synthèse.
Préparation d’un dérivé chloré
Activité
Expérimentale B08
Densité
Téb (°C)
2-méthylpropan-2-ol
0,781
83
2-chloro-2-méthylpropane
0,836
51
1
/
1
100%