stomates

La différenciation des stomates : un exemple d’étude de la
coordination spatio-temporelle chez les Angiospermes
Les Angiospermes se caractérisent par leur développement post-embryonnaire, localisé
essentiellement dans les méristèmes. Cependant, des événements de prolifération et de
différenciation cellulaires, parfois majeurs mais dans tous les cas très importants pour le cycle
de vie de la plante, sont également présents au sein de quelques cellules, tissus et organes bien
définis (méristèmes secondaires, cellules et tissus reproducteurs, ….).
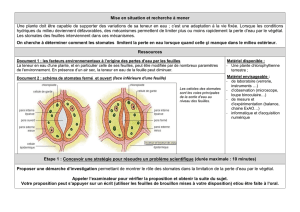
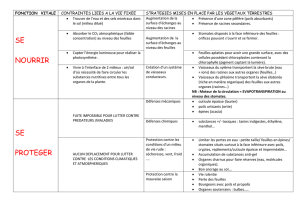
Les stomates, structures foliaires très spécialisées, ont comme principale fonction de
percevoir et de réguler le flux de gaz à la fois vers l’intérieur (gaz carbonique) et hors de la
feuille (eau) (cf figure). Notons également le fait que les hyphes mycéliens des champignons
pathogènes pénètrent fréquemment dans la plante par le stomate.
QuickTime™ et un
décompresseur TIFF (LZW)
sont requis pour visionner cette image.
A B C
Figure 1 : Stomates fermés (A, C) et ouvert (B)
La forme, la répartition des stomates, leur ouverture et leur fermeture varient en fonction
d’une très large gamme de signaux intracellulaires (calcium) ou même climatiques
(Hetherington and Woodward, 2003 ; Bergmann, 2004). Ainsi, une carence en eau entraîne
leur fermeture. L’épiderme de la face adaxiale (tournée vers la tige) et celui de la face
opposée, la face abaxiale, de la feuille de rosette d’Arabidopsis, possèdent pratiquement le
même nombre de stomates par unité de surface, autour de 150-160 par mm2 (Berger et
Altmann, 2000). Cependant le nombre de stomates par unité de surface varie fortement selon
les conditions de culture, le génotype utilisé, l’environnement, et selon que l’on observe
l’épiderme d’un cotylédon, d’une feuille de rosette, ou bien d’une feuille de la hampe florale,
entre 60 et près de 1500 stomates par mm2 (Figure 2).

Figure 2 : Epiderme foliaire de la variété Columbia (Arabidopsis thaliana)
Mise en place des stomates
La formation des stomates requiert des divisions cellulaires à partir de leur cellule précurseur,
le méristémoïde (Figure 3). De telles divisions surviennent durant la phase d’étalement de la
feuille, sur une période de plus de deux semaines (Donnelly et al., 1999). Chez Arabidopsis,
la petite cellule en général “triangulaire“, résultant d’une division asymétrique d’une cellule
de l’épiderme foliaire est nommée méristémoïde primaire, du fait qu’elle continue à se diviser
alors que les cellules alentour ont cessé leur division. Ce méristémoïde subira de une à trois
mitoses pour former les cellules de garde des stomates (Donnelly et al., 1999). Chacune de
ces divisions produit une cellule épidermique et une cellule à destinée méristémoïde (cf figure
3). Cette observation soulève donc la question fondamentale du ou des mécanismes assurant
le maintien de l’identité méristémoïde. L’observation à montré que les méristémoïdes se
formaient à la suite d’une division cellulaire asymétrique de leur cellule mère, tant sur le plan
de la géométrie qu’à celui du devenir des cellules filles. De même, leur maintien durant une à
trois mitoses est lié à la division asymétrique du méristémoïde lui-même.

1M
12
M
12
3
M
Cellule mère du
méristémoïde
DA
DA
DA
DA
DA : division
asymétrique
DS : division symétrique
du méristémoïde.
M : méristémoïde
MS : méristémoïde
secondaire
1 à 4 : cellules
épidermiques en puzzle
12
3
4M
64,4 %
1
28,9 %
1
2
6,7 %
1
2
3
1
2
3
4
1
MS
DA
DS
DS
DS
DS
Figure 3 : Formation des stomates.
Noter le fait que le complexe stomatique est anisocytique (cellules 1 à 4 de tailles différentes)

Ainsi que le décrivent Zhao et Sack (1999) : “Le premier événement cytologique détecté dans
la cellule mère du méristémoïde (ou CMM) est la polarisation du cytoplasme. En effet, avant
la division asymétrique, le noyau et une large part du cytoplasme sont localisés d’un côté de
la cellule, proche du futur site de division, notamment du futur plateau cellulaire, endroit
marqué par une fine bande préprophasique. Les méristémoïdes nouvellement formés sont des
cellules à cytoplasme dense, à paroi nouvelle fine, et dont le noyau est situé au centre de la
cellule. Par contre la cellule sœur en puzzle, issue de la division de la CMM est largement
vacuolisée, avec une fine zone cytoplasmique sur le pourtour cellulaire“. Enfin, la division
finale du méristémoïde donnant les deux cellules de garde du stomate, est une division
symétrique.
Un aspect fondamental de la mise en place des stomates est celui de la présence d’un espace
autour de chaque stomate (pas de stomates adjacents), avec entre deux stomates au moins une
cellule épidermique en puzzle (ou « pavement cell »). Cet espacement des stomates (cf figure
2) est caractéristique (Larkin et al., 1997). Il est fréquent de lire que les stomates sont répartis
aléatoirement sur l’épiderme. Mais ceci n’est vrai qu’en première approximation. En fait,
lorsque les plantes poussent en conditions naturelles, la répartition des stomates sur
l’épiderme n’est pas parfaitement aléatoire, suggérant l’existence d’un contrôle génétique de
l’organisation spatiale des stomates. Chez Arabidopsis et d’autres dicotylédones, il existe un
second type de méristémoïde nommé méristémoïde satellite, ou secondaire, résultant de la
division asymétrique d’une cellule adjacente au stomate. La polarité des divisions conduisant
à la formation du méristémoïde satellite est finement régulée. La division asymétrique de la
cellule adjacente au stomate est orientée de telle façon d’une part que la plus petite cellule
fille (le méristémoïde secondaire) qui va donner un stomate secondaire, se localise loin du
premier stomate, et d’autre part que la plus grande cellule fille sépare ce stomate secondaire
du stomate précédent. Ainsi, qu’il s’agisse des stomates provenant du méristémoïde primaire
ou de ceux issus du méristémoïde satellite, le nombre et la distribution, la position, des
stomates sont régulés durant le développement foliaire (Nadeau and Sack, 2002 ; Geisler
et al., 2000). Notons que les petites cellules que sont les méristémoïdes possèdent des noyaux
dont la quantité d’ADN demeure au niveau 2C, alors que les (parfois très) larges cellules en
puzzle atteignent jusqu’à 16C (Melaragno et al., 1993).
Les variations du nombre de stomates par unité de surface peuvent résulter soit de
modifications de la taille des cellules épidermiques, soit du nombre de cellules en puzzle, soit
enfin du nombre de stomates. L’indice stomatique (IS) a été conçu par Salisbury (1927), tel

que IS = nombre de stomates / nombre de cellules en puzzle + nombre de stomates, pour
pouvoir analyser les événements qui affectent l’épiderme.
Signalisation de la mise en place des stomates
Récemment, des travaux de génétique du développement ont permis l’obtention et la
caractérisation moléculaire et cellulaire de mutants extrêmement intéressants. En effet, les
mutations des gènes YODA (YDA), une kinase de type MAP kinase kinase kinase (Bergman et
al., 2004 ; Lukowitz et al., 2004), TOO MANY MOUTHS (TMM), un récepteur
transmembranaire à LRR (Nadeau and Sack, 2002), STOMATAL DENSITY AND
DISTRIBUTION (SDD1), une subtilisine (Berger and Altmann, 2000), FOUR LIPS
(FLP)(Yang and Sack, 1995 ; Larkin et al., 1997), affectent la production (nombre) et la
position des stomates. Les mutants tmm et flp contreviennent à la règle qui assure que les
stomates ne sont pas en contact (Geisler et al., 1998). L’hypothèse actuelle est celle d’un
ligand (SDD1), perçu par le récepteur TMM, déclenchant la transmission d’un signal qui
voyage par le biais de la kinase YODA, puis de facteurs de transcription tels que
FAMA (Sack, 2004 ; Serna and Fenoll, 2002 ; Serna 2004). La position de FLP est encore
indéterminée, mais FLP est génétiquement en aval de YODA (Bergmann et al., 2004). Le
signal transmis au noyau de la cellule mère du méristémoïde est une information dictant à la
fois son identité de CMM et son devenir en terme de polarité des divisions (division
produisant un méristémoïde, division donnant les cellules de garde). Des résultats très récents
viennent de conforter l’implication de récepteurs impliqués dans la signalisation
intercellulaire. En effet, Shpak et al. (2005) montrent que des interactions complexes entre le
récepteur TMM et les récepteurs kinase à LRR ERECTA, ERL1 et ERL2, ces deux derniers
très proches d’ERECTA, participent à cette voie de signalisation (cf figure 4). Enfin, Boudolf
et al. (2004) montrent que la cycline-dependent kinase (CDK) CDKB1;1 est fortement
exprimée dans les cellules de garde et dans les cellules précurseurs des stomates. De plus, une
expression réduite de cette CDK entraine une diminution de l’indice stomatique, par blocage
précoce de la division du méristémoïde et inhibition de la formation de méristémoïde satellite
(Boudolf et al., 2004). Les dernières données montrent que FLP est en fait un facteur de
transcription de type R2R3 MYB (MYB 124), qui possède un paralogue capable de
complémenter sa fonction, MYB 88 (Lai et al., 2005). Ces deux MYB agissent de concert
pour limiter la division. Une des cibles de ces facteurs de transcription pourrait être
CDKB1;1.
 6
6
 7
7
1
/
7
100%