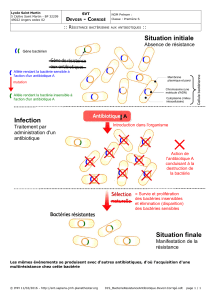
Infections sévères à bactéries à Gram négatif

INFECTIOLOGIE 619
INFECTIONS SEVERES A BACTERIES
A GRAM NEGATIF: MONO- OU BITHERAPIE
P. Moine 1 et M. Wolff 2 - 1Département d’Anesthésie-Réanimation de Bicêtre, Hôpital
de Bicêtre, 78 rue du Général Leclerc, 94275 Le Kremlin-Bicêtre. 2Service de Réani-
mation des Maladies Infectieuses, CHU Bichat Claude-Bernard, 75018, Paris.
INTRODUCTION
L’optimisation des traitements anti-infectieux est une nécessité. Cette optimisation
a pour objectifs l’amélioration de l’efficacité et de la tolérance de ces traitements. Les
moyens sont : le choix des antibiotiques, la recherche des posologies nécessaires et des
meilleurs rythmes d’administration, la détermination des durées de traitement néces-
saires et suffisantes, et la définition stricte des seules situations justifiant le recours aux
associations d’antibiotiques.
1. JUSTIFICATION DES ASSOCIATIONS D’ANTIBIOTIQUES
Les associations d’antibiotiques sont très largement utilisées en réanimation. Dans
deux travaux, l’un espagnol et l’autre français, des associations d’antibiotiques (ami-
noglycosides associés à d’autres molécules type uréidopénicilline ou céphalosporines
de deuxième ou troisième génération ou vancomycine) sont utilisées dans 75 % et 77 %
des traitements empiriques de pneumonies nosocomiales en réanimation [1, 2].
La sévérité des malades, mais aussi l’angoisse des médecins se conjuguent pour
expliquer cet état de fait. Dans le cadre d’une analyse critique des déterminants de la
prescription antibiotique, il est nécessaire de réaliser l’inventaire des éléments pouvant
rendre compte d’une certaine gravité, ou des difficultés thérapeutiques, et expliquer
(mais peut être pas justifier !), dans certains cas, le recours à des associations d’antibio-
tiques. Ces éléments sont : l’incertitude diagnostique, les caractéristiques du couple
bactérie-antibiotique et les gravités générales mais aussi locales.
1.1. INCERTITUDE DIAGNOSTIQUE
Elle ne justifie pas en elle-même le recours à des associations. Le traitement anti-
biotique doit couvrir les principales étiologies bactériennes envisageables. La nécessité
de prendre en compte des germes anaérobies, des staphylocoques résistants à la méti-
cilline, parfois des entérocoques, mais aussi des bactéries à Gram négatif souvent
multirésistantes peut conduire à une décision d’association d’antibiotiques pour élar-
gissement du spectre. L’incertitude sur le profil de sensibilité de certaines souches
hospitalières s’ajoute à l’incertitude sur le diagnostic microbiologique.

MAPAR 2000620
1.2. GRAVITE DE L’INFECTION
La gravité générale exprimée par des signes de choc ou de défaillance d’organe, ou
par l’évidente progression rapide du processus infectieux local constitue un détermi-
nant supplémentaire de la prescription d’antibiotique. Cependant, plus que les concepts
de monothérapie ou d’associations antibiotiques, les éléments de gravité doivent faire
discuter l’impact pronostique du caractère approprié ou non de l’antibiothérapie et
celui du délai de mise en route d’un traitement efficace.
Ainsi, dans une étude prospective «observationnelle» portant sur 2 184 malades
atteints de septicémie à bacilles à Gram négatif, la mortalité n’était pas influencée
par le caractère approprié de l’antibiothérapie probabiliste, sans différence entre
ß-lactamine seule ou en association avec un aminoglycoside. Les malades neutropéni-
ques constituaient dans cette étude le seul sous-groupe pour lequel un bénéfice de
l’association était clairement démontré (OR = 0,2 ; IC à 95 % = 0,05-0,7) [3]. De même,
les pneumonies nosocomiales représentent la première cause de décès lié à l’infection
nosocomiale avec des mortalités de l’ordre de 30 % à 50 %, pouvant même atteindre
70 % dans certaines populations de malades ou quand l’infection est liée à des germes
particulièrement difficile à traiter [4-7]. La survie des malades est liée à la précocité du
diagnostic et à l’adéquation initiale du traitement antibiotique [2, 8-10]. Et même si les
résultats de ces différents travaux peuvent être contestés, il est hautement probable
qu’un traitement antibiotique optimal mis en place dès les premiers signes de la mala-
die puisse améliorer le pronostic. Cependant des attitudes «antibiotiques» trop
délibérément probabilistes conduisent de manière excessive à recourir aux antibioti-
ques dont le spectre est le plus large et aux associations. C’est la raison pour laquelle il
est logique et raisonnable de recourir le plus possible aux investigations microbiologi-
ques préalables afin de réduire la part d’incertitude et de n’employer, dans la mesure du
possible, que des traitements parfaitement étayés.
1.3. PROBLEMES LOCAUX
D’autres éléments «locaux» peuvent aussi compromettre l’efficacité des antibioti-
ques, du fait de l’importance de l’inoculum bactérien, des difficultés de diffusion au
site de l’infection, des conditions physico-chimiques défavorables, de l’anoxie, de la
présence de pus ou de la présence d’un corps étranger. De l’innoculum bactérien dé-
pendent deux éléments pouvant contribuer à l’échec d’un traitement antibiotique :
1-la quantité d’enzymes produite, support de la résistance (telles des ß-lactamases), et
2-le nombre de mutants résistants au sein de la population bactérienne de départ,
susceptibles d’être sélectionnés par l’antibiotique en cours de traitement et de donner
naissance à une population bactérienne de remplacement responsable d’un échec se-
condaire [11]. Les conditions de l’activité des antibiotiques en pathologie sont bien
différentes de ce qui est obtenu en expérimentation standardisée. L’évolution clini-
que dépend de l’effet propre du traitement antibiotique mais aussi de la mise en jeu
des moyens de défense de l’organisme. C’est lorsque ces défenses sont moins opé-
rantes, comme dans l’endocardite ou chez le neutropénique, que les démonstrations
d’un bénéfice clinique et d’une synergie des associations sont obtenues [12].
2. «POUR» L’ASSOCIATION AVEC UN AMINOGLYCOSIDE
Les aminoglycosides constituent un élément important du traitement des infections
sévères notamment à bactéries à Gram négatif. Leur emploi en combinaison avec un
autre antibiotique, en général une bêta-lactamine, est justifié par les raisons suivantes :

INFECTIOLOGIE 621
2.1. ELARGISSEMENT DU SPECTRE ANTIBIOTIQUE
L’association avec un amynglycoside permet une activité microbiologique étendue
sur les bactéries à gram négatif (y compris P. aeruginosa ou Acinetobacter) fréquem-
ment responsables des infections nosocomiales. Cet élargissement du spectre limite
ainsi l’incertitude du prescripteur ou la probabilité qu’un traitement empirique soit inef-
ficace. Cependant, si l’aminoglycoside est le seul antibiotique efficace in vitro au sein
de l’association choisie, les chances de succès sont faibles sauf s’il s’agit d’un sepsis
d’origine urinaire [3].
2.2. BACTERICIDIE RAPIDE
D’une association de deux antibiotiques est attendue une synergie, c’est-à-dire une
efficacité supérieure à celle obtenue par chacun des produits de l’association adminis-
tré isolément, et surtout supérieure à celle de la simple addition des deux effets [12].
Cette efficacité devrait alors se mesurer en vitesse de bactéricidie, en rapidité d’éradi-
cation, et être transcrite cliniquement en guérison plus rapide ou en possibilité de
traitement plus court, ce qui est bien rarement le cas ! La synergie exercée par une
association d’antibiotiques sur une population bactérienne est en outre difficile à pré-
voir : éventuellement démontrée in vitro, elle peut ne pas s’exprimer in vivo, du fait des
conditions différentes d’activité des antibiotiques. Concernant les infections à bacté-
ries à Gram négatif, la synergie ß-lactamine-aminoside ne s’exprime que sur des bactéries
mal tuées par les ß-lactamines [12]. En pratique, l’association n’est habituellement
recommandée que pour le traitement des infections à P. aeruginosa ou à Acinetobac-
ter [3, 13]. Par extension, elle est souvent préconisée pour des infections à entérobactéries
peu sensibles aux ß-lactamines ou porteuses de mécanismes de résistance constitution-
nels (Enterobacter, Citrobacter, Serratia, ....). En dehors de la neutropénie, le bénéfice
clinique d’une synergie n’est pas clairement démontré, y compris au cours des septicé-
mies à P. aeruginosa [13] et n’est peut être apparent que chez les malades les plus
graves [14]. Il n’y a en général pas de synergie, mais indifférence ou addition, entre ß-
lactamines et fluoroquinolones ou entre fluoroquinolones et aminosides. Toutefois,
l’absence habituelle de synergie avec les fluoroquinolones peut être compensée par les
avantages qu’offrent ces molécules en terme de diffusion tissulaire.
2.3. DIMINUTION DE L’EMERGENCE DE RESISTANCE
Par analogie, les fréquences relativement élevées de mutations de S. aureus et P.
aeruginosa vis-à-vis des fluoroquinolones peuvent justifier cet objectif [12]. Cette atti-
tude peut aussi se justifier pour certaines souches au sein desquelles la proportion de
mutants résistants est élevée, telles P. aeruginosa, Acinetobacter baumannii ou les en-
térobactéries productrices de céphalosporinase chromosomique inductible [15]. En
pratique, la prévention de l’émergence de mutants résistants par le recours à une asso-
ciation n’est justifiée que pour ces espèces bactériennes, et particulièrement en début
de traitement ou l’inoculum bactérien est majeur [12].
Les résultats obtenus in vitro et dans des modèles animaux de pneumonie ou de
péritonite à bacilles à Gram négatif sont concordants et suggèrent un effet favorable
des associations en termes de réduction du risque de sélection de mutants résistants. Il
reste que ce bénéfice est difficile à démontrer en clinique. Dans une étude récente,
l’adjonction d’un aminoglycoside ne permettait pas de prévenir l’émergence de P. ae-
ruginosa résistants [16]. En raison d’un faible nombre d’infections à P. aeruginosa,
cette étude permet difficilement de conclure. Un essai randomisé comportant un nom-
bre suffisant de malades, avec une recherche systématique de mutants résistants,

MAPAR 2000622
responsables d’infection ou de colonisation serait nécessaire. Les infections concer-
nées devraient comporter un nombre important de bactéries «à risque» telles que P.
aeruginosa ou les entérobactéries productrices de céphalosporinases chromosomiques.
3. «CONTRE» L’ASSOCIATION AVEC UN AMINOGLYCOSIDE
3.1. NOUVEAUX ANTIBIOTIQUES
Avec l’apparition de nouveaux antibiotiques bactéricides à large spectre dans les
années 80, la nécessité des combinaisons avec des aminoglycosides est remise en ques-
tion. Avec la ceftazidime ou l’imipenem par exemple, deux molécules mises sur le
marché au milieu des années quatre-vingt, il n’est pas nécessaire d’ajouter un amino-
glycoside pour obtenir un élargissement du spectre sur les bactéries à Gram négatif y
compris sur P. aeruginosa. Les données cliniques sur l’intérêt des associations sont
rares. La justification de l’association ne devrait être alors que de courte durée, dans
l’attente des résultats microbiologiques. En outre, l’effet synergique d’une association
d’antibiotique est très variable d’une souche à l’autre. Enfin, il est impossible de
prédire l’existence d’une synergie sur la base uniquement de l’identification et de l’an-
tibiogramme [17]. Les arguments utilisés ainsi pour justifier des associations sont dans
la majorité des cas purement théoriques.
3.2. TOXICITE
La toxicité potentielle des aminoglycosides explique par ailleurs certainement les
réticences à leur administration. L’association d’un aminoglycoside à un traitement par
une ß-lactamine peut clairement augmenter la néphrotoxicité [18, 19]. L’incidence de
cette néphrotoxicité varie selon le type de patients étudiés. Les patients souffrant d’une
infection sévère présentent souvent des facteurs de risque associés (administration de
diurétiques de l’anse, âge avancé, hypovolémie, hypotension, néphropatie pré-
existante) susceptibles de potentialiser la néphrotoxicité des aminoglycosides. Néan-
moins, cette néphrotoxicité parait réversible [19]. A contrario, l’ototoxicité, souvent
méconnue, pose des problèmes sérieux puisqu’elle est en général irréversible. Elle est
cependant très mal étudiée. Quoiqu’il en soit, les modalités d’utilisation des aminogly-
cosides actuellement préconisées pour le traitement des infections sévères à bacilles à
Gram négatif, à savoir une administration en dose quotidienne unique et une durée de
traitement inférieure à 7 jours, réduisent significativement le risque de toxicité.
CONCLUSION
Il n’existe donc pas de consensus sur les indications respectives d’une association
au cours des infections sévères présumées ou documentées à bacilles à Gram négatif. Il
est cependant possible de faire les propositions suivantes :
1-Lors du traitement probabiliste
En cas d’infection extra-hospitalière, la monothérapie vis-à-vis des bacilles à Gram
négatif est parfaitement acceptable. L’utilisation d’un aminoglycoside pendant 48
heures, dans le but d’augmenter la vitesse de bactéricidie est également licite.
En cas d’infection nosocomiale, l’emploi d’une association ß-lactamine-
aminoglycoside ou ß-lactamine-fluoroquinolone au moins pour les premières 48 h,
c’est-à-dire en pratique jusqu’au résultat de l’antibiogramme, est recommandé.
L’association n’est poursuivie que si la ou les bactéries en cause sont «à risque»
(cf. plus haut).

INFECTIOLOGIE 623
2-Lors du traitement sur infection documentée
L’isolement ou non d’une bactérie «à risque» constitue le critère principal de choix
entre monothérapie et association.
REFERENCES BIBLIOGRAPHIQUES
[1] Fagon JY, Chastre J, Hance AJ, Domart Y, Trouillet JL, Gibert C. Evaluation of clinical judgement in
the identification and treatment of nosocomial pneumonia in ventilated patients. Chest 1993;103:543-553
[2] Alvarez-Lerma F. ICU-Acquired Pneumonia Study Group. Modification of empiric antibiotic treatment
in patients with pneumonia acquired in the intensive care unit. Intensive Care Med 1996;22:387-394.
[3] Leibovici L, Paul M, Poznanski O, Drucker M, Samra Z, Konigsberger H et al. Monotherapy versus
ß-lactam-aminoglycoside combination treatment for gram-negative bacteremia: a prospective, observational
study. Antimicrobial Agents Chemother 1997;41:1127-1133
[4] Chastre J, Fagon JY. Pneumonia in the ventilator-dependent patient. In: Tobin MJ, ed. Principles and
practice of mechanical ventilation. McGraw-Hill Inc; 1994;p.857-890
[5] Celis R, Torres A, Gatell JH, Almela M, Rodriguez-Roisin R, Augusti-Vidal A. Nosocomial pneumonia:
a multivariate analysis of risk and prognosis. Chest 1988;93:318-324
[6]
Craven DE, Driks MR. Nosocomial pneumonia in the intubated patient. Semin Respir Infect 1987;2:20-33
[7] Pennington JE. Nosocomial respiratory infection. In: Mandell GL, Douglas Jr RG, Bennett JE, eds.
Principles and practice of infectious diseases. 3rd ed. Churchill Livingstone; 1990; p.2199-2205
[8] Torres A, Aznar R, Gatell JM, Jimenez P, Gonzales J, Ferrer A, et al. Incidence, risk and prognosis
factors of nosocomial pneumonia in mechanically ventilated patients. Am Rev Respir Dis 1990;142:523-528
[9] Rello J, Gallego M, Mariscal D, Sonora R, Valles J. The value of routine microbial investigation in
ventilator-associated pneumonia. Am J Respir Crit Care Med 1997;156:196-200
[10] Kollef MH, Ward SM. The influence of mini-BAL cultures on patients outcomes: implications for the
antibiotic management of ventilator associated pneumonia. Chest 1998;113:412-420
[11] Thomas JK, Forrest A, Bhavnani SM, Hyatt JM, Cheng A, Ballow CH, et al. Pharmacodynamic
evaluation of factors associated with the development of bacterial resistance in acutely ill patients during
therapy. Antimicrob Agents Chemother 1998;42:521-527.
[12] Rybak MJ, Mc Grath BJ. Combination antimicrobial therapy for bacterial infections. Guidelines for
the clinician. Drugs 1996;52:390-405
[13] Hilf M, Yu VL, Sharp JA, Zuravleff JJ, Korvick JA, Muder RR. Antibiotic therapy for pseudomonas
aeruginosa bacteremia: outcome correlations in a prospective study of 200 patients. Am J Med 1989;87:540-545
[14] Korvick JA, Bryan CS, Farber B, Beam TRJr, Schenfeld L, Muder RR, et al. Prospective observational
study of Klebsiella bacteremia in 230 patients: outcome for antibiotic combinations versus monotherapy.
Antimicrob Agents Chemother 1992;36:2639-2644
[15] Sanders CC, Sanders WE. Emergence of resistance during therapy with the newer betalactam
antibiotics: role of inductible beta-lactamases and implications for the future. Rev Infect Dis 1983;5:639-648
[16] Cometta A, Baumgartner JD, Lew D, Zimmerli W, Pittet D et al. and the Swiss Antibiotic Study
Group. Prospective randomized comparison of imipenem monotherapy with imipenem plus netilmicin for
treatment of severe infections in non-neutropenic patients. Antimicrob Agents Chemother 1994;38:1309-1313
[17] Eliopoulos GM, Eliopoulos CT. Antibiotic combinations: should they be tested? Clin Microb Rev
1988;1:139-156
[18] Drusano GL, Warren JW, Saah AJ, Caplan ES, Tenney JH et al. A prospective, randomized, controlled
trial of cefoxitin versus clindamycin-aminoglycoside in mixed aerobic-anaerobic infections. Surg Gynecol
Obstet 1982;154:715-720.
[19] Solomkin JS, Fant WK, Rivera JO, Alexander JW. Randomized trial of imipenem/cilastin versus
gentamicin and clindamycin in mixed flora infections. Am J Med 1985;76 (Suppl. 6A):85-91
1
/
5
100%