Prise en charge du pied diabétique infecté M

La Lettre de l’Infectiologue - Tome XVII - n
o
8 - novembre-décembre 2002
265
MISE AU POINT
e risque d’amputation demeure un problème grave
du pied diabétique, et d’actualité, puisqu’on estime
que 5 à 10 % des diabétiques de type 2 seront un jour
amputés d’orteil, de pied ou de jambe (1). La neuropathie et
l'artérite sont les deux facteurs de risque essentiels d’infection
du pied diabétique. Une ulcération podologique survient sur
un pied neuropathique dans 50 % des cas, sur un pied neuro-
ischémique dans 30 % des cas et sur un pied vasculaire pur dans
20 % des cas. L’infection est une complication qui peut prendre
la forme d’une cellulite ou d’une ostéite.
PHYSIOPATHOLOGIE DES PLAIES DU PIED DIABÉTIQUE
Le terrain
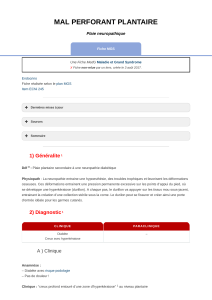
!Pied neuropathique : le mal perforant plantaire (photo 1).
Le mal perforant plantaire est une complication typique du pied
neuropathique Par définition, il est systématiquement infecté,
dans le sens où les résultats des prélèvements locaux sont tou-
jours positifs. Sa pathogénie repose surtout sur des mécanismes
biomécaniques : hyperpression plantaire au niveau des têtes
métatarsiennes, raideur articulaire avec déformations, troubles
trophiques responsables de sécheresse cutanée. Cependant,
c’est l’insensibilité à la douleur qui permet à ces différents fac-
teurs de construire, après des mois d’évolution, un mal perfo-
rant plantaire. Le patient appuie au niveau de zones privilégiées
d’hyperpression où se forme l’hyperkératose, qui se comporte
comme un corps étranger agressif. L’absence de douleur
entraîne la chronicisation avec apparition d’une poche de décol-
lement sous-cutanée sous tension, responsable d’une force de
cisaillement longitudinale. La corne se fendille, provoquant une
effraction cutanée qui favorise la surinfection. Le mal perfo-
rant se présente comme une ulcération au sein d’une plaque
d’hyperkératose. Il est parfois artificiellement fermé, recouvert
par cette plaque. Il sera alors révélé lors du soin de pédicurie
d’abrasion de cette plaque de corne.
*Service de diabétologie, hôpital Pitié-Salpêtrière, 75651 Paris Cedex 13.
Prise en charge du pied diabétique infecté
"
S. Jacqueminet*, G. Ha Van*, M. Lejeune*, A. Hartemann-Heurtier*
RÉSUMÉ.
Les prélèvements bactériologiques des plaies du pied diabétique sont dans la plupart des cas positifs, sans que, pour autant,
l’infection ait un rôle majeur dans la pathogénie. La gravité est liée au terrain ischémique artériel qui expose au risque de gangrène et
d’amputation. La chronicité est secondaire à la neuropathie, responsable d’une non-conscience de la gravité et d’une non-compliance
aux soins. L’antibiothérapie, nécessaire en cas de cellulite ou d’ostéite, n’est qu’une composante du traitement, qui repose en premier lieu sur
la mise en décharge complète de la plaie et la revascularisation artérielle si nécessaire.
Mots-clés :
Diabète - Neuropathie - Artérite - Ostéite.
L
Photo 1. Mal perforant plantaire.

Cette infection peut soit s’extérioriser à la peau, soit diffuser
en profondeur vers les gaines tendineuses ou l’os adjacent res-
ponsable d’ostéite. L’examen clinique du mal perforant
plantaire doit comporter impérativement la recherche de deux
complications qui changeront radicalement les modalités de la
prise en charge : il s’agit de l’ostéite et de l’artérite (voir plus loin).
L’absence de sensibilité à la douleur va non seulement retarder,
mais également rendre très difficile la prise en charge, dont la
composante principale est la mise en décharge totale de la plaie.
!Pied diabétique artéritique. L’athérosclérose chez les
patients diabétiques ne diffère pas de celle des non-diabétiques
sur le plan anatomopathologique. En revanche, elle est plus pré-
coce, plus sévère, et la répartition homme/femme est plus “éga-
litaire”. Elle touche beaucoup plus fréquemment les artères de
jambe, et sa fréquente association à la neuropathie explique
l’absence de douleur en cas d’ulcération et l’absence de clau-
dication intermittente. Dans l’étude d’Apelqvist (2), 50 % des
patients porteurs d’une gangrène n’avaient pas de douleur de
décubitus.
Le diagnostic clinique d’artérite repose sur la sémiologie clas-
sique, mais avec une prédominance des signes en distalité chez
le diabétique : diminution ou abolition d’un pouls, en particu-
lier tibial postérieur. L’examen de la peau, des phanères et de
la plaie peut apporter des arguments complémentaires en faveur
d’une artérite : peau fine, luisante, dépilée, plaie située sur des
zones de frottement (parties latérales et dorsale du pied), aspect
nécrotique.
L’INFECTION DU PIED DIABÉTIQUE
L’infection est une complication majeure des plaies chroniques
du pied diabétique. Elle est, dans la grande majorité des cas,
secondaire à une plaie, et non sa cause. Le facteur déclenchant
est d’abord une blessure mécanique donnant accès à l’infec-
tion, qui se propage ensuite aux tissus. Mais, parfois, une
mycose interdigitale ou unguéale peut se surinfecter et donner
naissance secondairement à une plaie.
Les causes de plaies sur un pied artéritique ou neuro-ischémique
sont souvent d’origine mécanique : frottement d’une chaussure,
blessure à partir d’un durillon ou d’un ongle incarné non soi-
gné, coupure avec des ciseaux, etc. La plaie passe inaperçue en
raison de la neuropathie associée, qui fait disparaître le signe
d’alerte qu’est la douleur. La plaie non soignée va rapidement
se surinfecter : infection des parties molles, puis, par contiguïté,
de l’os, touchant d’abord la corticale puis la médullaire.
Les signes locaux d’inflammation (rougeur, chaleur, œdème)
et leur localisation traduisent une infection des parties molles
et donnent une idée de son extension. Un écoulement, lorsqu’il
est purulent, affirme cliniquement cette infection, mais celle-
ci peut diffuser à distance et réaliser un abcès, voire un phleg-
mon des gaines tendineuses, sans s’extérioriser. Sur un pied
artéritique, ces lésions prendront rapidement un aspect nécro-
tique (cellulite nécrosante). La nécrose peut entretenir l’infec-
tion qui, en se propageant, étend la zone ischémique. Cette plage
nécrotique entourée d’un halo inflammatoire, voire purulent,
est appelée “gangrène humide”. Le risque est l’extension par
contiguïté aux zones saines. Si la plaie ne s’est pas surinfectée,
mais a favorisé une ischémie locale, l’aspect peut être celui
d’une gangrène sèche, limitée, de meilleur pronostic.
La fièvre est un signe de gravité, mais la plupart des infections
graves (cellulite, ostéite) du pied diabétique surviennent sans
décalage thermique. Dans une série publiée par Armstrong (3),
87 % des patients admis avec une ostéite étaient apyrétiques.
PRISE EN CHARGE D’UNE ULCÉRATION PODOLOGIQUE
Bilan
!Prélèvements bactériologiques. Le diagnostic des germes
incriminés dans l’infection est difficile, car l’écologie bactérienne
des ulcérations du pied est polymicrobienne, et il n’existe tou-
jours pas de consensus sur l’antibiothérapie de première inten-
tion à commencer avant les résultats bactériologiques. Les pré-
lèvements superficiels sont souvent contaminés par les germes
commensaux du pourtour de l’ulcère. Les prélèvements profonds
par aspiration/lavage au cathlon semblent plus fiables, mais ont
l’inconvénient de diluer le prélèvement, rendant l’examen direct
incapable de repérer le germe prédominant. Le prélèvement de
pus par drainage d’un abcès ou une biopsie chirurgicale est plus
fiable, mais pas toujours réalisable. L’étude de Wheat comparant
les différents types de prélèvements (4) montre que l’antibio-
thérapie instituée devant un prélèvement dit “non fiable” permet
dans 92 % des cas de traiter le germe profond, mais avec un
spectre trop large dans 31 % des cas. Un prélèvement à l’écou-
villon dans le fond de l’ulcération après en avoir désinfecté la
surface retrouve les germes responsables, mais aussi des com-
mensaux dont il faut savoir ne pas tenir compte.
En moyenne trois à cinq micro-organismes sont isolés par pré-
lèvement, d’autant plus nombreux que la plaie est profonde et
ischémique (5). Les germes les plus fréquemment retrouvés
sont les cocci à Gram positif, incluant Staphylococcus aureus,
staphylocoque à coagulase négative et streptocoque du
groupe B. Les entérocoques, les bacilles à Gram négatif (Pro-
teus spp, Escherichia coli, Klebsiella, Enterobacter) viennent
ensuite. Le Pseudomonas aeruginosa est fréquemment
retrouvé, mais doit être considéré la plupart du temps comme
non pathogène. Il en est de même pour Corynebacterium spp,
qu’on retrouve dans 20 % des cultures. Les germes anaérobies,
exceptionnellement trouvés seuls, sont présents dans 80 % des
cultures. Les anaérobies cocci à Gram positif doivent être consi-
dérés comme des contaminants, et sont présents dans les plaies
peu graves, alors que Bacteroides spp est retrouvé dans les
infections nécrosantes et doit être traité. L’incrimination du sta-
phylocoque à coagulase négatif, fréquemment retrouvé dans
les plaies banales, est s’il n’est pas seul isolé, discutable. On
peut ne pas en tenir compte dans la couverture antibiotique ini-
tiale, suivre l’évolution clinique en traitant les germes pyogènes
classiques, et ne le prendre en compte qu’en cas d’aggravation.
266
La Lettre de l’Infectiologue - Tome XVII - n
o
8 - novembre-décembre 2002
MISE AU POINT

!La recherche d’une ostéite. Le diagnostic d’ostéite peut
être affirmé dès l’examen clinique : la présence d’un contact
osseux lors de l’exploration de la plaie avec un stylet stérile
mousse affirme une ostéite avec une valeur prédictive de 85 %
(6) (photo 2). La mobilité complète d’une articulation (inter-
phalangienne ou métatarso-phalangienne) signe la dislocation
articulaire, dont l’origine dans ce contexte ne peut être que sep-
tique (ostéoarthrite). Des radiographies standard centrées sur
la lésion doivent être systématiquement prescrites et renouve-
lées tous les 15 jours en cas d’évolution non favorable. Elles
montrent des signes typiques, comme l’érosion corticale ou le
décollement périosté en regard de la plaie. Dans le cas d’une
plaie chronique, ne cicatrisant pas malgré la mise en décharge,
en l’absence de contact osseux et en présence de radiographies
d’interprétation difficile, on peut, en dernier recours, faire appel
à l’association d’une scintigraphie osseuse au 99Tc-MDP avec
la scintigraphie aux polynucléaires marqués au 99Tc-HMPAO.
Dans les cas douteux, cette association d’examens aurait une
sensibilité proche de 100 % et une spécificité de 95 % pour le
diagnostic d’ostéite (7).
!Bilan vasculaire (figure 1). Il est indispensable aux déci-
sions thérapeutiques. Toute chirurgie orthopédique doit être
précédée d’un bilan artériel minimal.
"Mesure de la pression transcutanée d’oxygène (TcPO2). Pos-
sible au lit du patient, elle évalue la qualité de la circulation cuta-
née, et sa baisse est corrélée à l’existence d’une ischémie cutanée.
La Lettre de l’Infectiologue - Tome XVII - n
o
8 - novembre-décembre 2002
267
MISE AU POINT
Photo 2. Recherche de contact
osseux à l’aide d’une pointe mousse
stérile.
Figure 1. Arbre décisionnel chirur-
gical devant une ulcération artéri-
tique ou neuro-ischémique.
Bilan vasculaire
#clinique
#TcPO2
#Doppler artériel jambe et pied
Douleur décubitus
et/ou nécrose
et/ou claudication serrée
Artériopathie
avec clichés tardifs
Pontage
et angioplastie
impossibles
Pontage distal
±angioplastie
+ poursuite
du traitement
médical
Assèchement
des lésions Assèchement
des lésions
Amputation limitée aux zones nécrotiques
ou “autoamputation”
Pas de nécrose
Pas de douleur
TcPO2*30mmHg et/ou doppler
artériel distal de mauvais pronostic
Pas de nécrose
Pas de douleur
TcPO2*30mmHg 1 axe
de jambe au doppler artériel
Traitement médical
Éviter le geste orthopédique Traitement médical
Si ostéite : chirurgie
conservatrice possible
Traitement médical
Si ostéite : chirurgie
conservatrice possible

268
La Lettre de l’Infectiologue - Tome XVII - n
o
8 - novembre-décembre 2002
MISE AU POINT
"Écho-doppler artériel. Il n’est pas indispensable au
diagnostic positif d’artérite, qui est le plus souvent clinique,
mais il est nécessaire en cas de doute, ou pour apprécier l’éten-
due et la sévérité des lésions
"Artériographie. Ce n’est pas un examen diagnostique ni
de suivi. Il doit être réservé aux patients chez lesquels l’in-
dication d’un geste de revascularisation a été posée. Les
lésions étant multifocales, avec une nette prédominance des
lésions fémoro-poplitées et jambières, l’exploration distale
est indispensable. Elle nécessite la réalisation de grands
clichés traditionnels tardifs. La totalité du pied doit être
visualisée, afin de pouvoir définir le site d’implantation d’un
pontage distal.
Tr aitement
!Hospitalisation. Elle est indispensable en cas :
– de plaie chez un artéritique, pour réaliser un bilan artériel et
contrôler la décharge ;
– de la présence de signes généraux ou locaux extensifs ;
– de la présence d’une ostéite ;
– de non-compliance à la décharge.
!Mise en décharge de la plaie. La mise en décharge est une
condition essentielle de cicatrisation. Elle doit supprimer ou
diminuer l’hyperpression ou le frottement sur la plaie. Certains
auteurs n’hésitent pas à dire qu’une plaie non correctement mise
en décharge est une plaie non traitée ! Différents moyens peu-
vent être mis en œuvre pour la décharge de la plaie en fonction
de sa localisation (8).
"Pour les plaies de l’avant-pied et des orteils. La solution
la plus adaptée et la plus simple est le port d’une chaussure
de décharge totale de l’avant-pied (type Barouk Mayzaud ou
Barouk). Ces chaussures permettent la cicatrisation du mal
perforant plantaire si elles sont portées à chaque fois que le
patient pose le pied à terre, et s’il n’existe pas d’artériopa-
thie sévère associée ou d’ostéite sous-jacente à traiter (voir
plus loin). Le plâtre de décharge permet une décharge totale
chez les patients ayant une mauvaise compliance pour la
décharge classique, et lorsque la chronicité de la plaie
entraîne un risque d’amputation. Cependant, il n’est pas ano-
din de mettre une botte plâtrée à des patients ayant une neu-
ropathie. La technique de pose doit être rigoureuse. Le béné-
fice de cette technique doit être pondéré par la nécessité d’une
parfaite maîtrise technique et d’une surveillance étroite avec
possibilité de revoir le patient régulièrement, et si besoin
en urgence. Elle ne doit donc pas être utilisée en première
intention. Elle est contre-indiquée chez les patients ayant une
artérite sévère ou des œdèmes des membres inférieurs non
stabilisés.
Les autres moyens de décharge de l’avant-pied peuvent être
l’alitement, le fauteuil roulant ou les cannes béquilles.
Remarque. Les semelles orthopédiques ou orthèses plantaires
sont habituellement inefficaces pour guérir totalement un mal
perforant plantaire.
"Pour les plaies dorsales des orteils ou des bords latéraux du
pied.Un mal perforant ou une ulcération artérielle peuvent par-
fois survenir sur une zone de frottement. Dans ce cas, il est
nécessaire de mettre en décharge la face dorsale de l’orteil, ou
la face latérale du pied. Le moyen le plus simple est d’inciser
en croix la chaussure habituelle en regard de la plaie. On peut
aussi avoir recours à une chaussure de décharge type Orthop
USA. Celle-ci, ouverte à l’avant, permet de loger un pansement
en évitant le frottement sur la face dorsale des orteils.
!Équilibration du diabète. L’équilibration du diabète doit
être optimale et rapide, comme dans toute infection bactérienne
chez le diabétique. L’arrêt des biguanides s’impose et le recours
à l’insuline est presque toujours nécessaire.
!Les soins locaux. Dans le cas d’un mal perforant, un débri-
dement large retirant toute l’hyperkératose qui entoure la lésion
doit être effectué de manière mécanique, à l’aide d’une pince
convexe, ou pince-gouge. La plaie sera nettoyée au sérum phy-
siologique. L’utilisation d’un antiseptique n’est pas recom-
mandée. On appliquera ensuite localement un pansement peu
gras du type Adaptic®. Une plaie nécrotique ne sera pas débri-
dée avant d’être revascularisée (risque d’aggraver la nécrose),
mais asséchée (fluorescéine aqueuse à 1 ‰). On doit néanmoins
“mettre à plat” et exciser les collections purulentes sous ten-
sion. Une mycose interdigitale doit être traitée.
!L’antibiothérapie (9). L’indication de l’antibiothérapie doit
être discutée. On distingue quatre éventualités :
– Si la plaie ne présente pas d’aspect inflammatoire (rougeur, cha-
leur, œdème), s’il n’y a ni signe septique (écoulement séropuru-
lent), ni aspect évocateur d’ostéite sous-jacente (voir plus loin),
elle ne nécessite ni prélèvement bactériologique, ni antibiothéra-
pie. La décharge, les soins locaux et l’équilibration du diabète, en
l’absence d’ostéite et d’artérite, doivent permettre la cicatrisation.
– Si la plaie présente des signes inflammatoires modérés (rou-
geur et chaleur localisées au pourtour de la plaie) et en l’ab-
sence de signes généraux (fièvre, frissons), il est préférable d’at-
tendre les résultats du prélèvement bactériologique et de suivre
l’évolution clinique, afin d’instaurer, uniquement si celle-ci
n’est pas rapidement favorable, une antibiothérapie adaptée.
Dans l’étude prospective randomisée de Chantelau sur des
plaies neuropathiques peu sévères et sans ostéite (10), l’effica-
cité du placebo est comparable à celle de l’amoxicilline plus
acide clavulanique (Augmentin®) en taux et durée de cicatrisa-
tion. Cette notion est renforcée par la constatation faite dans
différentes études d’une amélioration clinique des plaies
possible, alors même que l’antibiothérapie ne stérilise pas les
prélèvements (11, 12). On vérifiera l’absence d’ostéite. En
présence d’une artérite clinique, le patient sera hospitalisé pour
un bilan vasculaire et une surveillance quotidienne (13).
– Si la plaie présente des signes septiques évidents (écoulement
purulent), ou inflammatoires extensifs (cellulite extensive), ou
est associée à des signes ischémiques (nécrose pouvant traduire
la présence d’une artérite, ou fasciite nécrosante), ou des signes
généraux, il faut effectuer un prélèvement bactériologique,
mettre la plaie en décharge et débuter une antibiothérapie
probabiliste en attendant les résultats.

– Si la plaie s’accompagne de signes cliniques d’ostéite, l’ur-
gence de l’antibiothérapie dépend de la présence ou non des
signes de gravité décrits ci-dessus et de l’histoire de la plaie.
La 3eConférence de consensus de pathologie infectieuse a
conclu à l’absence d’urgence devant les formes chroniques d’in-
fections ostéo-articulaires (14). Il est donc justifié, devant une
plaie chronique sans signes de gravité, même en présence d’une
ostéite, d’attendre le résultat du prélèvement bactériologique
pour mettre en route l’antibiothérapie, étant entendu que
l’appui sur l’articulation doit être immédiatement et totalement
supprimé.
"L’antibiothérapie initiale. Il n’y a pas de consensus sur la
nature de l’antibiothérapie initiale à instituer, mais plusieurs para-
mètres sont à prendre en compte (15) :l’activité contre les micro-
organismes les plus fréquemment en cause ; les concentrations
à obtenir au site de l’infection (os et parties molles) compte tenu
de l’artérite ; la toxicité, en particulier rénale, chez des patients
diabétiques multicompliqués avec possible néphropathie.
"L’activité sur les germes pathogènes les plus fréquemment
en cause. Le seul antibiotique recueillant un certain consensus
dans le traitement initial est l’amoxicilline plus acide clavula-
nique. Il est actif sur les staphylocoques méticilline-sensibles,
les streptocoques, les entérocoques, les anaérobies et la plupart
des entérobactéries. En l’absence de signes de gravité (fièvre
ou signes locaux extensifs), on peut donc commencer un trai-
tement par l’amoxicilline plus acide clavulanique seul, en atten-
dant le résultat des prélèvements. En présence de signes de gra-
vité, il est licite d’associer un aminoside. Il est actuellement
conseillé d’administrer celui-ci en une seule injection par
24 heures.
La situation est différente chez un patient multihospitalisé pré-
sentant une plaie. C’est souvent le cas des patients diabétiques
ayant une ulcération du pied, qui sont les plus à risque de
“récidiver”. Si le patient a été hospitalisé dans l’année ou bien
fréquente une consultation hospitalière de podologie, il est à
haut risque d’être porteur d’une bactérie multirésistante (BMR)
(S. aureus méticilline-résistant ou P. aeruginosamultirésistant).
Chez ces patients, il pourrait être justifié, en présence de signes
généraux (fièvre, frissons), de commencer un triple traitement
couvrant les germes hospitaliers avant de pouvoir les adapter
aux prélèvements : association d’une bêtalactamine type pipé-
racilline plus tazobactam (Tazocilline®) ou imipénème plus
cilastatine (Tienam®), avec un aminoside et un glycopeptide
(Vancomycine®,Targocid®). Il est également licite, en dehors
de signes infectieux graves, de ne pas couvrir les BMR et de
traiter par amoxicilline-acide clavulanique, sachant que les
BMR sont retrouvées dans moins de 50 % de ces plaies.
"Les concentrations à obtenir au site de l’infection doivent
être bactéricides, ce qui est difficile, compte tenu de la présence
d’une artérite, limitant la diffusion des antibiotiques. Les poso-
logies maximales de l’AMM doivent être prescrites, et l’admi-
nistration doit se faire par voie parentérale. La toxicité rénale
doit être prise en compte : les aminosides ne seront pas admi-
nistrés plus de 5 jours, les posologies d’aminosides et de gly-
copeptides doivent être adaptées à la clairance de la créatinine,
et des dosages résiduels doivent être demandés à 24 heures.
"À la réception des résultats bactériologiques, le traitement
doit être poursuivi en tenant compte des mêmes règles (poso-
logie maximale de l’AMM, voie veineuse si possible) et des
paramètres suivants : ne pas traiter d’emblée les germes com-
mensaux, instituer un traitement avec le spectre le plus étroit
possible, et, en cas d’ostéite (16), associer deux antibiotiques
à bonne diffusion osseuse : pristinamycine, rifampicine, fosfo-
mycine, acide fusidique, fluoroquinolones. Dans bien des
cas, l’aide des bactériologistes est souhaitable, car une erreur
de prescription peut favoriser l’émergence de bactéries multi-
résistantes.
"La durée de l’antibiothérapie n’est pas définie. Elle doit
prendre en compte l’évolution clinique. La disparition des
signes locaux inflammatoires et la stérilisation des prélève-
ments devraient conduire à son arrêt. Certaines équipes la pour-
suivent pourtant jusqu’à cicatrisation. En cas d’ostéomyélite,
la durée totale de traitement recommandée serait de 10 à
12 semaines (17). Elle pourrait être plus courte en cas de résec-
tion chirurgicale du foyer ostéitique.
!Chirurgie orthopédique. En présence d’une ostéite, le délai
de cicatrisation peut être nettement raccourci par l’association
au traitement médical d’une chirurgie dite conservatrice (18).
Après quelques jours de traitement médical visant à “refroidir”
la plaie, on peut proposer un geste chirurgical, le plus limité
possible, sur la partie osseuse infectée. Ce geste concernera
donc une phalange ou une tête métatarsienne sans élargisse-
ment aux parties saines. Cette chirurgie limitée permet non seu-
lement de raccourcir la durée de la plaie, mais aussi de conser-
ver le maximum de points d’appui et l’aspect extérieur du pied.
L’objectif est surtout de limiter le risque de récidive, mais aussi
d’offrir une bonne acceptation psychologique. À l’occasion du
geste chirurgical, l’ulcération sera mise à plat et la plaie refer-
mée à l’aide de points de suture lâches. La mise en décharge
postopératoire doit être totale jusqu’à cicatrisation. Cette
chirurgie est réservée aux pieds neuropathiques, en l’absence
d’artérite sévère.
!Chirurgie vasculaire. Devant un pied artéritique ou neuro-
ischémique, tout geste de débridement agressif ou toute chi-
rurgie orthopédique doivent être précédés d’un geste de revas-
cularisation.
Le cas le plus fréquent chez les patients diabétiques présentant
une plaie ischémique du pied reste celui des lésions infra-ingui-
nales isolées (fémoro-poplité) avec, fréquemment, une des-
truction quasi complète du réseau jambier. Heureusement, dans
la majorité des cas, les clichés tardifs de l’artériographie révè-
lent la présence d’un axe artériel distal en bas débit, mais dont
la revascularisation peut permettre le sauvetage du membre et
la cicatrisation. Ainsi, on réalise des pontages artériels distaux.
En raison de sa longueur, la technique de référence est le pon-
tage par veine saphène inversée in situ. Le risque périopéra-
toire de cette chirurgie est aussi variable selon les études de
La Lettre de l’Infectiologue - Tome XVII - n
o
8 - novembre-décembre 2002
269
MISE AU POINT
 6
6
1
/
6
100%