Mélanges thermoplastique/thermodurcissable à base d`époxy

Etude Bibliographique
7
CHAPITRE I :
Etude Bibliographique

Etude Bibliographique
8

Etude Bibliographique
9
I-1] Les réseaux époxydes
Les réseaux époxydes sont utilisés dans de nombreuses applications industrielles. Ils
sont en général formés par polyaddition d’un mélange monomère époxyde et durcisseur dans
lequel un au moins des composants a une fonctionnalité supérieure à 2 afin d’obtenir un
réseau après réaction [PAS02]. De nombreux systèmes réticulants peuvent être utilisés. Ce
sont par exemple des molécules nucléophiles telles que les anhydrides d’acide, les poly-
amines aromatiques ou aliphatiques, les alcools et éventuellement des amorceurs
(imidazole…) qui augmentent la vitesse de polymérisation… Parmi tous ces durcisseurs, les
plus utilisés sont de type amine.
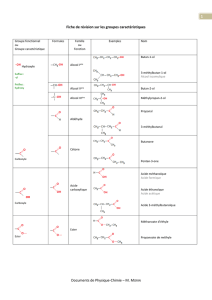
La réaction entre époxyde et diamine est celle que nous avons utilisée. Elle peut être
décrite en 3 réactions principales comme schématisées ci-dessous :
Equation 1
Equation 2
Equation 3
L’Equation 1 traduit la réaction d’addition d’un groupement époxyde avec
l’hydrogène d’une amine primaire. L’amine secondaire formée de la première réaction réagit
avec un autre groupement époxyde pour donner une amine tertiaire (Equation 2). Ces
réactions époxyde/amine sont connues pour être auto-catalysées par les groupements
hydroxyle présents initialement dans le milieu et créés au cours des 2 réactions. C’est
pourquoi, k
1
et k
2
correspondent aux constantes cinétiques du mécanisme catalysé et k
1
’ et k
2
’
à celles du mécanisme non catalysé. Nous pouvons définir le rapport des constantes de
réactivité de l’amine secondaire sur l’amine primaire, noté r = k
2
/k
1
qui permet la
comparaison de réactivité des différentes amines. Ce rapport est égal à 0,65 dans le cas de
mélange DGEBA (diglycidyle éther de Bisphénol A) et diamine MCDEA (4,4’-méthylènebis
[3-chloro 2,6-diéthylaniline]) [GIR95].
L’Equation 3 correspond à la réaction d’éthérification qui a lieu entre groupements époxyde
et hydroxyle. La plupart du temps, cette réaction est négligée. Elle intervient essentiellement
pour des fortes températures de polymérisation et lorsque la concentration en amine est faible,
donc en fin de réaction. Cependant Girard-Reydet [GIR95], a également montré grâce à des
analyses infrarouges, que la réaction 3 se produisait dans le cas de la MCDEA et devait être
prise en compte pour une bonne description du modèle cinétique. Il a également montré qu’il
n’en était rien avec deux autres diamines : la 4,4’-diaminophényl sulfone, DDS et la 4,4’-
méthylènebis dianiline, MDA.

Etude Bibliographique
10
La réaction d’un thermodurcissable fait intervenir deux transformations structurales
majeures : la gélification et la vitrification. Le terme de gélification marque le passage de
l’état initial liquide ou visqueux selon les formulations, à l’état caoutchoutique. Ce
phénomène est lié à la brutale augmentation des masses molaires moyennes du réseau en
formation. A ce moment, tout le volume réactionnel est occupé par une molécule
tridimensionnelle.
La vitrification traduit le passage de l’état liquide ou caoutchoutique à un état vitreux du fait
de l’augmentation de la densité de réticulation. C’est le moment où la température de
transition vitreuse du système est du même ordre de grandeur que la température de réaction
et donc la réaction est contrôlée par la diffusion. Cette transformation peut intervenir avant la
gélification suivant la température de réaction.
Gillham [ENN83] résume l’ensemble de ces phénomènes sur un diagramme appelé
TTT, Temps-Température-Transformation présenté ci-dessous :
Figure I1 : Diagramme T-T-T de Gillham pour un système réactif [ENN83].
Cette représentation permet d’estimer le temps de réaction nécessaire à l’obtention de
la gélification et de la vitrification pour une température de réaction choisie.
I-2] Modélisation des cinétiques des réactions époxyde/amine
Deux sortes de modèles peuvent rendre compte des cinétiques de réaction entre amine
et époxyde. L’approche mécanistique s’appuie sur les mécanismes de réaction alors que le
modèle phénoménologique est l’application d’un modèle mathématique pour correspondre au
mieux aux points expérimentaux.
I-2-a) Approche mécanistique
Elle se base sur les trois réactions principales époxy/amine décrites par les Equations
1, 2 et 3. En s’appuyant sur les dites réactions, il est possible d’obtenir le jeu d’équations
suivantes (Equations 4) où tous les paramètres ont un sens physique [GIR96] :

Etude Bibliographique
11
()
[
]
()
[
]
()
[
]
()
{
}
OHOHkkaOHkkaOHkk e
dt
de
3
'
322
'
211
'
1
⋅++⋅++⋅+=−
()
[]
OHkka2e
dt
da
1
'
11
1
+⋅⋅=−
Equations 4
()
[
]
()
[
]
{
}
22
'
211
'
1
2
aOHkkaOHkk e
dt
da ⋅++⋅+=
() ()
[]
()
[
]
{}
22
'
211
'
1
aOHkkaOHkk e
dt
OHd ⋅++⋅+=
avec e : concentration en groupement époxyde
a
1
, a
2
: concentration en groupement amine primaire et secondaire
(OH) : concentration en groupement hydroxyle
k
1
, k
2
: constantes de vitesse des réactions autocatalysées
k’
1
, k’
2
: constantes de vitesse des réactions non catalysées
k
3
, k’
3
: constantes de vitesse de réaction d’éthérification
De ce jeu d’équations, découle le modèle de Horie qui prend en compte le caractère
autocatlytique des réactions époxyde/amine (Equation 5). Il fait intervenir la concentration en
hydroxyle au cours de la réaction comme suit. Riccardi et al [RIC84] ou Horie et al [HOR70]
l’ont utilisé pour étudier les réactions DGEBA/diamines aliphatiques.
()
{}
()
²x1xekOHkke
dt
de
01
0
1
'
1 0
−++=−
qui équivaut à
{
}( )
²x1xKK
dt
dx 10 −+=
Equation 5
en posant (OH)=(OH)
0
+e
0
-e et x.e
0
= e
0
-e
avec e
0
: concentration initiale en groupement époxyde
x : conversion en groupement époxyde
(OH)
0
: concentration initiale en groupement hydroxyle
K
0
=e
0
.{k
1
’+k
1
(OH)
0
}
: constante de vitesse à l’instant initial
K
1
= k
1
e
0
² : constante de vitesse du processus autocatalysé
K
0
et K
1
suivent la loi d’Arrhénius.
Ce modèle peut être précisé en tenant compte des réactions d’éthérification [COL91]
et de l’effet de substitution des amines (Equations 6). Il a été utilisé par Riccardi et al
[RIC86] et Girard-Reydet et al [GIR95] [GIR96] pour modéliser des réactions
DGEBA/amines. Les équations sont les suivantes :
() ()
[]
() ()()()
r2LαFr2rααr12αFKKx1
dt
dx
2
r
1
'
1
−⋅
⎥
⎦
⎤
⎢
⎣
⎡−++−⋅+⋅−=
()
(
)
[]
αFKKx12α
dt
dα
1
'
1
+⋅−⋅=−
Equations 6
avec
() ()()
()
r2
ααr1
e
OH
1αF
2
r
0
0
−
⎥
⎦
⎤
⎢
⎣
⎡+−
−+=
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%