Lire l'article complet

Act. Méd. Int. - Métabolismes - Hormones - Nutrition, Volume V, n° 6, novembre-décembre 2002
240
étude des fonctions biologiques a com-
mencé avec la description des organes,
de leur rôle, de leurs sécrétions, etc. Ces
approches étaient essentiellement physiolo-
giques. Au fur et à mesure que cela a été pos-
sible, l’analyse des mécanismes qui contrô-
lent les fonctions biologiques a été faite au
niveau moléculaire.
Les techniques du génie génétique apparues
dans les laboratoires il y a bientôt vingt ans
ont commencé à modifier la manière dont les
biologistes ont abordé l’étude des mécanismes
de régulation des fonctions. Il est en effet
devenu alors possible d’isoler quelques
gènes, ceux qui étaient les plus abondamment
exprimés ou dont on connaissait les protéines
pour lesquelles ils codaient. La simple des-
cription de la structure des gènes permet
d’établir des corrélations entre la structure
primaire de l’ADN et ainsi des protéines cor-
respondantes et parfois avec l’activité bio-
logique de ces dernières. D’autres techniques,
permettant de procéder in vitro à des muta-
tions de gène puis à réintroduire des mutants
dans des cellules, ont fait franchir un fossé
considérable entre la chimie des molécules
du vivant et leurs activités dans une cellule ou
un organisme entier.
Dans ce concert, le transfert de gène à un
organisme entier devait très logiquement
prendre une place essentielle. La transgenèse,
réussie pour la première fois chez les ani-
maux en 1980, offre en effet la possibilité de
modifier précisément le patrimoine génétique
d’un organisme entier. Un pas supplémen-
taire a été franchi lorsqu’il est devenu pos-
sible non seulement d’ajouter une informa-
tion génétique à un génome, mais aussi de
remplacer très précisément un de ses gènes
par un autre, qui peut être un mutant actif ou
inactif mais aussi bien un tout autre gène.
Cette opération a été réussie pour la première
fois en 1989.
Ces expériences pionnières ont indiqué sans
ambiguïté que les biologistes étaient sortis de
l’obligation de devoir attendre des mutations
spontanées pour pouvoir les étudier. Cette
approche a été et reste très fructueuse chez
les micro-organismes, les végétaux et cer-
tains animaux comme la drosophile dont la
reproduction est rapide et bien contrôlée. La
mutagenèse induite par des agents chimiques
est également très pratiquée chez ces espèces.
Elle augmente la fréquence des mutations et
offre donc un plus grand choix au biologiste
bien que celles-ci restent tout aussi aléatoires.
La mutagenèse induite par des agents chi-
miques a commencé à être appliquée à grande
échelle chez la souris. Cela n’a de sens que
parce que les moyens ont progressé. Les
chercheurs disposent d’animaleries très per-
formantes qui permettent d’élever de très
nombreuses souris. Des méthodes d’investi-
gation faisant appel, en particulier, à l’ima-
gerie in vivo, permettent de faire un examen
systématique des mutants et d’orienter des
recherches approfondies par des laboratoires
spécialisés dans l’étude des fonctions ainsi
modifiées par la mutation. Une troisième
condition, tout aussi essentielle, est également
Dossier : Génomique, recherche et thérapie en endocrinologie
* Unité de biologie du développement et
biotechnologies, Institut national de la
recherche agronomique, Jouy-en-Josas.
✎Le séquençage complet des génomes
humains et murins offre des possibilités
sans précédent pour étudier le rôle des
gènes in vivo via la transgénèse.
✎Les éléments qu’il faut ajouter dans
une construction pour obtenir une expres-
sion fiable du transgène sont de mieux
en mieux connus (introns, isolateurs, ampli-
ficateurs, stabilisateurs d’ARNm, etc.).
✎Il est de plus en plus possible de cibler
l’intégration d’un gène et d’obtenir une
expression conditionnelle du transgène
contrôlé par des agents inducteurs
n’agissant pas sur les gènes de l’animal.
✎L’interférence de l’ARN est utilisée
chez la drosophile et Caenorhabditis
elegans à la place de l’inactivation des
gènes par recombinaison homologue.
Ce protocole est actuellement étendu à
la souris et à d’autres vertébrés.
✎L’inactivation systématique de tous les
gènes de la souris a été entreprise.
✎La technique de clonage des embryons
par transfert de noyau a permis d’inac-
tiver des gènes par recombinaison
homologue chez le mouton, la souris et
le porc. Cela devrait devenir possible
chez le lapin, le rat et quelques autres
espèces chez lesquelles le clonage sera
maîtrisé.
✎Il existe des structures qui permettent
un examen systématique des souris,
notamment en utilisant les techniques
d’imagerie in vivo.
✎La transgenèse permet d’utiliser le lait
comme source abondante de protéines
recombinantes pour en étudier les pro-
priétés ou les utiliser à des fins théra-
peutiques.
L’
Les apports de la transgenèse
dans la recherche biomédicale
L.M. Houdebine*

Act. Méd. Int. - Métabolismes - Hormones - Nutrition, Volume V, n° 6, novembre-décembre 2002
241
satisfaite. La cartographie puis la séquence
du génome de souris ont été établies. Ces
données permettent au biologiste, dans le
meilleur des cas, d’établir une corrélation
entre l’effet phénotypique d’une mutation et
la structure mutée d’un gène. Ainsi peuvent
être identifiés des gènes impliqués dans le
déclenchement de maladies retrouvées chez
l’homme.
La transgenèse suit dans une certaine mesure
un parcours un peu semblable. Les souris
transgéniques sont de plus en plus soumises
à de multiples examens destinés à déterminer
les effets physiologiques des mutations appor-
tées par le transfert de gène. Des projets en
cours visent à inactiver un maximum de
gènes de souris (et d’autres animaux expéri-
mentaux comme la drosophile et un ver, le
Caenorhabditis elegans) pour dresser un
inventaire le plus complet possible du rôle
des gènes. Ces approches sont bien évidem-
ment guidées par l’espoir de définir de nou-
velles substances d’intérêt thérapeutique.
Les biologistes sont donc en train de vivre
une nouvelle révolution, après celle qu’a
constituée l’utilisation artisanale du génie
génétique dans les laboratoires. Cette révo-
lution a pour fondement la rencontre de la
cartographie et du séquençage des génomes
d’une part; la détermination du patron d’ex-
pression des gènes grâce à l’utilisation des
puces à ADN d’autre part et, enfin, l’obten-
tion de mutants par action d’agents chimiques,
par introduction aléatoire de séquences étran-
gères (transposons, rétrovirus), par piégeage
de gène et par transgénèse.
C’est le caractère systématique et coordonné
de ces approches qui constitue la révolution
en question. Le biologiste se voit désormais
offrir une possibilité sans précédent d’étudier
au niveau moléculaire un maximum de méca-
nismes qui contrôlent les fonctions biolo-
giques. L’étude des génomes au sens large
constitue donc, non pas le triomphe du réduc-
tionnisme comme certains le prétendent, mais
bien au contraire le début d’une tentative
d’étude des organismes vivants dans leur
entière complexité, en intégrant un maximum
d’informations.
Dans cette aventure, la transgenèse fait le lien
entre l’élément réduit qu’est le gène isolé et
ses effets biologiques dans le contexte com-
plexe qu’est l’animal. Cela explique l’éclosion
d’ateliers publics et privés, dont la fonction
est d’obtenir en série des animaux transgé-
niques, et d’animaleries pour les abriter.
La transgenèse offre d’autres possibilités plus
directement appliquées, dont certaines sont
déjà devenues réalité. Dans le domaine médical,
les animaux transgéniques sont des modèles
sans précédent pour l’étude de certaines
maladies humaines et la mise au point de
médicaments. Il n’est pas impossible que des
cellules et certains organes de porc (cœur,
rein, foie, etc.) deviennent immunologique-
ment tolérés par des patients lorsque certains
gènes auront été transférés aux animaux. Il
est admis que le lait et le blanc d’œuf d’ani-
maux transgéniques vont devenir une des
sources essentielles de protéines recombi-
nantes pour des usages thérapeutiques. L’autre
grand domaine d’application de la biologie,
l’agroalimentaire, va également bénéficier
progressivement de la transgenèse, comme
cela est déjà le cas pour les plantes. Les éle-
veurs pourront ainsi résoudre des problèmes
en face desquels la sélection génétique est
impuissante.
Les techniques de transgenèse
Le nombre de laboratoires dans lesquels la
transgenèse animale est pratiquée de manière
courante reste limité à une bonne cinquan-
taine en France. Ce potentiel répond tout juste
aux besoins des chercheurs. La raison en est
clairement que la transgenèse comporte des
contraintes qui sont relativement dissuasives.
La méthode presque exclusivement utilisée
pour obtenir des souris transgéniques repose
sur la microinjection d’ADN dans le noyau
des embryons d’un jour. Le remplacement de
gène implique la manipulation de cellules ES
et de blastocystes, méhode bien plus lourde
encore. À cela, il faut ajouter le poids de la
mise à disposition d’animaleries conséquentes
et du personnel nécessaire pour prendre soin
des animaux.
L’utilisation des animaux transgéniques ne
pose par contre pas de difficultés particu-
lières, même si des règles de biosécurité – qui
seront décrites plus loin – doivent être res-
pectées. L’ensemble des techniques de trans-
gènes sont décrites dans plusieurs livres
récents (1-3).
La construction des vecteurs
d’expression des transgènes
Dans la plupart des cas, l’expérimentateur ne
souhaite pas uniquement transférer un gène
natif mais bien une combinaison de promo-
teur de gène rapporteur, etc. Ces assemblages
ne posent pas de difficulté particulière puis-
qu’ils font appel aux techniques classiques du
génie génétique.
Une mention particulière doit toutefois être
faite pour les vecteurs comportant de longs
fragments d’ADN. Ces situations se rencon-
trent de plus en plus fréquemment. Il est en
effet parfois souhaitable d’introduire dans un
animal d’assez longs fragments d’ADN
génomique qui seuls contiennent l’ensemble
des éléments régulateurs d’un gène. Pour les
mêmes raisons, il est avantageux d’utiliser de
longs fragments d’ADN génomique, conte-
nant l’ensemble des éléments régulateurs
d’un gène ou d’un locus, pour faire exprimer
un gène étranger. Cela suppose que le gène
en question ait été introduit précisément dans
un site du locus. Ces opérations ne peuvent
pas se faire dans un tube Eppendorf, comme
la construction classique de plasmides.
L’introduction d’un fragment d’ADN étran-
ger dans un vecteur BAC (bacterial artifical
chromosome) de 50-300 kb ou un vecteur
YAK (yeast artifical chromosome) ne peut se
faire que par recombinaison homologue réa-
lisée à l’intérieur d’une bactérie ou d’une
levure. Les meilleures techniques actuellement
utilisées dans ce but ont été résumées et com-
mentées dans une publication récente (1).
La plus grande difficulté rencontrée pour
construire un vecteur d’expression pour un
transgène tient surtout dans le choix des élé-
ments à assembler.
Les toutes premières expériences de transgé-
nèse, puis de nombreuses autres qui ont suivi,
Dossier : Génomique, recherche et thérapie en endocrinologie

Act. Méd. Int. - Métabolismes - Hormones - Nutrition, Volume V, n° 6, novembre-décembre 2002
242
ont révélé que les transgènes fonctionnent in
vivo de manière quelque peu imprévisible. Le
transgène est très peu actif, voire totalement
inactif, dans nombre de lignées. Le transgène
s’exprime, par ailleurs, plus ou moins dans
des tissus autres que celui dans lequel le pro-
moteur utilisé est normalement actif.
Il est admis que ces événements sont dus à
des effets de position. La microinjection
introduit l’ADN étranger dans des sites très
variables du génome. La chromatine exerce
des effets stimulateurs ou inhibiteurs sur les
transgènes par l’intermédiaire d’amplifica-
teurs ou de silenceurs qui se trouvent au voi-
sinage de l’ADN intégré.
La réalité est en fait plus subtile. Le nombre
de cas où un transgène reste silencieux est
relativement élevé, ce qui laisse supposer que
la chromatine contient de nombreux silen-
ceurs.
De nombreuses expériences démontrent qu’un
transgène a d’autant plus de chance de
s’éteindre qu’il contient un ADNc plutôt
qu’un fragment génomique comportant des
introns ou des séquences riches en CpG
(notamment de l’ADN d’origine bacté-
rienne) et qu’il est intégré sous forme de
copies multiples (5, 6). Il semble donc que
les transgènes dont l’organisme ne peut pas
se débarrasser soient facilement éteints, vrai-
semblablement par des mécanismes qui inac-
tivent les transposons et les rétrovirus. Il est
vraisemblable que l’inactivation des trans-
gènes a lieu dès la vie embryonnaire précoce,
au moment où le génome se méthyle sélecti-
vement et où sont définis les gènes qui reste-
ront silencieux (7).
Pour éviter ces inconvénients, il est néces-
saire de modifier les gènes pour réduire leur
contenu en CpG, d’ajouter des introns (au
moins un, plutôt devant l’ADNc) et surtout
d’ajouter des isolateurs de gènes devant le
promoteur (et éventuellement après le termi-
nateur) (8), ou de longs fragments d’ADN
génomique contenant des isolateurs. Ces iso-
lateurs sont constitués d’un ensemble d’élé-
ments qui empêchent l’hétérochromatine
inactive de propager sa structure compacte
jusqu’au transgène et qui maintiennent la
chromatine dans une conformation ouverte.
Les ouvreurs de chromatine favorisent l’acé-
tylation locale des histones H3 et H4 et s’op-
posent à leur méthylation ainsi qu’à la méthy-
lation de l’ADN (9).
D’autres règles doivent être respectées pour
optimiser l’expression des transgènes. Les
codons peuvent être mutés pour être adaptés
au mieux à la cellule dans laquelle ils doivent
fonctionner. Un intron ajouté après un ADNc
ne doit pas être éloigné de plus de 50 bp du
codon de terminaison, sous peine de déclen-
cher un mécanisme de destruction de l’ARNm,
mécanisme appelé NMD (non sense mediated
decay). Les ADNc ne doivent pas contenir des
régions 5’UTR (untranslated region) riches
en GC et hautement structurées. Les régions
3’UTR ne doivent pas contenir des séquences
riches en AU qui déstabilisent les ARNm.
Ces recommandations sont résumées dans un
chapitre du livre édité par C.A. Pinckert (10).
L’expression simultanée
de plusieurs transgènes
Pour exprimer simultanément deux gènes ou
ADNc, deux constructions indépendantes
peuvent être coinjectées. Elles seront cointé-
grées avec une fréquence de 70 % environ.
Une séquence IRES (internal ribosome entry
site) peut être introduite entre les deux ADNc
d’un gène bicistronique. L’utilisation des
IRES doit suivre des règles et il faut considé-
rer que, dans la majorité des cas, les ADNc
sont moins bien exprimés que chacun d’entre
eux introduit dans un vecteur propre (11).
L’expression conditionnelle
des transgènes
Un modèle biologique est d’autant plus inté-
ressant que le transgène ne s’exprime que là
et lorsque l’expérimentateur le souhaite.
Plusieurs familles de vecteurs ont été définies
pour n’exprimer leur transgène que sous l’in-
fluence d’inducteurs exogènes n’agissant pas
sur les gènes de l’hôte. Le système tétracycline
est le plus utilisé. Une des versions les plus
sophistiquées est décrite dans la figure 1. La
souris doit exprimer simultanément trois
gènes: deux gènes régulateurs (KRAB et tet
on) et le gène d’intérêt. L’addition de doxy-
cycline à l’eau de boisson des souris induit
réversiblement l’expression du gène d’intérêt.
Les deux régulateurs assurent un bruit de
fond très réduit et une bonne induction par la
doxycycline.
Dossier : Génomique, recherche et thérapie en endocrinologie
I
R
A
R
A+
R
I
R
–
KRAB
KRAB
gène d'intérêt
promoteur
promoteur gène d'intérêt
promoteur
pas d'expression haute expression
IRES tet on
tet on
+ doxycycline
– doxycycline
terminateurintronisolateur
Figure 1. Le contrôle des transgènes par la doxycycline. Des souris exprimant deux facteurs de transcription
KRAB et tet on sont croisées avec des souris portant le gène d’intérêt placé sous la dépendance des deux fac-
teurs de transcription. En absence de doxycycline, le silenceur KRAB inhibe l’expression du gène d’intérêt.
En présence de doxycycline, le facteur tet on prend la place du facteur KRAB et stimule l’expression du gène
d’intérêt.

Act. Méd. Int. - Métabolismes - Hormones - Nutrition, Volume V, n° 6, novembre-décembre 2002
243
Le remplacement de gènes
et l’intégration ciblée
Le remplacement de gènes et leur intégration
ciblée reposent sur un processus de recombi-
naison homologue. Ceux-ci sont peu fréquents.
Les cellules où le remplacement de gène a eu
lieu doivent être sélectionnées à l’aide de
vecteurs similaires à celui décrit dans la
figure 2.
Une construction de gène peut être ciblée
dans un site préalablement choisi du génome
dans lequel a été introduite une séquence
LoxP. La recombinase Cre permet au vecteur
possédant lui-même une séquence LoxP de
s’introduire dans le site LoxP du génome
(figure 3). Le remplacement de gène permet
de substituer un gène donné par des allèles
naturels ou définis par l’expérimentateur ou
par tout autre gène. Dans le premier cas, on a
le plus souvent réalisé l’invalidation du gène
(knock out) et, dans le second, une opération
désignée par knock in. Le ciblage par le sys-
tème Cre LoxP permet d’introduire de mul-
tiples versions d’un gène dans le même site.
Cela limite les effets de position sur le trans-
gène à ceux intrinsèques au site choisi.
L’inhibition d’un gène de l’hôte
Il est aussi important d’inhiber un gène endo-
gène que d’apporter un gène supplémentaire
dans un génome. Cette démarche a plus de
chance de révéler le rôle d’un gène qui est
devenu manquant. L’invalidation de gène par
recombinaison homologue même optimisée
en la restreignant à un type cellulaire donné
et à une période précise de la vie de l’animal
est contraignante et elle présente l’inconvé-
nient d’être irréversible. L’expression peut
être obtenue par des outils très différents qui
agissent aux diverses étapes de l’expression
génétique.
Les régions composées de polypurines (au
moins 20) peuvent former une triple hélice
stable avec un ADN ou un ARN simple brin
anticomplémentaire. Une telle triple hélice
s’oppose à la transcription du gène ciblé. Ce
système a fait ses preuves in vitro dans des
cellules en culture (12). Plusieurs tentatives
pour transposer cette technique chez les ani-
maux transgéniques se sont soldées par des
échecs. Les animaux qui naissent ne sont pas
transgéniques ou n’expriment pas leur trans-
gène. Cela suggère qu’un simple brin anti-
complémentaire composé seulement de
purines reconnaît de multiples séquences du
génome et rend les embryons non viables.
Dossier : Génomique, recherche et thérapie en endocrinologie
A
B
Recombinaison homologue
Neo
Neo
ADN
génomique
ADN
génomique
TK
Vecteur de
recombinaison
(G 418 r, ganc r)
(G 418 r, ganc s)
Recombinaison hétérologue
Neo TK
Vecteur de
recombinaison
Neo TK
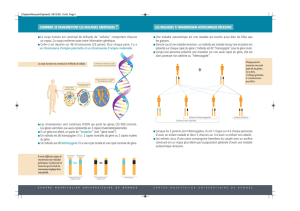
Figure 2. Les vecteurs avec double sélection sont utilisés pour éliminer les cellules dans lesquelles une recom-
binaison illégitime (ou hétérologue) a eu lieu. Les régions homologues qui se recombinent sont indiquées par
des croix. Le gène neo confère la résistance des cellules au G 418 tandis que le gène TK est létal pour les cellules
mises en présence de ganciclovir. Les cellules ES ainsi sélectionnées sont introduites dans des blastocystes.
ADN
génomique
recombinase
Cre
intégration
au hasard
gène d'intérêt
gène
d'intérêt
isolateurisolateur
isolateur isolateur
Lox P
Lox P
Lox P
isolateur isolateur
Lox P
Lox P
Figure 3. Principe de l’intégration ciblée d’un gène
en un site donné du génome. Un site LoxP conte-
nant 35 paires de bases est introduit dans le génome
par recombinaison homologue, ou au hasard par
microinjection. Le site retenu peut recevoir une
construction de gène portant elle aussi un site
LoxP. La recombinase Cre est apportée dans l’em-
bryon en coinjectant un plasmide circulaire expri-
mant le gène Cre et la construction à intégrer. Le
site LoxP peut avoir été bordé par un isolateur pour
réduire les effets de position des gènes intégrés dans
ce site.

Act. Méd. Int. - Métabolismes - Hormones - Nutrition, Volume V, n° 6, novembre-décembre 2002
244
Dossier : Génomique, recherche et thérapie en endocrinologie
Des ARN antisens monocatenaires peuvent
en principe s’associer spécifiquement à un
ARNm et inhiber sa traduction. Un ARN
antisens est encore plus puissant lorsqu’il
contient un ribozyme qui clive l’ARNm ciblé.
Ces outils sont en pratique peu performants
car les deux partenaires ARNs complémen-
taires ne se rencontrent pas aisément dans
une cellule. Les ARNs sont souvent confor-
més en structure secondaire et associés à des
protéines qui s’opposent à une association
avec un autre ARN complémentaire. L’asso-
ciation d’une hélicase au ribozyme augmente
nettement son efficacité, qui peut être plus
élevée lorsqu’on choisit des régions de
l’ARNm cible qui sont sous forme monoca-
tenaire (13).
La découverte récente de l’interférence de
l’ARN offre des perspectives particulière-
ment intéressantes chez les organismes pluri-
cellulaires. De longs ARNs en double brin
(300 bp) induisent une destruction sélective
et intense d’un ARN ayant une séquence
complémentaire. On sait maintenant que
l’ARN double brin est clivé en fragment de
21-23 paires de bases ayant 2-3 nucléotides
saillants en 3’OH. Ces structures ciblent
l’ARN correspondant et induisent une RNAse
qui détruit l’ARN (figure 4). Ce phénomène
permet en routine de cibler les ARNms chez
la drosophile ainsi que chez le Caenorhabditis
elegans via la transgenèse. Chez les vertébrés,
et notamment les mammifères, le phénomène
n’est pas observé aussi aisément. Les ARN
double brin de 30 bp ou plus induisent
l’interféron et un arrêt de la synthèse pro-
téique. Des ARNs double brin synthétiques
de 21-23 bp transfectés dans les cellules inhi-
bent parfaitement l’ARN ayant la même
séquence. Des expériences récentes ont mon-
tré que de tels ARNs pouvaient être synthéti-
sés dans les cellules par des vecteurs trans-
crits par l’ARN polymérase III. C’est le cas
pour le promoteur du gène U6. Le transfert
de ces constructions de gène inhibe spécifi-
quement les ARNs cellulaires ou viraux. Ces
résultats établis avec des cellules devraient
pouvoir l’être également in vivo via la trans-
génèse.
Le mécanisme d’interférence de l’ARN peut
être un des moyens de contrôler l’expression
des gènes cellulaires. Il semble que ce soit
aussi un moyen de défense contre des
génomes viraux. Pour l’expérimentateur, les
ARNi (double brin ayant un effet interférent)
représentent un équivalent plus simple et plus
souple que l’inactivation de gène par recom-
binaison homologue pour arrêter l’expression
d’un gène.
La dernière étape de l’expression génétique
sur laquelle l’expérimentateur peut agir est la
protéine elle-même. L’expression intense
d’une protéine mutante exerçant un effet
leurre sur ses partenaires cellulaires peut
inhiber les effets de la protéine normale. De
telles protéines leurres sont pour cette raison
appelées “transdominants négatifs”. Les vec-
teurs conventionnels permettent une surex-
pression de tels gènes.
Les applications biologiques
et médicales de la transgenèse
Comme il vient d’être mentionné, la trans-
genèse permet de créer toutes sortes de
mutants conditionnels qui apportent aux
expérimentateurs des outils incomparables
pour décrypter les mécanismes cellulaires les
plus variés. La transgenèse permet également
l’obtention de modèles pour l’étude de mala-
dies humaines que n’autorise pas le simple
élevage de souris.
Les modèles animaux pour l’étude
des maladies humaines
Obtenir un modèle animal pertinent pour
l’étude d’une maladie humaine n’est pas une
chose aussi simple qu’il y paraît. Des lignées
de souris transgéniques peuvent souvent ne
mimer que très partiellement la maladie. C’est
notamment le cas des cancers. Il est admis
qu’une tumeur dérive d’une seule cellule qui
a subi toutes les mutations des oncogènes et
des antioncogènes qui caractérisent la cellule
cancéreuse. Ces mutations et leurs combinai-
sons sont multiples. La souris transgénique
n’est que rarement aussi subtile. Un système
permettant une activation aléatoire et donc
monoclonale du gène K-ras a permis d’obtenir
des souris transgéniques reflétant mieux que
les précédentes le cancer de la vessie.
Les maladies résultant d’une dégénérescence
cellulaire sont multifactorielles et se déve-
loppent lentement. Divers modèles de souris
pour l’étude de la maladie d’Alzheimer ont
ainsi pu être obtenus. Ces animaux permettent
une description satisfaisante de la maladie
mais aussi la mise au point de nouvelles sub-
stances chimiques qui sont autant de médica-
ments candidats.
ARNm
RNAse
RNAse
géne codant pour
un ARN double brin
ARN double brin
plasmide
transfection
ou injection
transfection
ou injection
transfection
ou injection
Figure 4. Inhibition de l’expression d’un gène par
l’interférence de l’ARN. Un ARN double brin d’au
moins 300 bp est clivé en fragments qui ciblent
l’ARN cellulaire correspondant, ou le dégradent.
Les ARN interférents de 21-23 bp peuvent être
introduits dans les cellules par transfection ou
microinjection ou être synthétisés par des vecteurs
appropriés, notamment celui du gène de l’ARN U6
qui est transcrit par l’ARN polymérase III.
 6
6
 7
7
 8
8
1
/
8
100%