Arguments pour l’intégration des biomarqueurs théranostiques de la

Correspondances en Onco-Théranostic - Vol. I - n° 4 - octobre-novembre-décembre 2012
174
Réparation
dossier thématique
Arguments pour l’intégration
des biomarqueurs théranostiques de la
réparation de l’ADN en pratique clinique
dans le cancer bronchopulmonaire
A case for the integration of theranostic markers of DNA repair
into the clinical management of lung cancer
Tony Sourisseau*, Ken Olaussen*, Jean-Charles Soria*
* Institut Gustave Roussy,
Villejuif.
RÉSUMÉ
Summary
»
L’altération de la machinerie de réparation de l’ADN est à la base
de l’instabilité génomique observée dans les cellules cancéreuses,
mais elle ouvre également, dans le même temps, des opportunités
thérapeutiques. Parmi les marqueurs sur lesquels s’appuie
l’émergence d’une médecine personnalisée pour le traitement
des cancers bronchopulmonaires, les facteurs de réparation de
l’ADN figurent au nombre des plus prometteurs. Comment ces
biomarqueurs peuvent-ils guider l’élaboration d’une stratégie
thérapeutique efficace et personnalisée, et quelles sont les
bases mécanistiques de l’activité thérapeutique des inhibiteurs
pharmacologiques de ces facteurs ? Nous aborderons ces questions
en particulier dans le cadre des cancers bronchiques non à petites
cellules au travers de plusieurs biomarqueurs de la réparation :
ERCC1, MGMT, MSH2, BRCA1, PARP, RRM1, TS et DNAPK. Nous
discuterons la valeur clinique de ces marqueurs dans le traitement
des cancers du poumon, et nous verrons comment la connaissance
fondamentale de la réparation de l’ADN et l’amélioration des
technologies de biologie moléculaire devraient permettre d’intégrer
ces marqueurs dans la pratique clinique.
Mots-clés : Cancer du poumon − Réparation de l’ADN − Biomarqueurs.
Alterations of the DNA repair machinery is at the heart
of the genomic instability displayed by most cancer cells
but can also open therapeutic opportunities. Amongst the
biomarkers enabling the development of a personalized
medicine for the treatment of lung cancer, DNA repair
factors stand among the most promising. How can these
biomarkers guide the design of personalised and efficient
therapeutic strategies and what is the mechanistic basis of
the therapeutic activity of their pharmacologic inhibitors?
This review aims to address these questions in the context
of lung cancer, in particular non-small-cell lung cancer
through several DNA repair biomarkers: ERCC1, MGMT,
MSH2, BRCA1, PARP, RRM1, TS and DNAPK. We will discuss
the clinical value of these markers for the treatment of
lung cancer, and how basic knowledge of DNA repair as
well as the constant improvement of molecular biology
technologies should enable these biomarkers to be
successfully integrated into the clinic.
Keywords : Lung cancer − DNA repair − Biomarkers.
Introduction
Le cancer, une maladie de (la réparation de) l’ADN
L’ADN de nos cellules est exposé à des dizaines de mil-
liers de lésions par jour. Ces lésions proviennent de
l’environnement ou de métabolites produits lors du
fonctionnement cellulaire normal (1). Nombre de ces
dommages sont potentiellement létaux, mais un pro-
gramme cellulaire est chargé de les éliminer : la réponse
aux dommages de l’ADN. L’une des phases majeures
de cette réponse est la réparation de l’ADN, assurée par
une série de voies de réparation. Cet arsenal moléculaire
est indispensable au fonctionnement cellulaire normal,
à l’homéostasie tissulaire et à la stabilité génomique.
Il n’est donc pas surprenant que des anomalies de la
machinerie de réparation de l’ADN soient à l’origine de
nombreuses pathologies, parmi lesquelles le cancer (2).
Un grand nombre d’altérations héréditaires de la
réponse aux dommages de l’ADN est en effet associé
à une prédisposition congénitale au cancer. Par ailleurs,
les propriétés oncogènes sont souvent associées à la
capacité d’une molécule à endommager l’ADN (3). Il y a

Correspondances en Onco-Théranostic - Vol. I - n° 4 - octobre-novembre-décembre 2012
175
Arguments pour l’intégration des biomarqueurs théranostiques de la réparation de l’ADN
en pratique clinique dans le cancer bronchopulmonaire
donc un rapport de causalité très clair, quoique difficile
à démontrer, entre la capacité à prendre en charge des
dommages de l’ADN et le cancer (4).
Les cancers bronchopulmonaires
Les cancers bronchopulmonaires présentent principa-
lement 2 types histologiques : les cancers bronchiques
non à petites cellules (CBNPC) et les cancers bron-
chiques à petites cellules (CBPC). Ces 2 types de cancers
diffèrent par leur fréquence, leur origine cellulaire, leur
pronostic vital et leur prise en charge thérapeutique.
Même si les altérations héréditaires de la réponse aux
dommages de l’ADN sont peu décrites dans le cancer
bronchopulmonaire, leur incidence est étroitement liée
à l’exposition à des molécules créant des dommages de
l’ADN, comme les agents alky lants présents en grand
nombre dans la fumée de cigarette (5).
Les dommages de l’ADN et leur réparation,
un moteur de la carcinogenèse mais aussi
une opportunité pour le traitement
Les perturbations de la réponse aux dommages de
l’ADN sont donc sans doute à l’origine du développe-
ment de la plupart des cancers. Par ailleurs, l’activité
thérapeutique de nombreux agents anticancéreux
est basée sur leur capacité à endommager l’ADN
dans les cellules tumorales. Nous voyons donc qu’une
connaissance détaillée des événements moléculaires
associés à la réponse aux dommages de l’ADN et à
leur régulation est non seulement indispensable à
la compréhension des mécanismes de la tumorige-
nèse, mais devrait également permettre de mieux
comprendre l’activité des agents thérapeutiques et
d’en améliorer l’efficacité.
Cet article se propose de présenter les facteurs de répa-
ration de l’ADN les plus prometteurs pour une inté-
gration dans la prise en charge clinique des cancers
pulmonaires, que ce soit pour leur valeur pronostique
ou prédictive de la réponse au traitement anticancéreux,
ou bien en tant que cibles thérapeutiques.
ERCC1 et la voie NER
La voie NER (Nucleotide Excision Repair) prend en
charge la réparation des adduits de l’ADN induisant
un encombrement stérique suffisamment important
pour perturber la conformation en double hélice de
l’ADN (figure). L’exposition aux sels de platine provoque
de telles lésions de l’ADN. Les effets thérapeutiques du
platine sont par conséquent étroitement liés à l’effica-
cité de la voie NER, dont l’une des étapes clés est assu-
rée par ERCC1 (Excision Repair Cross-Complementing
group 1).
L’expression d’ERCC1 a une valeur prédictive du béné-
fice de la chimiothérapie adjuvante dans les cancers
bronchiques opérés (6). Le traitement adjuvant à base
de cisplatine profite aux patients dont la tumeur pré-
sente une faible expression d’ERCC1 mais n’apporte
aucun bénéfice à ceux dont la tumeur exprime de
hauts niveaux protéiques d’ERCC1, comme l’a montré
la mesure de son expression sur des pièces opérées de
CBNPC provenant de 783 patients inclus dans l’essai
IALT (International Adjuvant Lung cancer Trial).
Outre sa valeur prédictive, le niveau d’expression
d’ERCC1 a une valeur pronostique en l’absence de tout
traitement. Une expression élevée d’ERCC1 est en effet
associée à un diagnostic favorable.
Étant donné l’impact de l’activité d’ERCC1 sur la réponse
aux chimiothérapies génotoxiques, le contrôle phar-
macologique de son activité pourrait avoir un intérêt
thérapeutique évident. La fonction d’ERCC1 dans la voie
NER se prête mal au développement d’inhibiteurs phar-
macologiques, mais des données précliniques récentes
suggèrent que des molécules anticancéreuses peuvent
avoir des effets intéressants sur son activité (7).
MGMT et la voie DR
La voie de réparation DR (Direct Repair) prend en charge
la réparation des adduits de faible encombrement sté-
rique, tels que les méthylations de guanines. Dans la
mesure où une guanine méthylée s’apparie de préfé-
rence avec une thymine lors de la réplication, ces lésions
peuvent être mutagènes et cancérigènes, ou bien être
toxiques dans le cadre d’une thérapie anticancéreuse.
La MGMT (O-6-methylguanine-DNA methyltransferase),
aussi connue sous le nom d’alkylguanine alkyltransfé-
rase (AGT), catalyse l’élimination de ces groupements
méthyle. En participant ainsi à la détoxification des
cellules traitées par des agents alkylants utilisés en
chimiothérapie, la MGMT peut jouer un rôle prépon-
dérant dans l’échec du traitement. L’inhibition pharma-
cologique de la MGMT dans le but de potentialiser les
effets du témozolomide ou d’autres agents alkylants est
un champ d’investigation très actif (8) [tableau, p. 176].
MSH2 et la voie MMR
MSH2 est un facteur essentiel de la voie MMR (MisMatch
Repair) [figure], qui prend en charge de nombreuses
lésions provoquées par des agents alkylants ou dues

Correspondances en Onco-Théranostic - Vol. I - n° 4 - octobre-novembre-décembre 2012
176
dossier thématique
Réparation
à des erreurs lors de la réplication de l’ADN. À l’instar
d’ERCC1, les niveaux d’expression de MSH2 semblent
avoir une valeur à la fois pronostique et prédictive.
En l’absence de traitement, les patients MSH2-positifs
ont en effet un meilleur pronostic que les patients
MSH2-négatifs. Par ailleurs, une faible expression de
MSH2 est corrélée à une meilleure réponse à la chimio-
thérapie à base de sels de platine dans certains CBNPC
à des stades avancés (9).
Enfin, certains travaux suggèrent une corrélation entre
la perte d’expression de MSH2, courante dans les CBNPC,
et une sensibilité à l’inhibition de la dihydrofolate réduc-
tase par le méthotrexate (10). Les niveaux d’expression
de MSH2 sont donc potentiellement un indicateur de
la réponse au pémétrexed, un autre inhibiteur de la
dihydrofolate réductase utilisé pour le traitement de
nombreux cancers bronchopulmonaires.
BRCA1 et la voie RH
BRCA1 (BReast CAncer 1, early onset) joue un rôle essen-
tiel dans la réparation des cassures double-brin par
recombinaison homologue (RH) [figure]. Des muta-
tions congénitales du gène prédisposent aux can-
cers du sein et de l’ovaire, et confèrent dans le même
temps une sensibilité aux inhibiteurs de PARP [Poly
(ADP-Ribose) Polymerase] par un mécanisme de létalité
Tableau. Exemples d’essais cliniques sur les cancers bronchopulmonaires impliquant des facteurs de réparation de l’ADN.
Biomarqueur/
cible thérapeutique Intervention
thérapeutique Identifiant Titre de l’étude
ERCC1 Cisplatine NCT00775385 TAilored post-surgical therapy in early stage NSCLC (TASTE)
ERCC1, RRM1 Gemcitabine, cisplatine NCT00792701 Gemcitabine and cisplatin in treating patients with stage I non-small cell
lungcancer that was removed by surgery
Carboplatine, gemcitabine,
docétaxel, vinorelbine
NCT00736814 First-line combination chemotherapy in treating patients with stage IIIB
orstage IV non-small cell lung cancer that cannot be removed by surgery
NCT00499109 Phase III of RRM1 & ERCC1 directed customized chemotherapy for the treatment
of patients with NSCLC
NCT01648517 Genotype-driven treatment of advanced non-small cell lung cancer based
onmRNA expression of ERCC1 & RRM1 as first-line chemotherapy
NCT00215930 MADe IT: molecular analyses directed individualized therapy for advanced
non-small cell lung cancer
BRCA1 Docétaxel, cisplatine,
gemcitabine
NCT00478699 Randomized customized adjuvant chemotherapy (GECP-SCAT)
BRCA1, RRM1 Gemcitabine, docétaxel,
cisplatine, irinotécan
NCT01424709 Individualized chemotherapy based on BRCA1 and RRM1 mRNA
for advanced non-small cell lung cancer (NSCLC) [BRAVO]
ERCC1, RRM1, BRCA1 Cisplatine, gemcitabine,
docétaxel, vinorelbine,
pémétrexed
NCT00705549 Individualized therapy based of tumoral mRNA levels of ERCC1, RRM1
andBRCA1 in advanced non-small cell lung cancer
PARP1 Gemcitabine, carboplatine,
iniparib
NCT01082549 Trial of gemcitabine/carboplatin with or without iniparib (SAR240550)
[aPARP1 inhibitor] in subjects with previously untreated stage IV squamous
non-small cell lung cancer (NSCLC) [ECLIPSE]
Gemcitabine, cisplatine,
SAR240550
NCT01086254 SAR240550 in combination with gemcitabine/cisplatin in non-small cell lung
cancer
Thymidylate synthase Gemcitabine, cisplatine,
pémétrexed
NCT01401192 Pemetrexed/cisplatin versus gemcitabine/cisplatin according to thymidylate
synthase expression
Pémétrexed, cisplatine NCT00887549 A study of thymidylate synthase expression in patients with non-small cell lung
cancer
TS, ERCCI, RRM1 Cisplatine, gemcitabine,
pémétrexed
NCT01194453 Pemetrexed plus cisplatin versus gemcitabine plus cisplatin for advanced
andmetastatic non-small cell lung cancer (AP/GP)
MGMT Lomustine NCT00293280 Lomustine in treating patients with stage III or stage IV non-small cell lung
cancer
ERCC1, ERCC2, XRCC1, XRCC3,
BRCA1, RRM1
Chimiothérapies
néoadjuvantes
NCT00797238 DNA repair genes and outcomes in patients with stage III NSCLC

Correspondances en Onco-Théranostic - Vol. I - n° 4 - octobre-novembre-décembre 2012
177
Arguments pour l’intégration des biomarqueurs théranostiques de la réparation de l’ADN
en pratique clinique dans le cancer bronchopulmonaire
synthétique. Dans le poumon, même si BRCA1 n’est
que rarement muté, il semble que son expression,
fréquemment dérégulée, ait une valeur pronostique.
Dans les stades précoces de CBNPC, de forts niveaux de
l’ARNm de BRCA1 sont en effet associés à un pronostic
défavorable (11, 12).
Sensibilité aux chimiothérapies
Les niveaux d’ARNm de BRCA1 pourraient par ailleurs
guider le choix du traitement des CBNPC. Une étude
préclinique sur des modèles ex vivo montre en effet
que des niveaux élevés de messagers BRCA1 sont
associés à une résistance aux agents génotoxiques
et, dans le même temps, à une sensibilité aux poi-
sons des microtubules. A contrario, les cellules pré-
sentant une faible expression de BRCA1 résistent
aux taxanes, mais sont sensibles aux dommages
de l’ADN (13).
PARP et la voie BER (Base Excision Repair)
Les déficiences de PARP1 rendent les cellules hypersen-
sibles aux cassures double-brin de l’ADN. Les inhibiteurs
de PARP sont de ce fait de puissants sensibilisateurs aux
irradiations et au cisplatine (14, 15). On perçoit donc
clairement la justification mécanistique de l’association
d’un inhibiteur de PARP aux chimiothérapies à base de
platine ou à la radiothérapie.
DNAPK et la voie NHEJ
La DNAPK (DNA-dependent Protein Kinase) est un com-
plexe enzymatique essentiel à la voie de réparation
des cassures double-brin NHEJ (Non-Homologous End
Joining) [figure]. Une réduction de l’activité de DNAPK
a été associée à un accroissement du risque de CBNPC,
et l’activité cytotoxique d’agents thérapeutiques peut
être augmentée dans les CBNPC par l’inhibition phar-
macologique de la DNAPK (16, 17).
Enzymes de la biosynthèse des nucléotides
La disponibilité des nucléotides est essentielle à
une réparation efficace des dommages de l’ADN,
et le ciblage de la biosynthèse nucléotidique peut
avoir un effet toxique sur les cellules cancéreuses en
inhibant la réparation. Deux enzymes participant à la
biosynthèse des nucléotides sont les cibles d’agents
anticancéreux.
RRM1
Les niveaux d’expression de RRM1 (Ribonucleotide
Reductase M1), dont l’activité est inhibée par la gem-
citabine, ont une valeur pronostique et peuvent prédire
la réponse à la gemcitabine (18, 19). Des études cliniques
sont en cours pour confirmer ces résultats (tableau).
Thymidylate synthase
La thymidylate synthase (TS) est une cible majeure
du pémétrexed, dont l’effet thérapeutique est étroite-
ment lié à son niveau d’expression, comme l’illustre la
sensibilité plus faible des carcinomes épidermoïdes,
tumeurs exprimant de hauts niveaux de TS, comparés
aux adénocarcinomes, qui en expriment des niveaux
moindres (20).
Combinaison de marqueurs
de la réparation
Les biomarqueurs que nous avons décrits ont une
valeur prédictive ou diagnostique plus ou moins fiable.
Pourquoi ne pas les combiner pour affiner les prédic-
tions ? C’est une possibilité actuellement testée par de
nombreuses études cliniques (tableau). Plusieurs études
prospectives étudient par exemple la possibilité d’uti-
liser les niveaux d’expression de RRM1 et ERCC1 pour
guider le choix du doublon le plus efficace combinant
gemcitabine, sel de platine et poison du microtubule.
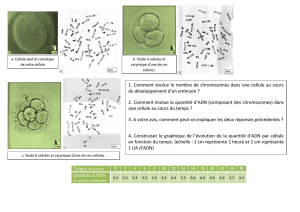
Figure. Principaux types de lésion de l’ADN, voies de réparation correspondantes et bio marqueurs
associés.
Lésions de l’ADN
Cassure simple-brin
Lésion de base
BER NER MMRDR NHEJ
Voies de
réparation
Valeur
pronostique
Valeur
prédictive
Ciblage
thérapeutique
Biomarqueurs
Adduits/
déformation Mésappariement
Méthy-
lation
HR
Cassure double-brin

Correspondances en Onco-Théranostic - Vol. I - n° 4 - octobre-novembre-décembre 2012
178
Réparation
dossier thématique
Une stratégie similaire peut être employée en utilisant
les niveaux d’expression d’ERCC1 et de BRCA1, qui pour-
rait guider le choix entre une thérapie basée sur les
sels de platine ou sur des poisons du microtubule (21).
Mise en place de tests fonctionnels
de la réparation de l’ADN
La connaissance du statut fonctionnel des différentes
voies de réparation est extrêmement précieuse, mais
difficile à acquérir. La compréhension des mécanismes
moléculaires de la réparation ainsi que les progrès tech-
nologiques récents ont toutefois rendu cette perspec-
tive envisageable.
Il est par exemple possible de visualiser dans les cellules
tumorales certains dommages de l’ADN, comme les cas-
sures double-brin ou les adduits de platine, en utilisant
un anticorps reconnaissant l’histone H2A phosphorylée
ou l’anticorps R-C18, respectivement. La cinétique de
réparation de ces lésions par RH ou NER est ainsi acces-
sible sur des échantillons de tumeur et peut guider un
choix thérapeutique.
L’activité de la RH peut par ailleurs être directement
évaluée en détectant la formation de foci nucléaires
de la recombinase RAD51.
Enfin, les méthodes récentes de séquençage et l’utilisation
en routine de techniques telles que la CGH (Comparative
Genomic Hybridization) permettent désormais d’obtenir le
“spectre mutationnel” d’une tumeur et de révéler ainsi la
dérégulation d’une voie de réparation. On sait par exemple
que certaines déficiences de la voie RH entraînent des
réarrangements génomiques caractéristiques qui peuvent
être mis en évidence par ces approches.
Conclusion
Les progrès dans la prise en charge des cancers bron-
chopulmonaires peuvent être attribués à une poignée
d’avancées marquantes. La prochaine pourrait-elle
être l’intégration des marqueurs de la réparation de
l’ADN dans la pratique clinique ? Ces biomarqueurs
permettent une personnalisation du diagnostic, mais
offrent également une base mécanistique au choix
thérapeutique, à tel point que certains auteurs sug-
gèrent de baser la classification des tumeurs sur leurs
capacités de réparation, en sus de leur origine tissulaire
et de leurs caractéristiques histologiques.
L’utilisation des marqueurs de la réparation de l’ADN en
clinique reste néanmoins confrontée à un certain nombre
d’obstacles. La standardisation des procédures de mesure
et d’analyse des niveaux d’expression entre différents
centres d’analyse reste un problème majeur.
Plusieurs perspectives technologiques et méthodolo-
giques s’ouvrent cependant. L’utilisation des cellules
tumorales circulantes, des cellules sanguines ou même
de l’ADN circulant dans le sérum ouvre des possibilités
nouvelles, et pourrait par exemple permettre des études
pharmacodynamiques de la réponse aux thérapies (22).
Enfin, le transfert vers la pratique clinique de tests fonc-
tionnels de la réparation de l’ADN pourrait, dans le futur,
fournir des indications encore plus précises sur le statut
de chaque voie de réparation dans une tumeur. ■
1.
Lindahl T, Barnes DE. Repair of endogenous DNA damage.
Cold Spring Harbor Symp Quant Biol 2000;65:127-33.
2.
Jackson SP, Bartek J. The DNA-damage response in human
biology and disease. Nature 2009;461(7267):1071-8.
3. Hoeijmakers JH. Genome maintenance mechanisms for
preventing cancer. Nature 2001;411(6835):366-74.
4.
Bartkova J, Horejsí Z, Koed K et al. DNA damage response as
a candidate anti-cancer barrier in early human tumorigenesis.
Nature 2005;434(7035):864-70.
5.
Hecht SS. Tobacco smoke carcinogens and lung cancer.
J Natl Cancer Inst 1999;91(14):1194-210.
6. Olaussen KA, Dunant A, Fouret P et al. DNA repair by ERCC1
in non-small cell lung cancer and cisplatin-based adjuvant
chemotherapy. N Engl J Med 2006;355(10):983-91.
7. Jiang H, Yang LY. Cell cycle checkpoint abrogator UCN-01
inhibits DNA repair: association with attenuation of the inter-
action of XPA and ERCC1 nucleotide excision repair proteins.
Cancer Res 1999;59(18):4529-34.
8.
Jiang G, Li LT, Xin Y et al. Strategies to improve the killing of
tumors using temozolomide: targeting the DNA repair protein
MGMT. Curr Med Chem 2012;19(23):3886-92.
9.
Kamal NS, Soria JC, Mendiboure J et al. MutS homologue 2
and the long-term benefit of adjuvant chemotherapy in lung
cancer. Clin Cancer Res 2010;16(4):1206-15.
10. Martin SA, McCarthy A, Barber LJ et al. Methotrexate
induces oxidative DNA damage and is selectively lethal to
tumour cells with defects in the DNA mismatch repair gene
MSH2. EMBO Mol Med 2009;1(6-7):323-37.
11. Rosell R, Skrzypski M, Jassem E et al. BRCA1: a novel pro-
gnostic factor in resected non-small cell lung cancer. PloS
One 2007;2(11):e1129.
12. Bartolucci R, Wei J, Sanchez JJ et al. XPG mRNA expres-
sion levels modulate prognosis in resected non-small cell lung
cancer in conjunction with BRCA1 and ERCC1 expression. Clin
Lung Cancer 2009;10(1):47-52.
13.
Quinn JE, Kennedy RD, Mullan PB et al. BRCA1 functions as
a differential modulator of chemotherapy-induced apoptosis.
Cancer Res 2003;63(19):6221-8.
14.
Powell C, Mikropoulos C, Kaye SB et al. Pre-clinical and
clinical evaluation of PARP inhibitors as tumour-specific radio-
sensitisers. Cancer Treat Rev 2010;36(7):566-75.
15. Miknyoczki SJ, Jones-Bolin S, Pritchard S et al. Chemo poten-
tiation of temozolomide, irinotecan, and cisplatin activity by
CEP-6800, a poly(ADP-ribose) polymerase inhibitor. Mol Cancer
Ther 2003;2(4):371-82.
16.
Auckley DH, Crowell RE, Heaphy ER et al. Reduced DNA-
dependent protein kinase activity is associated with lung
cancer. Carcinogenesis 2001;22(5):723-7.
17. Eriksson A, Yachnin J, Lewensohn R, Nilsson A. DNA-
dependent protein kinase is inhibited by trifluoperazine.
Biochem Biophys Res Commun 2001;283(4):726-31.
18. Zheng Z, Chen T, Li X et al. DNA synthesis and repair genes
RRM1 and ERCC1 in lung cancer. N Engl J Med 2007;356(8):800-8.
19. Bergman AM, Eijk PP, Ruiz van Haperen VW et al. In vivo
induction of resistance to gemcitabine results in increased
expression of ribonucleotide reductase subunit M1 as the major
determinant. Cancer Res 2005;65(20):9510-6.
20. Ceppi P, Papotti M, Scagliotti G. New strategies for targeting
the therapy of NSCLC: the role of ERCC1 and TS. Adv Med Sci
2010;55(1):22-5.
21. Wang L, Wei J, Qian X et al. ERCC1 and BRCA1 mRNA
expression levels in metastatic malignant effusions is asso-
ciated with chemosensitivity to cisplatin and/or docetaxel.
BMC Cancer 2008;8:97.
22. Wang LE, Yin M, Dong Q et al. DNA repair capacity in
peripheral lymphocytes predicts survival of patients with non-
small cell lung cancer treated with first-line platinum-based
chemotherapy. J Clin Oncol 2011;29(31):4121-8.
Références
1
/
5
100%