29 Urgences chez un patient porteur d’un stimulateur cardiaque ences Médecins

Urgences chez un patient porteur
d’un stimulateur cardiaque
Introduction
Grâce à la microélectronique et à l’informatique embarquée, la technologie des
stimulateurs cardiaques a très largement évolué au cours des dix dernières années. Ils
sont souvent d’une grande aide dans le diagnostic et le traitement des troubles du
rythme et de la conduction mais leur complexité est parfois génératrice de diagnos-
tics de «faux dysfonctionnement », ce qui induit d’inutiles consultations. Leur inter-
prétation électrocardiographique nécessite d’avoir assimilé les principaux modes de
fonctionnement des stimulateurs cardiaques actuels.
Pour le médecin urgentiste, se pose au quotidien le problème de la prise en charge du
patient implanté en fonction des différents cadres nosologiques rencontrés. Si la
présence du stimulateur cardiaque est souvent déroutante pour le praticien, une
bonne connaissance de ce merveilleux outil peut parfois faciliter la prise en charge du
patient, y compris hors de l’hôpital.
1. Les différents modes de stimulation et la terminologie
1.1. Code international
Les indications à l’implantation d’un stimulateur cardiaque sont larges et variées. Il
en découle de nombreuses combinaisons de stimulation et d’écoute entre les diffé-
rentes cavités cardiaques (oreillettes et ventricules). Il existe donc un code interna-
tional (North American Society of Pacing and Electrophysiology et British Pacing and
Electrophysiology Group) qui permet de comprendre immédiatement le fonctionne-
ment global d’un stimulateur.
La première lettre désigne toujours le site de stimulation :
–ventricule (V) ;
–oreillette (A) ;
Conférences Médecins
391
Urgences chez un patient porteur d’un stimulateur cardiaque
URGENCES 2004
Chapitre 29
T. ZERAH
03_ConfMed_SFMU04_LC 15/03/04 15:39 Page 391

–les deux (D) ;
–aucun des deux (O).
Parfois S désigne soit le ventricule, soit l’oreillette : S pour single chamber/mono-
chambre.
La deuxième lettre désigne le site de détection selon le même code.
La troisième lettre désigne le mode de fonctionnement :
–inhibé (I) ;
–déclenché (T pour triggered);
–les deux (D) ;
–aucun des deux (O).
La quatrième lettre désigne la «programmabilité», la possibilité de télémétrie ou
d’asservissement de fréquence :
–O : non programmable ;
–P : jusqu’à deux fonctions programmables ;
–C : communication, possibilité de télémétrie ;
–M : multiprogrammable, avec trois fonctions ou plus (la plupart des stimulateurs
de dernière génération) ;
–R : asservissement de fréquence (augmentation de fréquence de stimulation à
partir des informations fournies par un capteur mesurant un paramètre lié à
l’effort).
Une cinquième lettre est utilisée pour les fonctions antitachycardiques :
–O : aucune ;
–P: pacing antitachyarythmique ;
–S : choc ;
–D : double (P et S).
Conférences Médecins
392
Troubles conductifs
URGENCES 2004
Tableau 1 – Code international des modes de fonctionnement d’un stimulateur
Lettre (n°) 1 2 3 4 5
Fonctions Site de Site de Mode de Programmabilité, Autres
stimulation détection fonctionnement télémétrie, fonctions
asservissement
de fréquence
Codes V : ventricule I : inhibéO : non programmable O : aucune
A : oreillette T : déclenché (trigger) P : jusqu’à deux fonctions P : pacing
D : A et V D : I et T programmables antitachya-
O : aucun des deux O : aucun des deux C : possibilité de télémétrie rythmique
M : multiprogrammable S : choc
S : parfois utilisé pour (≥3, fonctions)* D : double
«single chamber »R: fréquence asservie** (P et S)
(monochambre), désigne
le ventricule ou l’oreillette
M* : dans la plupart des stimulateurs de dernière génération.
R** : augmentation de la fréquence de stimulation à partir des informations fournies par un capteur mesurant
un paramètre lié à l’effort.
03_ConfMed_SFMU04_LC 15/03/04 15:39 Page 392

1.2. Modes de programmation le plus souvent rencontrés
Mode VOO : stimulation asynchrone du ventricule sans écoute.
Mode AOO : stimulation asynchrone de l’oreillette sans écoute.
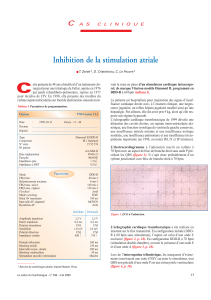
Mode VVI : stimulation du ventricule (monochambre) avec écoute : quand la
sonde ventriculaire du stimulateur cardiaque détecte une activité spontanée dans le
ventricule, il est inhibé, c’est-à-dire qu’il interrompt l’intervalle d’échappement en
cours et le recycle sur l’événement détecté. Si aucune activité n’a été détectée au
terme de cet intervalle, le stimulateur stimule le ventricule : l’intervalle d’échappe-
ment et l’intervalle de stimulation correspondent tous deux à l’intervalle à la
fréquence de base programmée (figure 1).
Mode AAI : stimulation monochambre mais atriale (figure 2).
Mode DDD (figure 3) : stimulation la plus physiologique car respectant la synchroni-
sation auriculoventriculaire. Le principe est de synchroniser la stimulation ventricu-
laire sur la détection atriale. De plus, s’il existe une activité atriale spontanée, elle
inhibe la stimulation atriale. Le même principe vaut pour le ventricule. De plus, la
relation entre les deux canaux (atrial et ventriculaire) est régie par le délai auriculo-
ventriculaire (DAV) dont la valeur est programmable. Chez un patient porteur d’un
stimulateur cardiaque double chambre, il est donc possible de constater quatre types
de tracés électrocardiographiques :
–onde P détectée dans l’oreillette et onde R détectée dans le ventricule avant la fin
du DAV programmé: tracé «normal » sans intervention du stimulateur cardiaque ;
–onde P non détectée dans l’oreillette et onde R non détectée dans le ventricule
avant la fin du DAV programmé: tracé comportant deux spikes de stimulation.
Le premier précède l’auriculogramme électroentraîné, le deuxième précède le
ventriculogramme électroentraîné;
–onde P détectée dans l’oreillette mais onde R non détectée dans le ventricule
avant la fin du DAV programmé: l’onde P «physiologique » est suivie, au terme
du DAV programmé, d’un spike suivi du ventriculogramme électroentraîné;
–onde P non détectée dans l’oreillette et onde R détectée dans le ventricule avant
la fin du DAV programmé: spike précédant l’auriculogramme électroentrainé
puis ventriculogramme spontané «physiologique ».
La programmation en mode DDD est la plus souvent rencontrée chez les patients
porteurs de stimulateurs cardiaques intracorporels.
Mode DDI : stimulation atriale et ventriculaire, détection atriale et ventriculaire, inhi-
bition par les événements atriaux et ventriculaires. C’est un mode de stimulation un
peu particulier mais qu’il faut connaître car il est souvent utilisé lors des commuta-
tions de mode des stimulateurs cardiaques pendant les passages en trouble du
rythme atrial. Lorsque la fréquence de stimulation programmée est supérieure à la
fréquence sinusale spontanée du patient, la stimulation est «double chambre », il y a
un spike devant l’auriculogramme, puis un spike devant le ventriculogramme.
Lorsque la fréquence sinusale spontanée du patient est supérieure à la fréquence
programmée, le stimulateur détecte une activité atriale et fonctionne comme s’il était
programmé en monochambre ventriculaire (VVI) : il y a une dissociation auriculo-
Conférences Médecins
393
Urgences chez un patient porteur d’un stimulateur cardiaque
URGENCES 2004
03_ConfMed_SFMU04_LC 15/03/04 15:39 Page 393

ventriculaire. Lors de la survenue d’un trouble du rythme atrial, un algorithme permet
au stimulateur de se commuter en DDI ce qui revient à stimuler le patient en VVI
(puisque des événements atriaux sont détectés) sans qu’il y ait une association d’un
ventriculogramme pour chaque auriculogramme détecté. On évite ainsi une tachy-
cardie induite par le trouble du rythme atrial.
Il existe, bien sûr, d’autres modes de stimulation mais ils sont bien moins souvent
rencontrés.
1.3. Algorithmes
À côté de ces différents modes de programmation, les constructeurs proposent
nombre de «petits algorithmes » dont la fonction et l’utilité varient d’un modèle à
l’autre. Leur méconnaissance peut conduire le praticien à poser un faux diagnostic de
dysfonctionnement.
L’hystérésis de fréquence : hystérésis vient du grec «hysterein » (qui vient plus tard).
C’est un intervalle ajouté à l’intervalle de stimulation déclenché sur un événement
spontané. En pratique, cela signifie que la fréquence à partir de laquelle le stimulateur
induit sa stimulation est plus basse que la fréquence de base programmée. Cela a
théoriquement pour intérêt de moins stimuler le patient (figure 4).
L’hystérésis du DAV : même principe appliqué au délai auriculoventriculaire. Cela
permet d’éviter une stimulation ventriculaire lorsque le DAV spontané est proche du
DAV programmé (figure 5).
Fréquence de nuit : la fréquence de stimulation programmée (par exemple 60 bpm)
est automatiquement réduite (par exemple 50 bpm) la nuit. Soit les horaires sont
programmés (début et fin), soit ils sont corrélés au capteur d’asservissement. Le but
est de respecter la bradycardie physiologique nocturne.
Capteur d’asservissement : lorsque le sinus d’un patient ne s’accélère pas suffisam-
ment lors d’un effort (dysfonction sinusale) il est possible, par la mise en route du
capteur d’asservissement, d’augmenter artificiellement la fréquence de stimulation
suivant une pente plus ou moins définie par le stimuliste. De nombreux capteurs sont
proposés par les constructeurs.
Période réfractaire atriale postventriculaire : intervalle dont la durée est program-
mable après la stimulation ventriculaire qui évite au stimulateur de détecter un
événement atrial (onde P rétrograde par exemple) et d’y synchroniser la stimulation
ventriculaire.
Détection unipolaire ou bipolaire : sur une sonde unipolaire, la détection se fait
entre la distalité de la sonde et le boîtier, alors qu’avec une sonde bipolaire la détec-
tion se fait entre la distalité de la sonde et une électrode située un peu plus haut sur la
sonde. La détection avec une sonde unipolaire est donc moins sensible et moins
spécifique que sur une sonde bipolaire car le champ balayé est alors plus grand. Il
peut survenir des détections «parasites » tels des myopotentiels pectorals, ou au
contraire des sous-détections, notamment auriculaires, du fait de l’existence de
«bruit de fond » qui masque un faible potentiel atrial. Les sondes unipolaires sont
Conférences Médecins
394
Troubles conductifs
URGENCES 2004
03_ConfMed_SFMU04_LC 15/03/04 15:39 Page 394

pour l’instant plus fines que les sondes bipolaires, elles sont aussi moins fragiles. Pour
des raisons d’abord vasculaire, certaines équipes préfèrent utiliser des sondes unipo-
laires dans le ventricule afin d’éviter de ponctionner une veine sous-clavière car les
sous-détections y sont beaucoup moins fréquentes. En ce qui concerne les oreillettes,
les sondes bipolaires sont de loin les plus implantées.
Stimulation unipolaire et bipolaire : le principal intérêt de la stimulation bipolaire
est de concentrer le champ d’énergie sur le dipôle intracavitaire, et donc d’éviter des
contractions musculaires parfois invalidantes. Le principal inconvénient est de rendre
moins visible les spikes de stimulation sur l’électrocardiogramme de surface, ce qui
est générateur de consultations inutiles. Pour cette raison, la plupart des centres
programment la stimulation sur le mode unipolaire, et ce même en présence de
sondes bipolaires, la stimulation bipolaire pouvant être programmée en cas de
contractions musculaires.
Algorithmes de prévention de la fibrillation atriale : sur les stimulateurs cardiaques
de nouvelle génération, il est possible de programmer un algorithme qui permet de
prévenir la survenue d’une fibrillation atriale en stimulant le patient transitoirement à
une fréquence supérieure à sa fréquence de base (technique de l’overdrive).
2. Les véritables dysfonctionnements du stimulateur cardiaque
2.1. Perte de capture
La perte de capture correspond à une incapacité pour le stimulateur d’obtenir une
contraction myocardique après la délivrance du courant électrique. Il est à différen-
cier de l’inhibition de la stimulation qui est la non-délivrance du courant électrique
par le générateur.
La perte de capture peut être précoce après l’implantation et correspond le plus
souvent soit à un déplacement des sondes, soit à une augmentation du seuil de stimu-
lation. Le tableau clinique est souvent identique à celui ayant motivé la mise en place
du stimulateur cardiaque (syncope ou lipothymie, insuffisance cardiaque,
asthénie…). Le déplacement de sonde est une urgence vitale chez un patient stimulo-
dépendant. Il doit être dépisté et traité rapidement. Il se caractérise par la perte cons-
tante ou intermittente (si la sonde est dite «flottante ») de la capture myocardique,
même à haute énergie. Le diagnostic est posé par l’électrocardiogramme de surface.
Lorsque le patient présente un rythme spontané sans intervention du stimulateur
cardiaque, l’application de l’aimant sur le boîtier permet le fonctionnement sur un
mode asynchrone (VOO, AOO ou DOO) qui dévoile le défaut permanent ou inter-
mittent de stimulation (figure 6).
Si le défaut de capture ventriculaire est facile à voir, il peut être moins évident sur la
sonde atriale lorsque la stimulation est permanente en DDD car l’auriculogramme
électrostimulé est de faible amplitude (figure 7).
Conférences Médecins
395
Urgences chez un patient porteur d’un stimulateur cardiaque
URGENCES 2004
03_ConfMed_SFMU04_LC 15/03/04 15:39 Page 395
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%