Nouvelles perspectives de la chirurgie bariatrique ? Nouvelles réfl exions sur l’obésité

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVII - n° 6 - juin 2013
169169
dossier thématique
do
do
do
do
o
ssss
ss
s
s
s
s
ie
i
ie
i
r
r
r
r
r
r
th
th
t
th
th
ém
ém
ém
ém
ém
m
m
ém
at
a
at
at
t
a
iq
i
iq
q
q
q
ue
ue
ue
e
ue
e
e
e
e
e
e
e
e
Nouvelles réfl exions
sur l’obésité
et ses complications
Nouvelles perspectives
de la chirurgie bariatrique ?
New perspectives in bariatric surgery?
Sabrina Chiheb*, Camille Cussac-Pillegand*
* Service d’endo-
crinologie, diabétologie,
nutrition, hôpital Jean-
Verdier (AP-HP), centre
de recherche en nutrition
humaine (CRNH) d’Île-de-
France, centre intégré
nord-francilien de prise
en charge de l’obésité
(CINFO), Bondy.
points forts
Highlights
»
La prise alimentaire et, donc, le poids sont contrôlés en partie
par les hormones digestives.
»
Après une chirurgie bariatrique, les améliorations très rapides
de l’équilibre glycémique chez le diabétique suggèrent un rôle
propre des hormones digestives.
»
Les modifi cations des hormones digestives ne sont pas toujours
corrélées à l’importance de la perte de poids et évoluent
diff éremment selon la technique chirurgicale employée.
»
La gastrectomie longitudinale, ou sleeve gastrectomy, est aussi
une chirurgie endocrinienne.
Mots-clés : Chirurgie bariatrique – Chirurgie métabolique – Hormones
digestives.
Food intake and, therefore, weight, are partly under gut
hormones control.
The improvement of glycemic control in diabetic patients
after bariatric surgery suggest that gut hormones may have
their own metabolic role.
Changes in gut hormones are not always correlated with
the importance of weight loss and may diff er according to
the type of bariatric surgery.
Sleeve gastrectomy may now also be considered as an
endocrine surgery
Keywords: Bariatric surgery – Metabolic surgery – Gut
hormones.
L
a chirurgie bariatrique, quand son indication
est validée (1), repose soit sur des techniques
restrictives visant à diminuer la capacité gastrique
(gastroplastie par anneau ajustable, gastrectomie lon-
gitudinale en manchon, ou sleeve gastrectomy), soit sur
des techniques mixtes, restrictives et malabsorptives.
Ces dernières ne réduisent pas seulement la capacité
gastrique, mais entraînent également une malabsorp-
tion du bol alimentaire. La technique la plus fréquem-
ment réalisée est le court-circuit gastrique, ou gastric
bypass.
La chirurgie de l’obésité fournit des résultats probants
en termes de perte de poids et de sa stabilisation.
La qualité de vie et les comorbidités se trouvent
améliorées significativement, en particulier pour
l’hypertriglycéridémie, l’équilibre glycémique chez
les diabétiques, les niveaux tensionnels et l’hyper-
uricémie (1, 2).
La perte pondérale après la chirurgie est supérieure
à celle obtenue avec les mesures médicales seules.
Elle est également plus précoce : il suffi ra de 30 jours
à un patient obèse pour perdre 10 kg là où il en
faudrait 55 en cas de restriction calorique, même
sévère (1 000 kcal/j) [3]. Un court-circuit gastrique
entraîne souvent une amélioration, voire une rémis-
sion rapide du diabète, avant même la perte de poids.
Cela suggère l’implication d’autres facteurs que ceux
liés à la seule restriction calorique ou à la malabsorp-
tion (4). La sécrétion des hormones produites le long
du tube digestif et dont le “circuit” est modifi é par les
diff érents montages chirurgicaux pourrait y participer
à la fois au niveau central (eff ets sur la satiété) et au
niveau périphérique (eff ets à la fois sur la satiété et
sur le métabolisme).
Les hormones qui nous intéressent sont sécrétées par
les cellules fundiques de l’estomac pour la ghréline, par
les cellules I duodénales pour la cholécystokinine (CKK),
par les cellules L pour le peptide YY (PYY), l’oxyntomo-
duline (OXM) et le GLP-1 (Glucagon-Like Peptide 1) ; et
par les cellules K du duodénum et du jéjunum pour le
GIP (Gastric Inhibitory Peptide, ou Glucagon-dependent
Insulinotropic Peptide). Nous parlerons en outre de 2
des principales adipokines : la leptine et l’adiponectine
(fi gure, A et B, p. 170).

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVII - n° 6 - juin 2013
170170
dossier thématique
do
do
d
d
d
d
do
d
d
d
o
d
d
d
d
d
d
d
s
ss
s
s
s
s
ss
ss
ss
s
s
ss
ie
e
ie
e
r
r
th
th
th
th
th
é
ém
m
ém
m
é
ém
é
at
at
a
at
t
t
iqiq
q
q
q
i
i
ue
ue
ue
ue
u
Nouvelles réfl exions
sur l’obésité
et ses complications
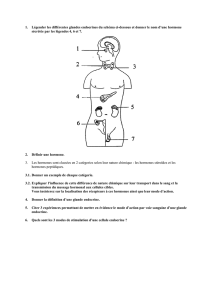
Figure. A. Action centrale des hormones digestives. B. Action périphérique des hormones
digestives.
NA : noyau arqué ;
NPV : noyaux paraventri-
culaires ; TA : tissu adipeux.
NA : noyau arqué ;
NPV : noyaux paraventri-
culaires ; TA : tissu adipeux.
A
B
Le rôle des hormones digestives
La ghréline
Peptide de 28 acides aminés principalement produit par
les cellules X/A de l’estomac, la ghréline est présente à
des taux non négligeables le long du tube digestif (5) et
au niveau de l’hypothalamus. L’acylation de la ghréline
est nécessaire à sa fi xation sur son récepteur, et donc à
ses eff ets biologiques. Il s’agit d’une hormone oréxigène
(fi gure, A) et lipogénique. La demi-vie plasmatique de
l’hormone active est comprise entre 5 et 30 mn, ce
qui rendait dans le passé son dosage diffi cile, mais les
méthodes ont été améliorées. La sécrétion de la ghré-
line est sous la dépendance complexe de nombreux
facteurs neuroendocriniens.
La sécrétion de la ghréline est rythmée par les repas. Elle
intervient dans l’homéostasie énergétique. Les concen-
trations de ghréline doublent avant les repas, stimulant
la prise alimentaire, et diminuent de manière signifi ca-
tive dans l’heure qui suit. Cette diminution est liée non
seulement à la distension gastrique mais également à
la présence d’aliments caloriques dans l’estomac (6, 7).
La concentration plasmatique de ghréline dépend des
réserves énergétiques : on a montré une corrélation
inverse entre les taux de ghréline circulante, l’indice de
masse corporelle (IMC) et la taille des adipocytes (8).
On observe en outre que les taux de ghréline à jeun
sont plus bas et leur diminution postprandiale, plus
prononcée, chez les sujets obèses que chez les sujets
dont l’IMC est normal (9).
On comprend que toute procédure chirurgicale visant
la réduction de la poche gastrique ou l’exclusion d’une
partie de l’intestin puisse avoir une incidence sur la
sécrétion de ghréline. La majorité des études ont mon-
tré que les taux de ghréline après la réalisation d’un
court-circuit gastrique étaient diminués (10), parfois
fortement (11), tant à jeun qu’en période postpran-
diale, avec cependant des données contradictoires :
augmentation dans une étude (12), stabilité dans une
autre (9). La gastroplastie par anneau modulable tend
à réduire la ghréline circulante postprandiale à des
taux comparables à ceux observés après la réalisation
d’un court-circuit gastrique, alors que, à jeun, les taux
sont augmentés (13). La perte de poids dans le cas
de l’anneau gastrique ne s’explique donc pas par un
eff et de la ghréline. Dans une étude prospective en
double aveugle comparant les eff ets de la gastrecto-
mie longitudinale et du court-circuit gastrique (14),
S.N. Karamanakos et al. ont montré qu’après la gas-
trectomie longitudinale, par laquelle une grande partie
de l’estomac est amputée, la ghréline circulante est
signifi cativement diminuée à jeun et après les repas,
avec une réduction drastique de l’appétit par rapport
à ce qui est observé dans le cas du court-circuit gas-
trique (tableau).
La plupart des études tendent donc à souligner le rôle
joué par la suppression de la ghréline dans la perte de
poids après la réalisation d’un court-circuit gastrique
ou d’une gastrectomie longitudinale. Cependant, la
perte de poids à long terme dépend également d’autres
hormones digestives (15).
Le peptide YY
Le PYY est sécrété en période postprandiale par les
cellules L de l’intestin proportionnellement à la den-
sité calorique des aliments (fi gure, A et B). Sa sécrétion
n’est pas modifi ée par la distension gastrique (16), et

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVII - n° 6 - juin 2013
171171
Nouvelles perspectives de la chirurgie bariatrique ?
le PYY3-36, composé de 36 acides aminés, en est la
principale forme circulante. Le PYY inhibe les sécrétions
gastriques, pancréatiques et intestinales et réduit la
motilité gastro-intestinale (15). Il exerce son eff et satié-
togène directement au niveau de l’hypothalamus via
le récepteur NPY Y2R.
Dans une étude qui avait inclus 4 groupes de femmes :
femmes normopondérales, femmes ayant subi une
gastroplastie, femmes ayant bénéficié d’un court-
circuit gastrique et témoins non opérés obèses, les
taux de PYY total et de PYY3-36, bien que compa-
rables à jeun, étaient 2 à 4 fois plus élevés durant la
période postprandiale chez les sujets ayant bénéficié
d’un court-circuit gastrique. La perte de poids plus
importante après la réalisation d’un court-circuit
gastrique qu’après la pose d’un anneau gastrique
s’explique en partie par une satiété plus précoce après
les repas, ce qui suggère un rôle du PYY (17). Dans
une autre étude menée en double aveugle, les taux
circulants de PYY à jeun ou durant la période post-
prandiale étaient similaires après une gastrectomie
longitudinale et après la réalisation d’un court-circuit
gastrique (tableau) [14].
A. Bartolome et al. ont étudié, dans une étude pros-
pective, les variations des taux de PYY et de GLP-1
en réponse à un repas test standard chez 9 sujets
obèses normoglycémiques. Avant la réalisation d’un
court-circuit gastrique, la sécrétion des 2 peptides ne
variait pas après le repas test. Six semaines après la
chirurgie, alors que les patients étaient encore obèses,
les taux de PYY et de GLP-1 s’élevaient signifi cative-
ment durant la période postprandiale. Parallèlement,
la sensation de satiété était élevée, et la sensation
de faim avait diminué signifi cativement. Il n’y avait
cependant pas de corrélation entre la variation des
hormones digestives et le comportement alimen-
taire (18).
Le GLP-1
Peptide de 30 acides aminés, le GLP-1 est une hormone
insulinotropique glucodépendante. Le GLP-1 est sécrété
par les cellules L intestinales, comme le PYY et l’OXM.
Ces peptides ont une synergie anorexigène postpran-
diale (fi gure A).
Le GLP-1 entraîne un ralentissement de la vidange gas-
trique, stimule la satiété et inhibe la sécrétion du glu-
cagon (19-21). Dans les modèles animaux diabétiques
et non diabétiques, le GLP-1 stimule la prolifération et
la diff érenciation des cellules β pancréatiques (22). La
demi-vie plasmatique du peptide dans les conditions
physiologiques est courte, d’environ 2 minutes, à cause
de l’action des dipeptidyl peptidases de type IV (DPP4).
La majorité des études ont montré que, chez les sujets
ayant bénéfi cié d’un court-circuit gastrique, les taux de
GLP-1 s’élevaient dans la période postprandiale (23).
Lors de la gastrectomie longitudinale, on observe les
mêmes variations. C’est l’augmentation de la vidange
gastrique, entraînant une interaction plus précoce du
bol alimentaire avec les cellules intestinales, qui expli-
querait cet eff et (24, 25). Cela explique que l’anneau
gastrique n’entraîne pas de variation de la sécrétion
du GLP-1 (tableau) [26]. L’eff et incrétine sur l’insuline
du GLP-1 pourrait bien expliquer l’amélioration des
glycémies chez les patients diabétiques ayant bénéfi cié
d’un court-circuit gastrique avant même une perte de
poids signifi cative (18, 27).
L’oxyntomoduline (OXM)
C’est un peptide de 37 acides aminés ayant en commun
29 acides aminés avec le glucagon, autre produit du
gène du proglucagon. Il agit via le récepteur du GLP-
1, et son action semble en partie similaire. Libéré par
les cellules L de l’intestin distal en réponse à une prise
alimentaire afi n d’obtenir un sentiment de satiété, il
prolonge la vidange gastrique, inhibe les sécrétions
Tableau. Eff et de la chirurgie bariatrique sur les hormones digestives (43).
Eff et hypothalamique
sur la satiété Taux plasmatiques
après bypass
Taux plasmatiques
après gastrectomie
longitudinale
Taux plasmatiques
après anneau gastrique
Ghréline Orexigène
PYY Anorexigène =
GLP-1 Anorexigène =
OXM Anorexigène ??
GIP Pas d’eff et ??
CKK Anorexigène =?

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVII - n° 6 - juin 2013
172172
dossier thématique
do
do
d
d
d
d
do
d
d
d
o
d
d
d
d
d
d
d
s
ss
s
s
s
s
ss
ss
ss
s
s
ss
ie
e
ie
e
r
r
th
th
th
th
th
é
ém
m
ém
m
é
ém
é
at
at
a
at
t
t
iqiq
q
q
q
i
i
ue
ue
ue
ue
u
Nouvelles réfl exions
sur l’obésité
et ses complications
acides gastriques et diminue la fonction exocrine du
pancréas. L’OXM est rapidement dégradée par la DPP4.
Seules des perfusions intraveineuses d’OXM à des doses
supra-physiologiques peuvent induire chez l’homme
un amaigrissement, réduisant l’IMC et augmentant la
satiété et la dépense énergétique au repos (28).
Récemment a été mis en évidence un doublement de la
sécrétion d’OXM après une charge en glucose réalisée
dans les suites d’un court-circuit gastrique versus un
amaigrissement obtenu par traitement médical. Ce pic
d’OXM était fortement corrélé à celui du GLP-1 et du
PYY, mais semblait indépendant des modifi cations de
l’insulinémie. Cela suggère un eff et indirect de l’OXM
sur l’équilibre diabétique après la réalisation d’un court-
circuit gastrique. Cette conjonction des 3 hormones
pourrait expliquer la perte de poids et la meilleure
amélioration du diabète de type 2 après la réalisation
d’un court-circuit gastrique (29).
La cholécystokinine (CCK)
C’est la première hormone digestive découverte ; elle
est impliquée dans la régulation de l’appétit. Elle est
sécrétée durant la période postprandiale par les cellules
L du duodénum (fi gure, A). Sa structure est similaire
à celle de la gastrine et elle a pour précurseur la pré-
procholécystokinine. Sa demi-vie plasmatique est très
courte, de l’ordre de quelques minutes ; elle est sécrétée
au maximum 15 mn après le début de la prise alimen-
taire. Elle stimule les sécrétions pancréatiques, améliore
la motilité intestinale et retarde la vidange gastrique.
Des récepteurs de CCK sont présents au niveau hypo-
thalamique, et une partie de son action semble liée à
une modifi cation de la balance vagosympathique via
l’activation du nerf vague. D’autres neurotransmetteurs
sont probablement mis en jeu, comme la sérotonine
et la noradrénaline.
La réponse de la CKK après un repas est augmentée
après une chirurgie bariatrique, et de façon plus mar-
quée en cas de gastrectomie longitudinale qu’en cas de
court-circuit gastrique (30, 31). Ces modifi cations sont
retrouvées aussi en cas de ballon intragastrique (32) ;
nous ne disposons pas d’étude après une gastroplastie.
Le GIP
Il s’agit d’un peptide de 42 acides aminés produit par
les cellules K du duodénum et du jéjunum (fi gure, A). Sa
demi-vie plasmatique est de 7 minutes. Le GIP est égale-
ment dégradé par les DPP4. Tout comme le GLP-1, le GIP
est sécrété durant la période postprandiale et a un eff et
incrétine vis-à-vis de l’insuline. Il inhibe, mais de façon
négligeable, les sécrétions gastriques et a les mêmes
eff ets sur les cellules β pancréatiques que le GLP-1 (20,
23, 33). Le GIP stimule la prolifération des ostéoblastes
et inhibe leur apoptose (20). Le GIP a des eff ets anabo-
lisants via son action directe sur l’adipocyte (fi gure, B).
Les souris invalidées pour le récepteur du GIP ou pour
les cellules K sont protégées de l’obésité lorsqu’elles
sont soumises à un régime hyperlipidique (23).
Chez les sujets obèses et les diabétiques, le GIP contri-
bue à l’insulinorésistance. On trouve des taux plus élevés
à l’état basal et après stimulation chez les intolérants
au glucose que chez les sujets normopondéraux (34).
Une étude a évalué l’eff et du court-circuit gastrique sur
les hormones digestives et le métabolisme glucidique
chez 10 patients obèses (IMC entre 40 et 53 kg/m2),
dont 6 étaient diabétiques sous antidiabétiques oraux.
Trois semaines après la chirurgie, les taux de GIP à jeun
étaient signifi cativement réduits chez les diabétiques
mais restaient inchangés en l’absence de diabète (35).
Dans une autre étude évaluant plus tardivement (après
24,6 ± 2,0 mois) l’eff et du court-circuit gastrique et de
la gastroplastie, le taux de GIP était diminué signifi ca-
tivement en cas de court-circuit gastrique par rapport
aux témoins obèses non opérés, même chez des sujets
non diabétiques. Il n’y avait pas de corrélation entre le
taux de GIP et le taux d’insuline (18). Actuellement, on
ne dispose pas de données suffi santes quant à l’eff et
de la gastrectomie longitudinale sur le GIP.
Les adipokines
Les adipokines jouent un rôle important dans les régu-
lations pondérales et métaboliques, interagissant avec
les hormones digestives. C’est pourquoi nous avons
voulu compléter notre revue en examinant leurs eff ets
potentiels propres (fi gure, A et B) et leur évolution après
chaque type de chirurgie bariatrique.
La leptine
La leptine est un peptide de 146 acides aminés sécrété
par le tissu adipeux. Elle régule la sensation de faim en
agissant directement au niveau des noyaux arqués.
Elle augmente la captation musculaire du glucose,
l’oxydation des acides gras et diminue la synthèse
hépatique de glucose et la synthèse d’insuline par les
cellules β pancréatiques. La leptine a d’autres eff ets non
métaboliques : elle interagit avec la biologie osseuse,
le système immunitaire, l’angiogenèse et la fonction
gonadotrope (36, 37). La leptine inhibe la production
de PYY. Une augmentation de la leptine provoquée
par une augmentation de la masse grasse devrait donc
permettre de limiter la prise de poids. Cependant, des
taux très élevés de leptine, proportionnels à la masse

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVII - n° 6 - juin 2013
173173
Nouvelles perspectives de la chirurgie bariatrique ?
grasse, sont observés chez les patients obèses sans leur
permettre de moduler leur appétit. Cette leptinorésis-
tance n’est pas clairement expliquée.
Après amaigrissement, et ce quelle que soit la technique
médicale ou chirurgicale utilisée, la leptinémie diminue.
Cette diminution est corrélée au poids, à l’IMC et à la
masse grasse. Cet eff et n’est pas spécifi que à la chirurgie
bariatrique mais est lié à l’amaigrissement ; la diff érence
observée entre les techniques chirurgicales ne semble
pas liée à leur qualité intrinsèque mais à l’importance
de l’amaigrissement. Ainsi, la diminution de la leptine
est la même après un amaigrissement obtenu par une
prise en charge médicale, une gastrectomie longitudi-
nale ou un “switch” duodénal, bien qu’elle ne soit pas
signifi cative dans cette étude (38).
L’adiponectine
L’adiponectine est un peptide de 244 acides aminés. C’est
l’adipokine sécrétée par le tissu adipeux dont la concen-
tration plasmatique est la plus élevée. Une diminution
des taux d’adiponectine est décrite chez les patients
obèses et, de façon encore plus importante, chez les
patients diabétiques. Cette diminution est probable-
ment liée à un eff et direct de l’insuline sur la production
d’adiponectine, mécanisme non sensible à l’insulinorésis-
tance. L’adiponectine régule la sensibilité à l’insuline en
augmentant l’oxydation des acides gras, en particulier au
niveau des muscles squelettiques et hépatique, stimulant
la captation du glucose et réduisant la néoglucogenèse
hépatique. Certaines études réalisées dans des popula-
tions spécifi ques (Indiens Pimas, Japonais et Coréens)
ont démontré que les taux d’adiponectine permettaient
de prédire le risque de diabète de type 2.
Une augmentation de l’adiponectinémie est observée
en cas d’amaigrissement, et cette augmentation est
corrélée à une amélioration de l’insulinosensibilité. Elle
est moins bonne en cas de diabète de type 2. Après
une chirurgie, une augmentation des taux circulants
d’adiponectine est observée, et cela de façon plus
importante chez les patients non diabétiques que chez
les patients diabétiques (qui cependant présentent
déjà des taux plus élevés d’adiponectine plasmatique
en préopératoire) [39]. Cette amélioration semble liée
à la perte de poids plutôt qu’à la technique chirur-
gicale employée ; elle est progressive, parallèle à la
variation de poids et à l’amélioration de l’insulino-
sensibilité (40, 41).
Conclusion
La perte de poids après une chirurgie bariatrique ne
semble pas seulement liée à la restriction calorique ou
à la malabsorption. Les diff érentes techniques chirur-
gicales, tant restrictives pures que mixtes, entraînent
des modifi cations des hormones digestives dont les
eff ets synergiques concourent à la perte de poids et
aux améliorations métaboliques observées, parfois
avant une perte pondérale signifi cative. Ces consta-
tations conduisent à considérer la chirurgie de l’obé-
sité non plus comme une simple chirurgie bariatrique
mais également comme une chirurgie métabolique
et hormonale.
Il semble, en outre, que les hormones digestives et les
adipokines jouent un rôle dans la reprise de poids après
la chirurgie bariatrique. Par exemple, dans un modèle
animal, il apparaît que les rats incapables de maintenir
un ratio PYY/leptine élevé peinent à conserver leur
perte de poids dans le temps après la réalisation d’un
court-circuit gastrique (42). ■
1. Poghosyan T, Polliand C, Bernard K et al. [Comparison of qua-
lity of life in morbidly obese patients and healthy volunteers. A
prospective study using the GIQLI questionnaire]. J Chir (Paris)
2007;144(2):129-33; discussion 134.
2.
Sjostrom L, Lindroos AK, Peltonen M et al. Lifestyle, diabetes,
and cardiovascular risk factors 10 years after bariatric surgery.
N Engl J Med 2004;351(26):2683-93.
3.
Olivan B, Teixeira J, Bose M et al. Eff ect of weight loss by
diet or gastric bypass surgery on peptide YY3-36 levels. Ann
Surg 2009;249(6):948-53.
4. Odstrcil EA, Martinez JG, Santa Ana CA et al. The contribu-
tion of malabsorption to the reduction in net energy absorp-
tion after long-limb Roux-en-Y gastric bypass. Am J Clin Nutr
2010;92(4):704-13.
5. Date Y, Kojima M, Hosoda H et al. Ghrelin, a novel growth
hormone-releasing acylated peptide, is synthesized in a distinct
endocrine cell type in the gastrointestinal tracts of rats and
humans. Endocrinology 2000;141(11):4255-61.
6.
Tschop M, Smiley DL, Heiman ML. Ghrelin induces adiposity
in rodents. Nature 2000;407(6806):908-13.
7.
Cummings DE, Purnell JQ, Frayo RS et al. A preprandial rise
in plasma ghrelin levels suggests a role in meal initiation in
humans. Diabetes 2001;50(8):1714-9.
8. Tschop M, Weyer C, Tataranni PA et al. Circulating ghrelin
levels are decreased in human obesity. Diabetes 2001;50(4):
707-9.
9. Le Roux CW, Welbourn R, Werling M et al. Gut hormones as
mediators of appetite and weight loss after Roux-en-Y gastric
bypass. Ann Surg 2007;246(5):780-5.
10.
Geloneze B, Tambascia MA, Pilla VF et al. Ghrelin: a gut-
brain hormone: eff ect of gastric bypass surgery. Obes Surg
2003;13(1):17-22.
11. Cummings DE, Weigle DS, Frayo RS et al. Plasma ghrelin
levels after diet-induced weight loss or gastric bypass surgery.
N Engl J Med 2002;346(21):1623-30.
12.
Vendrell J, Broch M, Vilarrasa N et al. Resistin, adiponectin,
ghrelin, leptin, and proinfl ammatory cytokines: relationships
in obesity. Obes Res 2004;12(6):962-71.
13. Schindler K, Prager G, Ballaban T et al. Impact of laparo-
scopic adjustable gastric banding on plasma ghrelin, eating
behaviour and body weight. Eur J Clin Invest 2004;34(8):549-54.
14.
Karamanakos SN, Vagenas K, Kalfarentzos F et al. Weight
loss, appetite suppression, and changes in fasting and post-
prandial ghrelin and peptide-YY levels after Roux-en-Y gastric
bypass and sleeve gastrectomy: a prospective, double blind
study. Ann Surg 2008;247(3):401-7.
15. Pournaras DJ, Le Roux CW. The eff ect of bariatric surgery
on gut hormones that alter appetite. Diabetes Metab 2009;35(6
Pt 2):508-12.
Références
Les auteurs déclarent
ne pas avoir
de liens d’intérêts.
>>>
 6
6
1
/
6
100%