Lire l'article complet

DOSSIER
tmiqu
Le Courrier de la Transplantation - Volume VII - n
o 2 - avril-mai-juin 2007
67
Coordinateur : J.C. Chachques,
service de chirurgie cardiovasculaire
et laboratoire d’étude des greff es
et prothèses cardiaques, hôpital
européen Georges-Pompidou
et hôpital Broussais, Paris.
Médecine
régénératrice
Facteurs de croissance
et thérapie cellulaire chez les brûlés
et autres pathologies dermatologiques
G. Zakine*●
* Service de chirurgie plastique reconstructrice et
esthé tique, centre des brûlés, hôpital Rothschild,
Paris ; clinique Geoffroy-Saint-Hilaire, Paris.
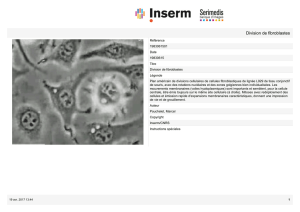
Les différents stades de la cicatri-
sation cutanée mettent en jeu de
nombreux facteurs de croissance,
polypeptides stimulant la proliféra-
tion, la migration et la différenciation
cellulaires (1-3). Ces stades font partie,
avec les cytokines qui sont de petites
protéines médiatrices dans l’immunité
et la réparation tissulaires, du groupe
des polypeptides régulateurs sécrétés
par de nombreuses lignées cellulaires.
Leurs rôles sont fondamentaux dans
la cicatrisation tissulaire (4-6), l’onto-
genèse, la cancérogenèse et dans la
régulation de l’équilibre entre le renou-
veau et la mort cellulaire (apoptose).
Se liant à des récepteurs membranaires
spécifiques qui sont alors phospho-
rylés, ils entraînent l’activation d’en-
zymes intracellulaires qui déclenche
une cascade de réactions conduisant
à l’activation de gènes permettant une
synthèse protéique ou préparant la
cellule à la mitose (c’est-à-dire stimu-
lant la multiplication cellulaire). Après
lésion cutanée, plusieurs facteurs de
croissance sont produits ; ils participent
au processus in ammatoire, permet-
tent la lutte contre la contamination
bactérienne, déclenchent et contrôlent
la réparation cutanée. Chaque facteur a
une ou des action(s) sur un ou plusieurs
type(s) cellulaire(s), et tous ces facteurs
sont dépistés à différentes concentra-
tions durant les différentes phases de
la cicatrisation (7, 8). Par ailleurs,
l’équilibre entre les divers facteurs de
croissance présents durant la cicatri-
sation n’est pas le même chez l’adulte
et le fœtus chez lequel (et cela est vrai
pour tous les fœtus de mammifères) la
régénération tissulaire se réalise sans
cicatrice (9).
Facteurs de croissance et thérapie cellulaire chez les brûlés
et autres pathologies dermatologiques – G. Zakine
La thérapie cellulaire comme traitement de l’incontinence urinaire
P. Sèbe, F. Haab, C. Pinset (page 75)
Régénération du myocarde par cardiomyoplastie cellulaire
M. Cortes-Morichetti, D. Mika, E. Chachques (page 77)
Thérapie cellulaire chez des patients atteints de diabète
R.J. Fernandez Vina, O. Andrin, J. Saslavsky, F. Vrsalovic, L. Camozzi,
O. Ferreyra, A. Classen, J. Ferreyra da Silva Lima, C.D. Adamo, R.F. Fernandez Vina,
F. Foressi, N. Muttis (page 86)
Thérapie cellulaire de l’ischémie critique des membres inférieurs
J. Emmerich, D. Smadja, P. Gaussem (page 90)
●
●
●
●
●

DOSSIER
tmiqu
Le Courrier de la Transplantation - Volume VII - n
o 2 - avril-mai-juin 2007
68
La peau, totalisant environ 15 % du
poids corporel pour 1,5 à 2 m
2
, assure
des fonctions de protection, de sensa-
tion, de thermorégulation et de méta-
bolisme. Elle est constituée de trois
couches : l’épiderme, composé d’un
épithélium strati é et kératinisé formé
de cinq couches distinctes et de 95 %
de kératinocytes, assurant la protection
et étant en contact avec l’extérieur ;
le derme, séparé de l’épiderme par la
membrane basale et composé du derme
papillaire super ciel et du derme réticu-
laire profond ; l’hypoderme, constitué
de tissu adipeux. Derme et hypoderme
contiennent des terminaisons nerveuses,
des annexes (glandes sébacées, glandes
sudoripares et follicules pileux) et de
nombreux vaisseaux sanguins.
La brûlure, le plus souvent thermique,
est une destruction plus ou moins
profonde de la peau. Cette dernière
cicatrise à partir de la couche basale,
si elle a été épargnée, et des annexes qui
contiennent des kératinocytes permet-
tant la régénération de l’épiderme. Le
derme, s’il est atteint, cicatrise en se
remodelant sur plusieurs mois. Plus
la brûlure est profonde et plus la cica-
trisation est longue, voire impossible
spontanément en cas de destruction
étendue en profondeur et en surface,
ce qui nécessite alors des excisions-
greffes cutanées. Accélérer et améliorer
la cicatrisation cutanée permettrait de
diminuer la morbidité et la mortalité,
d’écourter les douleurs et de réduire la
durée d’hospitalisation.
Des facteurs de croissance et des cyto-
kines interviennent lors de chacune des
phases de la réparation tissulaire après
brûlure ou autre lésion cutanée. Ces
phases sont l’in ammation, la déter-
sion, la prolifération (bourgeonnement
et épidermisation) et le remodelage.
La cicatrisation après lésion cutanée,
obtenue par reconstitution du derme et
de l’épiderme, est sous le contrôle des
nombreux facteurs de croissance dont
les FGF-2, KGF-1 et 2, VEGF, PDGF,
TGFβ, EGF et IGF-1.
FACTEURS DE CROISSANCE
ET BRÛLURE
Le FGF-2
Les FGF (Fibroblast Growth factors’)
sont une famille de 23 isoformes (10).
Le FGF-2 (bFGF [basic FGF]), qui est,
avec le FGF-1 (aFGF [acid FGF]), la
plus étudiée des isoformes, a été iden-
ti é pour la première fois en 1974 par
Gospodarowicz pour son action sur la
prolifération et la différenciation des
broblastes en culture (11). Le FGF-2
contient 146 acides aminés et a un poids
moléculaire de 18 à 24 kilodaltons (kD)
[1, 2]. Pour l’ensemble de la famille des
FGF, la transduction du signal se fait par
l’intermédiaire de quatre récepteurs tyro-
sine kinase transmembranaire (FGFR
1-4), qui peuvent lier indifféremment
tous les FGF, mais avec une affinité
différente.
Le FGF-2, présent dans pratiquement
tous les tissus, est synthétisé par de très
nombreux types cellulaires, et presque
toutes les cellules possèdent un récepteur
spéci que pour ce facteur. Le FGF-2
nécessaire à la prolifération et au main-
tien de la différenciation d’un grand
nombre de cellules d’origine méso- et
neuro-ectodermique, notamment les
cellules endothéliales et les myocytes
cardiaques et vasculaires, joue un rôle
important dans la régulation de la vascu-
larisation, ainsi que dans la formation
du tissu nerveux et du tissu conjonctif.
Son action neurotrophique et un puissant
effet angiogénique ont été démontrés in
vitro. Ses effets sur le développement
embryonnaire et néonatal, l’angio genèse
et la cicatrisation tissulaire ont, eux,
été démontrés in vivo. C’est un facteur
heparin binding, c’est-à-dire se xant
aux glycosaminoglycanes de la famille
des héparanes sulfates lors de son trans-
fert dans l’organisme.
Le FGF-2 accélère la réépidermisation
(12) et la formation du tissu de granula-
tion en favorisant la synthèse de différents
composants de la matrice extracellulaire
dont le collagène, la bronectine et des
protéoglycanes (13). Une administration
locale accélère la cicatrisation de plaies
chez le porc (12) et améliore la cicatri-
sation chez le rat diabétique (16). Par
ailleurs, le FGF-2 accélère la cicatrisa-
tion d’une plaie ischémique (17). Dans
la cicatrisation après brûlure, il inter-
vient lors de l’angiogenèse en stimulant
la production et le relargage d’enzymes
nécessaires au “démarrage” de l’angio-
genèse et en stimulant la prolifération et
l’organisation en μtubules des cellules
endothéliales. Par ailleurs, il va favoriser
la cicatrisation dermique en permettant
la multiplication et la migration des
fibroblastes et la synthèse de colla-
gène et accélérer la réépidermisation
en multipliant les kératinocytes. Cette
action sur la réépidermisation a été
démontrée expérimentalement (18, 19) et
surtout en clinique dans une large étude
multicentrique chinoise. L’application
topique de FGF-2 (recombinant d’ori-
gine bovine) a permis l’accélération de
la cicatrisation et la réduction de la durée
d’hospitalisation de patients présen-
tant des brûlures au deuxième degré
super cielles et profondes
(20).
Cette
même étude a été élargie à un groupe
de patients avec une zone donneuse de
greffe et à un autre groupe de patients
porteurs d’ulcère chronique. Elle a
également montré une accélération de
la cicatrisation (21). Très récemment,
le FGF-2 a été utilisé dans deux études
cliniques japonaises, dans lesquelles il
a été démontré qu’il améliore la qualité
de greffe de peau chez l’adulte (22) et
l’aspect hypertrophique de cicatrice de
brûlure au deuxième degré chez l’enfant
(23). Une amélioration signi cative de
la pigmentation, de la souplesse et de la
vascularisation a été retrouvée.
KGF-1 et KGF-2
(Keratinocyte Growth Factor)
Le KGF-1 et le KGF-2 sont deux facteurs
de la famille des FGF (KGF-1 = FGF-7
et KGF-2 = FGF-10) qui sont sécrétés
par les broblastes et les cellules endo-
théliales. Les KGF sont des protéines
de 26 et 28 kD. Ils interagissent avec
un récepteur retrouvé exclusivement
au niveau des cellules épithéliales
(24, 25).

DOSSIER
tmiqu
Le Courrier de la Transplantation - Volume VII - n
o 2 - avril-mai-juin 2007
69
Chez les souris transgéniques sans KGF,
l’épiderme est atrophique (25) et on
retrouve une diminution de l’expression
des KGF chez les souris diabétiques (26)
ou traitées par corticoïdes (27). L’adminis-
tration de KGF-1 ou de KGF-2 accélère la
réépithélialisation et augmente la synthèse
de collagène par les broblastes par l’in-
termédiaire des cellules épithéliales qui
sécrètent du PDGF, du TGFβ et des FGF
(28, 29). L’épidermisation de greffes cuta-
nées en let sur le rat “nude” est accélérée
par le KGF-2 (30). Récemment, l’action
d’un facteur proche des KGF et qui est
sécrété par les kératinocytes suprabasaux
après une lésion cutanée, le FGF-22, a
été mise en évidence dans la cicatrisa-
tion cutanée (31). Les KGF agissent sur
les kératinocytes, mais aussi sur d’autres
types de cellules épithéliales comme les
cellules intestinales et les hématocytes.
Ils protègent également ces cellules des
effets d’une irradiation ou d’un stress
oxydatif (32). Ils accélèrent la cicatrisa-
tion du derme et de l’épiderme chez le
rat transfecté par des liposomes contenant
du KGF ADNc (33).
Dans un modèle de brûlure super cielle
et profonde chez le porc, un KGF recom-
binant augmente la réépidermisation et
une hybridisation in situ retrouve une
expression prononcée de KGFR dans
les follicules pilaires et dans les kérati-
nocytes épidermiques (58).
En clinique, le KGF-2 accélère la cica-
trisation des ulcères veineux (34) et
l’intérêt du KGF-1 et 2 est évalué dans
des études en cours chez des patients
souffrant d’ulcérations buccales après
radiochimiothérapie.
Les KGF ont donc un rôle important
dans la reconstitution du derme et de
l’épiderme après brûlure.
VEGF
(Vascular Endothelial Growth Factor)
Le VEGF, appelé autrefois Vascular
Permeability Factor, est une glyco-
protéine homodimérique de 45 kD qui
présente quatre isoformes. Le VEGF,
comme les FGF, est un facteur heparin
binding. Puissant facteur angiogénique,
il agit essentiellement sur les cellules
endothéliales et joue un rôle dans le
développement des vaisseaux et dans
la réparation de l’endothélium.
Le VEGF a d’abord été identi é comme
une protéine sécrétée par des cellules
tumorales permettant d’augmenter la
perméabilité des microvaisseaux (35).
Ensuite, il se révéla être un facteur mito-
gène spéci que stimulant la prolifération
des cellules endothéliales vasculaires
(36). Son action sur la relaxation des
artères coronaires a été montrée (37),
ainsi que son action angiogénique favori-
sant la néoangiogenèse dans des modèles
animaux de lambeaux ischémiés (38,
39), dans des modèles d’ischémie liée
au gon age d’une prothèse d’expansion
tissulaire, ou encore dans des modèles
d’ischémie myocardique (40). L’adminis-
tration de VEGF stimule la libération de
monoxyde d’azote (NO) par les cellules
des endothéliums vasculaires, et la
NO
Synthase Inhibitor administrée dans un
modèle d’aorte thoracique explantée de
rat, en diminuant le taux de NO, augmente
l’expression d’ARNm VEGF (41).
Chez des patients atteints d’artériopathie
oblitérante des membres inférieurs, un
gène codant pour le VEGF a été injecté
en intra-artériel, ce qui a permis de
développer une circulation collatérale
distale (42).
Après une effraction cutanée ou après
brûlure, le VEGF est sécrété d’abord par
les kératinocytes, les macrophages et les
broblastes (43) ; sa production augmente
en réponse à la lésion (44) et favorise ainsi
la revascularisation. L’administration de
VEGF augmente le tissu de granulation
dans des plaies expérimentales, isché-
miques ou non (45). Le VEGF, par son
action angiogénique, favorise donc la
cicatrisation après brûlure.
PDGF
(Platelet Derived Growth Factor)
Le PDGF est un polypeptide organisé en
homo- ou hétérodimère par combinaison
de deux chaînes unies par des ponts
disulfures. Il présente trois isomères :
le PDGF-AA, le PDGF-AB et le PDGF-
BB, qui agissent sur deux récepteurs
spécifiques : α pour la chaîne A et β
pour la chaîne B (46).
Il est contenu dans les granules α des
plaquettes, où il a été initialement mis en
évidence, et on le retrouve aussi dans les
macrophages, les cellules endothéliales
et les cellules musculaires lisses.
Il est chémotactique pour les broblastes,
les monocytes, les polynucléaires neutro-
philes et les macrophages (47) et, in vitro,
il favorise l’organisation en μtubules de
cellules endothéliales en culture. Il est
mitogénique pour les broblastes et les
cellules musculaires lisses vasculaires.
Il stimule la production de collagène, de
protéoglycanes et agit pendant la phase
lésionnelle et la phase in ammatoire (48,
49). Il accélère la cicatrisation chez le rat
diabétique (50) et dans une série clinique
d’ulcères chroniques (51).
Dans la cicatrisation après brûlure, il
intervient lors de la première phase de
détersion et lors de la cicatrisation par
son effet pro-in ammatoire, angiogé-
nique et son action sur les broblastes.
Dans un modèle de brûlure super cielle
et profonde chez le porc, le PDGF-BB
augmente la formation de tissu de granu-
lation et n’a pas d’action sur la réépider-
misation (52).
TGFβ
(Transforming Growth Factor β)
Le TGFβ est une glycoprotéine de 25 kD,
de structure homodimérique et contenant
122 acides aminés par chaîne. Il a été
initialement isolé à partir de cellules
cancéreuses (53).
Il présente cinq isoformes (TGFβ 1-5),
trois récepteurs connus (deux à haute
af nité : molécules transmembranaires ;
un à basse af nité : récepteur III, dans
la matrice extracellulaire au niveau de
protéoglycanes) et se retrouve dans le
rein, le foie, le cœur et les vaisseaux
(54). Il est libéré par les plaquettes, les
macrophages et les broblastes.

DOSSIER
tmiqu
Le Courrier de la Transplantation - Volume VII - n
o 2 - avril-mai-juin 2007
70
Des rôles biologiques ont été démon-
trés dans le développement et la matu-
ration du système cardiovasculaire dès
la vie embryonnaire. Le TGFβ a un
rôle morphogénique sur les broblastes
cardiaques et un rôle antiprolifératif sur
les cellules endothéliales et les macro-
phages. Son rôle angiogénique a été
démontré. In vivo, il stimule la formation
de vaisseaux et, in vitro, il inhibe la proli-
fération de cellules endothéliales, régule
la protéolyse de la matrice extracellulaire
et stimule, par l’intermédiaire de l’ac-
tivation des broblastes, la production
de bronectine et de collagène (55). Le
PDGF, libéré par les plaquettes pendant
la formation du thrombus, exerce un
chimiotactisme sur les macrophages
qui sécrètent du TGFβ.
L’action principale du TGFβ est exercée
sur la migration, la maturation et l’acti-
vation (synthèse de matrice extracellu-
laire) des broblastes. Les principales
isoformes étudiées sont le TGFβ1, β2 et
β3. Le TGFβ1 accélère la cicatrisation
chez le rat et le lapin dans un modèle
de plaies cutanées irradiées, traitées
par corticoïdes ou non (56, 57). Une
augmentation de l’expression du TGFβ1
se retrouve au niveau des cicatrices
chéloïdes (58) et hypertrophiques (59).
En fait, l’action des trois principales
isoformes de TGFβ n’est pas la même.
Le TGFβ1 et le TGFβ2 favorisent la
production de matrice extracellulaire et
donc de cicatrice breuse, tandis que le
TGF
β
3 prévient la survenue de cicatrices
breuses (60). La neutralisation par des
anticorps de l’action des TGF
β
1 et
β
2
ou l’administration de TGFβ3 rédui-
sent l’épaisseur de la cicatrice chez le
rat (61). Par ailleurs, l’administration
de TGFβ1 provoque une brose dans
un modèle de cicatrice fœtale chez le
rat (62) et l’analyse d’une plaie fœtale
montre l’absence de TGFβ1 (63). Des
taux faibles de TGFβ1 et 2 et de PDGF et
des taux élevés de TGFβ3 sont retrouvés
dans les plaies embryonnaires, qui ont
comme caractéristique de régénérer sans
cicatrice (63). L’administration topique
par un gel d’un peptide synthétique
antagoniste du TGFβ, dans un modèle
de brûlure chez le porc et d’excision
cutanée chez le porc et le lapin, a montré
une accélération de la réépidermisation
et une diminution de la contraction et
de l’épaisseur de la cicatrice (64). Les
TGFβ1 et β2 ont donc probablement une
action favorisant l’apparition d’une cica-
trice hypertrophique ou chéloïde chez
le brûlé.
Le TGFα, qui est sécrété par les macro-
phages et les lymphocytes, agit égale-
ment dans la cicatrisation cutanée en
favorisant le développement du tissu
de granulation et en stimulant la réépi-
dermisation et l’angiogenèse.
EGF (Epidermal Growth Factor)
L’EGF, peptide de 5,7 kD, isolé initiale-
ment à partir de glande sous-maxillaire
de souris, est sécrété par les kératinocytes
et les macrophages. L’EGF stimule la
prolifération des myocytes vasculaires. Il
accélère l’épithélialisation et augmente la
production de collagénases par les bro-
blastes permettant un remodelage, une
maturation du derme. L’expression du
récepteur de l’EGF est augmentée dans
les cicatrices hypertrophiques (65), ce
qui permet de penser que l’EGF joue un
rôle dans la survenue de cicatrices hyper-
trophiques. L’expression du récepteur de
l’EGF est diminuée dans les broblastes
anciens (66), ce qui peut participer au
ralentissement de la cicatrisation chez les
sujets âgés. L’EGF inhibe par ailleurs la
contraction d’une cicatrice fœtale.
L’administration d’EGF accélère la cica-
trisation et la réépidermisation dans des
modèles de plaies (67) et de brûlures du
deuxième degré super cielles (68). Il joue
donc également un rôle important dans la
cicatrisation cutanée après brûlure.
En revanche, l’utilisation topique d’EGF
n’a pas accéléré l’épidermisation de
plaies super cielles dans une étude chez
le volontaire sain (69).
IGF (Insulin-like Growth Factor)
L’IGF est un peptide circulant de
70 acides aminés, sécrété principalement
au niveau du foie par les hépatocytes
et au niveau des muscles squelettiques.
Il est aussi sécrété par les cellules endo-
théliales, les myocytes vasculaires, les
fibroblastes, les neutrophiles et les
macrophages lors d’une lésion cutanée
(70). Il existe deux isoformes : l’IGF-I et
l’IGF-II. Il se xe à un récepteur spéci-
que et a des effets métaboliques sembla-
bles à ceux de l’insuline. Il stimule la
croissance des cellules endothéliales des
microvaisseaux, mais plus faiblement
que le FGF-2 ou le PDGF. L’expression
de l’IGF est stimulée par le FGF-2 dans
les broblastes et par le PDGF dans les
myocytes vasculaires. L’IGF stimule la
prolifération des kératinocytes et des
broblastes et la synthèse du collagène.
Il participe au contrôle du turnover des
cellules endothéliales et favorise l’an-
giogenèse (71). La concentration de
l’IGF-II dans les tissus diminue rapi-
dement après la naissance. C’est donc,
en dehors de la période fœtale, essentiel-
lement l’IGF-I qui joue un rôle dans la
cicatrisation cutanée. Sa concentration
augmente dans les 48 heures qui suivent
une plaie (70) et est diminuée chez le rat
diabétique (72) ou le rat traité par corti-
coïde (73). Par ailleurs, l’administration
d’IGF-I accélère la cicatrisation chez le
rat diabétique ou traité par corticoïdes.
Dans un modèle de brûlure thermique
chez le rat, la transfection par le gène
de l’IGF-I accélère la cicatrisation (74).
L’IGF-I a donc également un rôle dans
la cicatrisation après brûlure.
Résumé chronologique de l’action
des facteurs de croissance qui inter-
viennent dans la cicatrisation cutanée
(4, 5) [tableau]
Lors de la première phase succédant à
la lésion cutanée, la phase d’in amma-
tion, les plaquettes libèrent le PDGF,
le TGFα et β et l’EGF. Ces facteurs
attirent et stimulent les polynucléaires
neutrophiles qui jouent un rôle lors de la
phase de détersion par leurs actions de
phago cytose et de contrôle de l’infection
locale. Ils agissent aussi sur les macro-
phages qui produisent PDGF, TGFβ,
FGF-2, EGF, cytokines et participent à
la phagocytose, ainsi que sur les lympho-
cytes qui produisent le TGFβ et des

DOSSIER
tmiqu
Le Courrier de la Transplantation - Volume VII - n
o 2 - avril-mai-juin 2007
71
cytokines. Les cellules endothéliales des
vaisseaux et les kératinocytes stimulent
eux aussi les neutrophiles ainsi que les
monocytes qui vont sécréter le PDGF, le
TGFβ, le TNFα (Tumor Necrosis Factor)
et l’IL-1 (interleukine 1). Les polynu-
cléaires neutrophiles, les macrophages,
les lymphocytes et les monocytes vont
stimuler la migration, la multiplica-
tion et la synthèse des broblastes et
des cellules endothéliales. Les cellules
endothéliales et les broblastes produi-
sent les KGF-1 (ou FGF-7) et KGF-2
(ou FGF-10) qui vont stimuler la multi-
plication de cellules épithéliales. Par
ailleurs, le PDGF et le FGF-2 agissent
sur les myocytes vasculaires et les bro-
blastes qui sécrètent l’IGF-I, qui stimule
à son tour la prolifération des cellules
endothéliales, des kératinocytes et des
broblastes. Cette phase in ammatoire
qui dure quelques jours est suivie par
la phase dite de “prolifération”, durant
laquelle les broblastes vont synthétiser
des collagènes de type I et III, le FGF-
2, l’IGF-I, le TGFα et le PDGF. Les
cellules endothéliales, qui sont attirées
par le PDGF, se multiplient sous l’effet
du VEGF et du FGF-2, et s’organisent
en microtubules et en petits vaisseaux
en “glissant” sur la bronectine produite
par les fibroblastes ; ainsi s’instaure
l’angiogenèse. Les fibroblastes, par
leur synthèse, agissent donc aussi sur
les cellules endothéliales (migration,
multiplication et organisation) ainsi
que sur les cellules épithéliales. Ces
broblastes, lorsqu’ils ont synthétisé
la matrice extracellulaire, peuvent se
transformer, sous l’effet du PDGF et du
TGFβ produits par les macrophages, en
myo broblastes qui vont contracter la
plaie, participant à l’aspect rétractile des
cicatrices de brûlure. Les kératinocytes
vont se multiplier sous l’effet du FGF-2
(produit par les cellules endothéliales,
les broblastes et les macrophages), de
l’EGF (synthétisé par les macrophages),
Tableau. Structure et fonctions biologiques du RGTA (Regenerating agents) et des facteurs de croissance ayant un rôle dans la
cicatrisation après brûlure.
Structure Cellules sécrétantes Distribution Rôles biologiques Récepteurs
FGF-2 Gène : 3 exons et 2 introns
sur chromosome 4 146 AA
pas de séquence signal
4 isoformes de 18 à 24 kD
Macrophages
cellules endothéliales
broblastes
Cerveau, hypophyse, rétine,
glande surrénale, foie, rein,
prostate, thymus, os,
corps jaune, placenta
Angiogénique, myogénique,
neurotrophique, stimule la production
et le relargage d’enzymes nécessaires
à la digestion tissulaire précédant
la prolifération et la migration
des cellules endothéliales
Cellules endothéliales,
cellules musculaires,
myocytes cardiaques pendant
les périodes fœtale
et néonatale, myoblastes,
ostéoblastes
4 récepteurs di érents isolés
KGF-1
et 2
Famille des FGF 26 et 28 kD Fibroblastes
cellules endothéliales
Épiderme, rein, vessie,
estomac, pancréas, intestin
Réépithélialisation
(synthèse de collagène)
Cellules épithéliales
VEGF Glycoprotéine homodimérique
45 kD
4 isoformes
(121, 165, 189, et 206 AA)
Gène : 8 exons
Kératinocytes,
macrophages, broblastes
Myocyte cardiaque,
cerveau, glande pituitaire,
rein, foie, ovaire
Angiogenèse, réendothélialisation,
régulation de la perméabilité capillaire,
stimulation de l’expression
et du relargage d’enzyme dont l’action
précède la néoangiogenèse
Exclusivement les cellules
endothéliales micro-
et macrovasculaires
2 types de récepteurs
exprimés en permanence
PDGF Dimère
3 isoformes : AA, AB, BB
granules α des plaquettes
macrophages,
cellules musculaires lisses
et endothéliales
Vaisseaux Détersion d’une plaie, angiogenèse,
chémotactique pour broblaste, neutro-,
macro-, mitogénique pour bro.
et cellules musculaires lisses
Polynucléaires neutrophiles
macrophages
TGFβ Glycoprotéine 25 kD
5 isoformes
Plaquettes
macrophages, monocytes,
lymphocytes, broblastes
Cœur, foie, rein, vaisseaux Angiogenèse, régulation
de l’angiogénèse, stimulation
des broblastes (synthèse de collagènes,
GAG, bronectine)
Fibroblastes,
cellules endothéliales
EGF 5,7 kD Kératinocytes,
macrophages
Derme, vaisseaux Réépithélialisation, remodelage
et maturation du derme
Cellules épithéliales,
broblastes,
myocytes vasculaires
IGF-I Peptide 70 AA Fibroblastes
cellules endothéliales
myocytes vasculaires
macrophages
Foie, vaisseaux Stimule les broblastes, les kératinocytes,
l’épidermisation, la cicatrisation dermique
et angiogénique
Fibroblastes,
cellules endothéliales
RGTA Dérivé de dextran obtenu
par substitutions successives
65 kD
Angiogénique, myogénique,
ostéogénique, favorise la cicatrisation
de divers tissus, en mimant les propriétés
des héparanes sulfates
Se lit aux facteurs
de croissance “à a nité
pour l’héparine” : bFGF, VEGF,
TGFβ, PDGF, BMP, ou l’HBEGF
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%