M Prostate, adénome et diplopie

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 3 - mai-juin 2009
128
Cas clinique
M
onsieur C.J. a 75 ans. Ses antécédents sont
constitués d’un diabète de type 2, identifié
5 ans auparavant et traité par règles diététi-
ques et glinide (Novonorm®). Une hypercholestérolémie
associée est traitée par statine (Elisor® 40). Tout récem-
ment a été mis en évidence un carcinome prostatique
dont l’extension a fait récuser l’ablation chirurgicale. La
thérapeutique a reposé sur une irradiation pelvienne et,
en attendant sa pleine efficacité, la mise en route d’un
traitement par agoniste de la GnRH (Décapeptyl® LP
3 mg). La première injection a été parfaitement tolé-
rée. En particulier, il n’a été observé aucun symptôme
de flare up. Un mois plus tard, une nouvelle injection
intramusculaire de la formulation retard de Décapeptyl®
est effectuée. Elle est très rapidement suivie de l’appa-
rition de céphalées intenses, d’une baisse de l’acuité
visuelle, d’une diplopie et d’un ptosis droit, deux signes
témoins d’une parésie du III homolatéral. Cette bruyante
symptomatologie amène à hospitaliser le patient en
urgence.
Aux céphalées frontales et rétro-orbitaires intenses
s’associent des nausées. L’examen ophtalmologique
confirme le déficit partiel du nerf moteur oculaire
commun droit. Le reste de l’examen neurologique est
normal. Le patient pèse 85 kg pour 1,70 m, sa pression
artérielle est à 130/80 mmHg. Il apparaît en euthyroïdie
et en eucortisolisme cliniques. Le tableau clinique fait
réaliser en urgence une IRM encéphalique, qui objective
la présence d’une lésion hétérogène de l’hypophyse.
Le diaphragme sellaire est discrètement bombant.
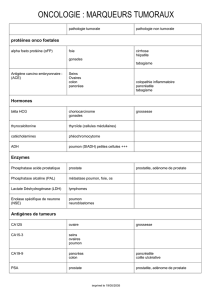
On est donc en présence d’un tableau d’apoplexie
hypophysaire (photo). Une intervention transsphé-
noïdale de décompression est rapidement réalisée et
est suivie d’une évolution postopératoire simple avec
disparition des céphalées et correction partielle de la
diplopie. L’évaluation de la fonction antéhypophysaire
retrouve alors un déficit pituitaire composite associant
insuffisances corticotrope, thyréotrope et somatotrope.
Le taux de prolactine plasmatique est à 3 ng/ml pour
une norme inférieure à 25. Le taux plasmatique des
gonadotrophines est indétectable, avec une testos-
téronémie inférieure à 0,1 ng/ml, chez un patient qui
a reçu 2 injections d’une formulation retard d’un ago-
niste de la GnRH. Une substitution par hydrocortisone
(15 mg/j) et LT4 (75 µg/j) est mise en route. Les injections
de Décapeptyl® sont interrompues et le relais est pris
par un traitement antiandrogénique pur.
Le tableau observé est donc celui d’une apoplexie
hypophysaire. Deux explications sont possibles à cet
accident aigu survenu soit sur un adénome pituitaire
silencieux et méconnu, soit sur une métastase pituitaire
du carcinome prostatique. La première hypothèse est
la plus vraisemblable.
La chronologie des événements permet de conclure à la
responsabilité du traitement par analogue de la GnRH.
Cet “effet secondaire” a déjà été rapporté à plusieurs
reprises dans deux situations particulières. Il s’agis-
sait, dans les premières circonstances, d’évaluations
de la fonction hypophysaire chez des patients atteints
d’un adénome hypophysaire antérieurement identifié.
L’injection i.v. de GnRH a été suivie d’un tableau aigu
d’apoplexie hypophysaire (1-3). Ce risque, rare mais
réel, a fait déconseiller l’utilisation du test à la GnRH
pour l’évaluation fonctionnelle hypophysaire dans un
contexte de macroadénome pituitaire. La deuxième
Prostate, adénome et diplopie
Jean-Marc Kuhn*
Photo.
* Service d’endocrinologie,
diabète et maladies méta-
boliques, CHU de Rouen.

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIII - n° 3 - mai-juin 2009
129
Prostate, adénome et diplopie
situation correspond à celle de Monsieur C.J. avec apo-
plexie, induite par un analogue de la GnRH prescrit à titre
thérapeutique, d’un adénome hypophysaire silencieux et
méconnu. Ce genre d’événement indésirable, révélateur
de la présence de l’adénome hypophysaire, a en effet
été décrit à plusieurs reprises (4-8). Cet accident spec-
taculaire apparaît suffisamment rare pour ne pas faire
conseiller la réalisation d’une IRM hypophysaire avant
l’initiation d’un traitement par analogue de la GnRH pour
carcinome de prostate. Au demeurant, les prescripteurs
doivent garder présent à l’esprit qu’un tel événement
peut survenir et qu’il nécessite alors une prise en charge
endocrinologique et neurochirurgicale en urgence dans
le double but de lever la compression des organes de
voisinage par l’adénome hypophysaire apoplectique et
de substituer l’insuffisance anté hypophysaire.
Enfin, la chronologie des événements observés
chez le patient (apparition des céphalées et de
l’ophtalmoplégie après injection d’un analogue
de la GnRH) permet d’écarter l’hypothèse d’une
métastase hypophysaire du carcinome de prostate,
cette localisation secondaire, quoique rare, étant
possible. Dans ce dernier cas, la symptomatologie
précède l’injection de l’agoniste de la GnRH, ce
qui amène à réaliser des examens radiologiques
encéphaliques avant la mise en route du traite-
ment. Une fois le diagnostic de métastases du car-
cinome de prostate établi, l’évolution, dans les cas
publiés, apparaît favorable sous traitement par
analogue de la GnRH, la lésion régressant sous
l’influence du traitement médical du carcinome
prostatique (9, 10).
■
1.Otsuka F, Kageyama J, Ogura T, Makino H. Pituitary apoplexy
induced by a combined anterior pituitary test: case report and
literature review. Endocr J 1998;45:393-8.
2.
Hernandez Morin N, Huet D, Hautecouverture M. Two cases
of non-functional gonadotroph adenoma pituitary apoplexy
following GnRH-agonist treatment revealing gonadotroph
adenoma and pseudopituitary apoplexy after GnRH admi-
nistration. Ann Endocrinol 2003;64:227-31.
3.Yoshino A, Katayama Y, Watanabe T et al. Apoplexy accom-
panying pituitary adenoma as a complication of preopera-
tive anterior pituitary function tests. Acta Neurochir (Wien)
2007;149(6):557-65.
4.
Chanson P, Schaison G. Pituitary apoplexy caused by GnRH-
agonist treatment revealing gonadotroph adenoma. J Clin
Endocrinol Metab 1995;80:2267-8.
5.Reznik Y, Chapon F, Lahlou N, Deboucher N, Mahoudeau J.
Pituitary apoplexy of a gonadotroph adenoma following gona-
dotrophin releasing hormone agonist therapy for prostatic
cancer. J Endocrinol Invest 1997;20:566-8.
6.Błaut K, Wiśniewski P, Syrenicz A, Sworczak K. Apoplexy
of clinically silent pituitary adenoma during prostate can-
cer treatment with LHRH analog. Neuro Endocrinol Lett
2006;27:569-72.
7.Massoud W, Paparel P, Lopez JG, Perrin P, Daumont M,
Ruffion A. Discovery of a pituitary adenoma following a
gonadotropin-releasing hormone agonist in a patient with
prostate cancer. Int J Urol 2006;13:303-4.
8.Hands KE, Alvarez A, Bruder JM. Gonadotropin-releasing
hormone agonist-induced pituitary apoplexy in treatment of
prostate cancer: case report and review of literature. Endocr
Pract 2007;13:642-6.
9.Couldwell WT, Chandrasoma PT, Weiss MH. Pituitary gland
metastasis from adenocarcinoma of the prostate. Case report.
J Neurosurg 1989;71:138-40.
10.Losa M, Grasso M, Giugni E, Mortini P, Acerno S, Giovanelli M.
Metastatic prostatic adenocarcinoma presenting as a pituitary
mass: shrinkage of the lesion and clinical improvement with
medical treatment. Prostate 1997;32:241-5.
Références
Les articles publiés dans “Correspondances en Métabolismes-Hormones-Diabètes et Nutrition” le sont sous la seule responsabilité de leurs auteurs.
Tout droits de reproduction, d’adaptation et de traduction par tous procédés réservés pour tous pays.
© octobre 1997 - Edimark SAS (éditions DaTeBe)
Imprimé en France – Axiom Graphic SAS - 95830 Cormeilles-en-Vexin – Dépôt légal à parution
1
/
2
100%