02/03/2016 GABEN Marion L2 CR : Nyl CHEMLI AIH JL

AIH – Immunité anti-infectieuse
02/03/2016
GABEN Marion L2
CR : Nyl CHEMLI
AIH
J-L. MEGE
20 pages
Immunité anti-infectieuse
A. Dialogue microbes – homme
Il y a un dialogue permanent entre l'hôte et les micro-organismes. Les micro-organismes sont de différentes
classes : bactéries, virus et parasites.
Des systèmes présents chez l'Homme vont permettre de neutraliser les micro-organismes. Parmi les acteurs de
cette défense contre les microorganismes pathogènes, il existe des acteurs humains (microbiote).
1/20
Plan
A. Dialogue microbe - Homme
I. Bactéries
II. Virus
III. Parasites
IV. Champignons
B. Réponse immune anti-infectieuse
C. Reconnaissance des microorganismes
I. Récepteurs cellulaires
II. Anomalies de la reconnaissance
D. La réponse immunitaire innée
I. Les acteurs de l'immunité innée
II. Mise en place du réseau des cytokines
III. Stratégies d'évitement de l'immunité innée
E. La réponse immunitaire adaptative
I. Réponse lymphocytaire
II. Echappement à la réponse adaptative

AIH – Immunité anti-infectieuse
I. Bactéries
Les bactéries peuvent être extracellulaires et intracellulaires.
Les bactéries extracellulaires ont un mode de pathogénicité essentiellement lié à la production de toxines. CR :
L'organisme doit mettre en place un certain système de défense pour éviter les infections à répétition.
Les bactéries intracellulaires sont intracellulaires obligatoires (lèpre, fièvre Q) ou intracellulaires facultatives
(tuberculose, Typhoide, Légionellose). CR : leur pathogénicité apparaît lorsque le système immunitaire est
déficient.
Elles donnent surtout des affections chroniques. La réponse immunitaire est déterminante.
Pathogénicité par réponse immune : elles détournent le système immunitaire
Ces deux types de bactéries vont engendrer des réponses immunitaires différentes.
CR : les noms de bactéries ci-dessus sont bien évidemment donnés à titre d'exemple
II. Les virus
Ce sont des organismes intracellulaires, on va donc retrouver des éléments communs avec les bactéries
intracellulaires.
Ils ont un tropisme cellulaire (CR : ils sont donc spécifiques d'un type cellulaire, ex = les monocytes) et
tissulaire qui va cibler les cellules du système immunitaire : monocytes (cytomégalovirus, virus dengue, HIV,
virus des fièvres hémorragiques), lymphocytes B (EBP = Epstein Barr virus), lymphocytes T (HIV, HTLV,
Herpes virus).
Contrairement au système bactérien, les modalités de réponses vont varier :
–soit il s'agit d'une infection aiguë puis clearence (poliovirus, virus influenza, virus respiratoire
syncytial)
–soit on a une infection aiguë puis latence (herpes virus, EBV)
–soit il y a infection aiguë puis persistance (HIV, virus hépatites B et C)
Les mécanismes immunitaires mis en jeux dans ces différentes situations sont différents.
Un mécanismes d’immunosuppression est induit par le virus pour qu'il puisse être latent ou persister.
III. Les parasites
•Les protozoaires : ils sont intracellulaires, ils présentent des points communs avec les bactéries
intracellulaires. Certains comme le toxoplasme vont être retrouvés plus particulièrement dans nos
régions. CR : on retrouve le Paludisme par le Plasmodium sp, la Maladie de Chagas par le
Trypanosoma cruzi ou encore la Leishmaniose par le Leishmania sp.
2/20

AIH – Immunité anti-infectieuse
•Les helminthes : ils sont plutôt extracellulaires, ce sont des vers. L'Ascaridiase est fréquente dans notre
région. Les autres sont des parasites que l'on retrouve beaucoup dans les pays en développement.
CR : retenir la Bilharziose et l'Ascaridiase
Un parasite suit un cycle : il va avoir différents états de maturation. Selon l'état de maturation, on aura des
niveaux de réponses immunitaires différents.
CR : La géographie est également très importante dans la fréquence des parasitoses ; elles sont plus fréquentes
dans les pays en voie de développement MAIS on note une augmentation dans les pays développés.
Une des conséquence est qu'aujourd'hui, on n'est incapables de faire des vaccins efficaces contre les parasites.
IV. Champignons
Ils peuvent être source d'infections superficielle, sous-cutanée et systémique.
Les infections systémique se font dans un contexte d'immunosuppression. On a un tableau clinique
extrêmement varié et une réponse immunitaire particulière.
CR : retenir les 2 infections superficielles, l'infection cutanée et le Cryprotococcus neoformans (méningite et
pneumonie SI ASSSOCIE AU VIH)
3/20

AIH – Immunité anti-infectieuse
B. La réponse immune anti-infectieuse
Pour faire face à ces micro-organismes il faut disposer d'un certain nombre de systèmes de reconnaissance.
Les bactéries commensales sont reconnues par le système immunitaire mais ne sont pas perçues comme des
sources de danger.
Dans un premier temps, il y a reconnaissance du micro-organisme potentiellement pathogène. La réponse
immunitaire se met en place :
–Soit elle réussit à éliminer complètement l'agent infectieux → On a besoin à la fois d'une réponse innée
et d'une réponse adaptative pour l'éliminer, il est quasiment impossible de l'éliminer qu'avec une
réponse innée. A la suite de cette élimination il y a mise en place d'une mémoire immune.
–Soit elle échoue et on développera une maladie infectieuse.
Dynamique de la réponse anti infectieuse :
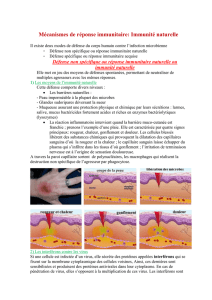
La réponse immédiate à l'infection est celle qui se fait entre 0 et 4h, elle repose essentiellement sur la réponse
immunitaire des muqueuses et de la peau (premier niveau de défense).
Au niveau de la peau et des muqueuses on retrouve :
–Des micro-organisme commensaux : la flore intestinale, cutanée, respiratoire. Elles vont prévenir les
infections par un mécanisme de correction.
–Des propriété physico-chimiques particulières : acidité de la peau, la température
–Présence de médiateurs préformés : peptides anti microbiens formés au niveau de l'intestin, de la peau
afin de mettre en place une certaine toxicité.
4/20

AIH – Immunité anti-infectieuse
Cette phase de réponse précoce joue rôle d'alarme : elle informe le système immunitaire d'un danger et donc de
la nécessité de mettre en place une réponse immunitaire innée.
Globalement il faut environ 4 jours pour avoir une réponse immunitaire innée complète. Elle se traduit par le
recrutement de cellules myéloïdes (PN, monocytes/macrophages, de cellules dendritiques ...)
Ces cellules reconnaissent les grandes classes de micro-organismes (Gram +, Gram -) grâce aux motifs qu'ils
portent à leur surface. Cela conduira à des phénomènes de phagocytose et de réaction inflammatoire.
A terme il y a élimination de 90% de l'agent infectieux. Il reste un pourcentage non négligeable d'agent
infectieux non éliminé par la réponse immunitaire innée.
Au bout de 4 jours se met en place la réponse adaptative qui repose sur l'activation des lymphocytes au niveau
des organes lymphoïdes. Cette réponse est basée sur la reconnaissance d'un antigène et non plus de motifs.
On va développer des LT et des LB spécifiques par une expansion clonale qui va déboucher sur des cellules
matures. A ce terme on est censé avoir éliminé la quasi totalité de l'agent infectieux (ce n'est pas vrai pour les
parasites de type protozoaire, ni pour les bactéries intracellulaires, car il reste un certain nombre de copies de
ces micro-organismes et il suffira d'une situation d'immunosuppression (due au stress par exemple) pour avoir
une réactivation de l'agent → on contient mais on ne nettoie pas complètement.)
Commensalisme : exemple du tube digestif
Concernant le microbiote intestinal (CR : le microbiote intestinal est le plus étudié de nos jours) on distingue 2
grands phyla :
–les Firmicutes
–les Bacteroidetes
Leur répartition varie en fonction du niveau où on va les mesurer : dans les selles , dans le colon, dans le
duodénum. On note des variations aussi si on les mesure au niveau de la paroi intestinale ou au niveau de la
lumière.
Cette flore présente une grande diversité et joue des rôles très complexes. On y trouve différentes classes de
micro-organismes :
–Probiotique : c'est une association transitoire avec l'hôte censée avoir un effet bénéfique
immunostimulant.
5/20
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%