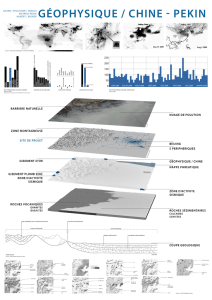
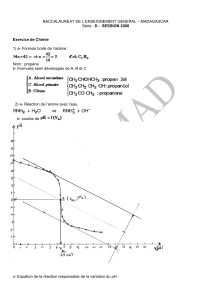
Les transformations radioactives I

29
Les transformations radioactives
I - Processus et transformations radioactifs
1 - 3 types de processus
2 - Equation radioactive
→ Emission α
ex :
ℎ
→ Emission β-
Antineutrino = particule sans charge, ni masse qui n’interagit peu avec la lumière,
particule très importante.
Ex :
→ Les neutrons vont donner des protons.
→ Emission β+
Ex :
→ Les protons vont devenir des neutrons
Emission
radioactive
Processus
Beta
Emission
Beta-
Emission
Beta+
Capture
électronique
Processus
Gamma Emission
Gamma
Conversion
interne
Processus
Alpha Emission
Alpha

30
Capture électronique
→
Ex :
→
Emission γ
→
Désexcitation du noyau
Conversion interne
→ Processus lors duquel l‘énergie émise lors de la
transition entre 2 niveaux nucléaires est utilisé pour
ioniser l’atome dans le noyau duquel à eu lieu la
transition. Ne pas confondre avec l’effet Auger.
3 - Les schémas de désintégration

31
Emission α Emission β+ et capture électronique
Emission β- Emission γ et conversion interne
Intérêt des schémas de désintégration : on peut visualiser l’enchaînement des
transformations

32
4 - Bilan énergétique et spectre d’émission
→ Spectre d’émission, courbant donnant la distribution des valeurs de l’énergie dans un
faisceau de particules.
dN/dE = nombre de particules qui ont cette énergie
Les deux types de spectres
→ Spectre de raies
→ Spectre continues

33
→ Energie γ :
→ Tous les photons γ issus d’une même transition ont la même énergie, possèdent donc
tous un spectre de raie.
N
→ Emission α et γ
→Energie produite par la réaction = (Masse initiale - Masse des produits)C². Masse disparue
pendant la réaction = Masse initiale - masse des produits.
→ Energie produite par la réaction = Ec(α) + Ec(Y) + Eγ = Energie cinétique de la particule α +
énergie de recul du noyau fils (a une valeur bien précise qui dépend des masses en
présences) + Energie du photon γ (Valeur précise).
→ La particule α a une valeur bien précise : nous avons donc un spectre de raie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%