La médecine personnalisée : historique et définition

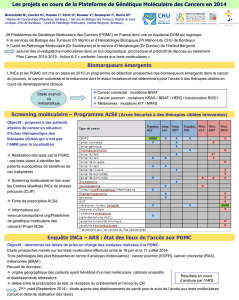
Figure 1. Cibles des agents de chimiothérapie cytotoxique et des thérapeutiques moléculaires ciblées.
Agents de chimiothérapie cytotoxique
ADN
Alkylants
Anti-
métabolites
Cisplatine
Oxaliplatine
5-FU
Gemcitabine
Enzymes
Anti-
topoisomérasesI
Anti-
topoisomérasesII
Irinotécan
Topotécan
Anthracyclines
Étoposide
Tubules
Anti-
microtubules
Taxanes
Vinorelbine
Ligand
Récepteur (partie
extracellulaire)
Récepteur (partie
intracellulaire)
Voie de signalisation
intracytoplasmique
Voie de signalisation
intranucléaire
érapeutiques moléculaires ciblées
“
284 | La Lettre du Cancérologue • Vol. XXI - n° 6 - juin 2012
ÉDITORIAL
La médecine personnalisée :
historique et défi nition
Personalized medicine: history and defi nition
Dr Christophe
LeTourneau
(département d’oncologie médicale,
institut Curie ;
unité d’investigation clinique,
Inserm U900, Paris).
À
bien y réfl échir, l’expression “médecine personnalisée” ressemble à première
vue à une lapalissade. En eff et, on peut se demander quelle intervention
médicale n’est pas “personnalisée”, dans le sens où chaque acte médical est
nécessairement adapté au patient, à la maladie dont il souff re, à son état général
etsescomorbidités. Et pourtant, la médecine personnalisée est une notion récente qui
parle à tout le monde, que ce soit dans le milieu médical ou dans la population générale.
En oncologie, le terme de “médecine personnalisée” n’est apparu dans
lelangage courant qu’au moment de l’émergence des thérapeutiques moléculaires
ciblées dans l’arsenal thérapeutique. À l’inverse des agents de chimiothérapie
cytotoxique, quidétruisent les cellules en division en agissant sur la machine
dedivision cellulaire (ADN et microtubules, pour simplifi er), les thérapeutiques
moléculaires ciblées bloquent une voie de signalisation censée être cruciale
pour la prolifération cellulaire, l’angiogenèse, la dissémination métastatique, etc.
(fi gure1). Alorsqueles agents dechimiothérapie cytotoxique sont d’habitude
issus du
screening
demolécules provenant du milieu naturel (végétal, marin,
animal, etc.), ces composés sont typiquement synthétisés de novo afi n de bloquer
spécifi quement une voie designalisation identifi ée au préalable. Le trastuzumab,
anticorps monoclonal ciblant HER2
(Human Epidermal growth factor Receptor 2)
,
estlapremière thérapeutique ciblée à avoir été approuvée, en 1998, en association avec
lachimiothérapie, chezlespatientes atteintes d’un cancer du sein surexprimant HER2.
Depuis,unevingtaine dethérapeutiques moléculaires ciblées ont été approuvées pour
letraitement dediff érentes tumeurs solides ou d’hémopathies malignes (fi gures 2 et 3).

Figure 2. Chronologie des thérapeutiques ciblées mises sur le marché (ou sur le point de l’être).
Figure 3. érapeutiques moléculaires ciblées et leurs principales cibles.
Trastuzumab Imatinib Géfi tinib Sorafénib
érapeutiques ciblées
Lapatinib
Temsirolimus
Évérolimus
Pazopanib
Ipilimumab
Crizotinib
Vismodégib
Vandétanib
Vémurafénib
Bévacizumab
Cétuximab
Erlotinib
Cétuximab
PanitumumabTrastuzumab
Vismodégib
Vémurafénib
EGFR: Epidermal Growth Factor Receptor; HER2: Human Epidermal growth factor Receptor2; mTOR: mammalian Target Of Rapamycin; PDGFR:
Platelet-Derived Growth Factor Receptor; PI3K: phosphoinositide 3-kinase; PTEN: Phosphatase and TENsin homolog; Smo: Smoothened.
Dasatinib
Temsirolimus
Évérolimus
Smo
Ras PI3K
Raf
SRC
STAT
Prolifération/migration cellulaire
Survie cellulaire
MEK1/2 mTOR
AKT PTEN
Crizotinib
c-MET
Imatinib
Vandétanib
RET
Erlotinib
Géfi tinib
EGFR
Lapatinib
HER2
Imatinib
Sunitinib
c-KIT
Sorafénib
Sunitinib
PDGFR
Crizotinib
ALK
Sunitinib
Panitumumab
2000 2005 2010
La Lettre du Cancérologue • Vol. XXI - n° 6 - juin 2012 | 285
ÉDITORIAL
En réalité, les puristes feront remarquer que les premières thérapeutiques moléculaires
ciblées, bien que non identifi ées comme telles à l’époque et non nécessairement
médicamenteuses, ont été utilisées dès la fi n du e siècle. En eff et, en 1896, Sir Beaston
réalisa une ovariectomie bilatérale chez 5femmes présentant un cancer mammaire,
et observa une réponse clinique chez 3 d’entre elles. Le premier traitement hormonal
(antihormonal, devrait-on plutôt dire) était né. Dans les années 1930, des résultats
similaires ont été obtenus dans le même contexte en réalisant des irradiations ovariennes.

286 | La Lettre du Cancérologue • Vol. XXI - n° 6 - juin 2012
ÉDITORIAL
Enfi n, le premier traitement médicamenteux est apparu dans les années 1960 ; il s’agissait,
bien entendu, du tamoxifène. Ces traitements sont eff ectivement desthérapeutiques
moléculaires ciblées dans le sens où ils ne sont effi caces que dans les cancers mammaires
hormonodépendants, c’est-à-dire surexprimant les récepteurs aux estrogènes
ouàlaprogestérone.
Il est toutefois important de faire 2remarques avant de revenir à la notion
de“médecine personnalisée”. La première est que la frontière entre “thérapeutique
moléculaire ciblée” et “agent de chimiothérapie cytotoxique” est parfois diffi cile àdélimiter.
Ainsi, les inhibiteurs de
polo-like
kinase ou les inhibiteurs de PARP (poly[ADP-ribose]
polymérase) sont classiquement considérés comme des thérapeutiques moléculaires
ciblées. Or, les cibles que sont les
polo-like
kinases et les enzymes PARP sont desmolécules
ubiquitaires, qui plus est, très impliquées dans la division cellulaire. D’ailleurs, les inhibiteurs
de
polo-like
kinase et les inhibiteurs de PARP présentent au premier plan des toxicités
hématologiques, comme c’est le cas pour les agents de chimiothérapie cytotoxique.
La seconde est que, dans le terme “thérapeutique moléculaire ciblée”, il estsous-entendu
queces traitements ne sont effi caces que lorsque la cible est exprimée.
Celan’adesens, bien évidemment, que si la cible n’est pas exprimée dans tous les cas.
Or,ils’avère qu’un biomarqueur lié à la voie de signalisation ciblée n’a été identifi é que dans
une petite proportion de thérapeutiques moléculaires ciblées (tableau).
Ainsi,les inhibiteurs de HER2 ne sont effi caces que lorsque HER2 est surexprimé ou amplifi é
dans les cancers mammaires ou gastriques. À l’inverse, aucun biomarqueur d’effi cacité n’a été
identifi é pour les thérapeutiques moléculaires ciblées antiangiogéniques ou lesinhibiteurs
demTOR
(mammalian Target Of Rapamycin),
par exemple. Ces thérapeutiques moléculaires
ciblées pour lesquelles il existe un biomarqueur d’effi cacité ou de non-effi cacité sont
àl’origine de ce qu’on entend par “médecine personnalisée”. Finalement, ce qui est sous-
entendu dans cette expression, c’est le choix d’une thérapeutique moléculaire ciblée fondée
sur un biomarqueur, et ce indépendamment de la localisation tumorale initiale.
Tableau. Principales thérapeutiques moléculaires ciblées approuvées ou en cours d’approbation, et leurs indications.
Inhibiteur Localisation tumorale Molécules Biomarqueur
EGFR Poumon
Côlon
ORL
Erlotinib
Géfi tinib
Cétuximab
Panitumumab
Cétuximab
Mutations de l’EGFR
Mutations de l’EGFR
Mutations de KRAS
Mutations de KRAS
-
HER2 Sein
Estomac
Trastuzumab
Lapatinib
Trastuzumab
Surexpression/amplifi cation de HER2
Surexpression/amplifi cation de HER2
Surexpression/amplifi cation de HER2
mTOR Rein Temsirolimus
Évérolimus
-
-
c-KIT Tumeurs stromales gastro-intestinales Imatinib Surexpression de c-KIT
VEGF(R) Sein, rein, côlon, poumon
Rein, tumeurs endocrines
Rein, hépatocarcinome
Bévacizumab
Sunitinib
Sorafénib
-
-
-
HDAC Lymphome cutané Vorinostat -
NF-κB Myélome Bortézomib -
CTLA-4 Mélanome cutané Ipilimumab -
RAF Mélanome cutané Vémurafénib Mutations de V600 RAF
ALK Poumon Crizotinib Translocation d’ALK
CTLA-4: Cytotoxic T-lymphocyte Antigen4; EGFR: Epidermal Growth Factor Receptor; HDAC: histone déacétylase; HER2: Human Epidermal growth
factor Receptor2; mTOR: mammalian Target Of Rapamycin; VEGFR: Vascular Endothelial Growth Factor Receptor.

La Lettre du Cancérologue • Vol. XXI - n° 6 - juin 2012 | 287
ÉDITORIAL
En réalité, la médecine personnalisée n’en est qu’à ses balbutiements,
et ce pour 2raisons principales. La première est que ces thérapeutiques moléculaires
ciblées, même lorsqu’un biomarqueur existe, ont été développées dans des types tumoraux
bien particuliers. En d’autres termes, le premier niveau de décision pour l’administration
d’unethérapeutique moléculaire ciblée demeure la localisation tumorale et le type
histologique, certains biomarqueurs n’étant analysés que dans un second temps pour décider
d’un tel traitement. La deuxième raison est que le nombre des biomarqueurs qu’il est utile
d’analyser pour la prescription d’une thérapeutique moléculaire ciblée est aujourd’hui encore
très limité pour un type de cancer donné, et donc pour un patient donné (tableau).
Nous sommes donc encore loin aujourd’hui de ce que l’on entend par médecine
personnalisée. Qui plus est, lorsque l’on parle de la médecine personnalisée du futur,
quipermettra d’administrer le bon traitement au bon patient au bon moment, les malades
imaginent que ce sera en vue d’une guérison, bien entendu, et non en vue seulement
deprolonger la vie de quelques mois. Aujourd’hui, seuls le trastuzumab et l’imatinib
permettent probablement de guérir des patients, puisqu’ils sont les 2 seuls à être approuvés
en situation adjuvante, avec une diminution signifi cative du risque de récidive,
ce qui signifi e bien que la maladie résiduelle a pu dans certains cas être éradiquée.
Toutes les autres thérapeutiques moléculaires ciblées n’ont d’indication, à l’heure actuelle,
qu’en situation métastatique ou de récidive. Or, jusqu’à preuve du contraire, seuls les agents
de chimiothérapie cytotoxique (et non les thérapeutiques moléculaires ciblées) ont démontré
qu’ils étaient capables, dans de rares cas dans ce contexte, de guérir des patients en situation
métastatique (lymphome ou tumeurs germinales).
En résumé, ce que nous entendons par “médecine personnalisée”, c’est la capacité
pour un patient donné de réaliser un “profi l moléculaire” de la tumeur, et, indépendamment
de la localisation tumorale, d’administrer une thérapeutique moléculaire ciblée
(ou une association) qui va permettre de bloquer la voie de signalisation essentielle àl’origine
delaprolifération tumorale et, ainsi, d’augmenter le taux de guérison. La réalisation
d’unprofi l moléculaire exhaustif, qui consiste à étudier l’ensemble du patrimoine génétique
d’une tumeur en une seule fois, est aujourd’hui quelque chose d’envisageable grâce
auxnouvelles technologies qui sont détaillées dans ce dossier thématique. Mais l’utilisation
deces technologies est associée comme nous le verrons également à de multiples défi s.
De nombreuses institutions se sont lancées dans la médecine personnalisée,
avecessentiellement des programmes qui consistent à réaliser le profi l moléculaire
delatumeur de patients métastatiques afi n de les orienter vers des essais cliniques.
SAFIR01, coordonnée par F.André de l’institut Gustave-Roussy (IGR, Villejuif), encours,
consiste à réaliser un profi l CGH
(Comparative Genomic Hybridization)
ainsi que l’étude desmutations de PI3K et d’AKT chez des patientes atteintes d’un cancer
dusein métastatique. L’étude MOSCATO, coordonnée par J.C. Soria à l’IGR, consiste
à réaliser unprofi l moléculaire chez des patients candidats pour un essai de phaseI
afi n de lesorienter vers le plus pertinent. Des programmes similaires à ce dernier sont
déjà encours auMDAnderson Cancer Center (États-Unis). Les Pays-Bas, le Canada
etl’Angleterre
( eStratifi ed Medicine Program)
ont initié des programmes qui consistent
à réaliser un profi l moléculaire chez tout patient qui présente un cancer. Enfi n,
nous mettons actuellement en place, à l’institut Curie, l’essai de phase II, randomisé,
multicentrique, de preuve de concept SHIVA, qui vise à comparer l’effi cacité d’un traitement
fondé surleprofi l moléculaire de la tumeur à celle d’un traitement conventionnel
par chimiothérapie chez des patients atteints d’un cancer réfractaire, et ce quelle que soit
lalocalisation tumorale (fi gure4, p.288). Cet essai sera ouvert aux adultes et aux enfants.
Seules desthérapeutiques moléculaires ciblées déjà approuvées seront utilisées dans cet essai.

Patients réfractaires
aux traitements standard
Consentement
signé
Consentement
signé
Patient éligible
R
érapeutique moléculaire ciblée
fondée sur le profi l moléculaire,
en monothérapie
Chimiothérapie cytotoxique
auchoix du médecin référent
Patient non
éligible
Biopsie
tumorale
Séquençage
+ SNP6.0/Cytoscan HD
+ immunohistochimie
Profi l
moléculaire
Staff
debiologie
moléculaire
érapie ciblée
approuvée
pertinente
Non Oui Crossover
”
288 | La Lettre du Cancérologue • Vol. XXI - n° 6 - juin 2012
ÉDITORIAL
Les patients progressant dans le bras standard pourront, bien entendu, recevoir le traitement
expérimental. Cet essai a pour objectif de valider le concept selon lequel l’administration
d’une thérapeutique moléculaire ciblée fondée sur le profi l moléculaire delatumeur peut
améliorer le devenir des patients en situation métastatique ou de récidive.
Au fi nal, il est très probable que le paradigme de traitement des cancers change
dansles années à venir, avec un traitement fondé sur la biologie, et non plus uniquement
surlalocalisation tumorale et le type histologique, et ce dès les stades précoces.
Figure 4. Essai SHIVA de phase II randomisé de preuve de concept comparant l’effi cacité d’un traitement orienté à partir
du profi l moléculaire de la tumeur à celle d’un traitement conventionnel chez des patients atteints d’un cancer réfractaire.
AVIS AUX LECTEURS
Les revues Edimark sont publiées en toute indépendance et sous
l’unique et entière responsabilité du directeur de la publication et
du rédacteur en chef.
Le comité de rédaction est composé d’une dizaine de praticiens (cher-
cheurs, hospitaliers, universitaires et libéraux), installés partout en
France, qui représentent, dans leur diversité (lieu et mode d’exercice,
domaine de prédilection, âge, etc.), la pluralité de la discipline. L’équipe
se réunit 2 ou 3 fois par an pour débattre des sujets et des auteurs
à publier.
La qualité des textes est garantie par la sollicitation systématique d’une
relecture scientifi que en double aveugle, l’implication d’un service de
rédaction/révision in situ et la validation des épreuves par les auteurs
et les rédacteurs en chef.
Notre publication répond aux critères d’exigence de la presse :
· accréditation par la CPPAP (Commission paritaire des publications et
agences de presse) réservée aux revues sur abonnements,
· adhésion au SPEPS (Syndicat de la presse et de l’édition des profes-
sions de santé),
· indexation dans la base de données INIST-CNRS,
· déclaration publique de liens d’intérêts demandée à nos auteurs,
· identifi cation claire et transparente des espaces publicitaires et des
publirédactionnels en marge des articles scientifi ques.
1
/
5
100%