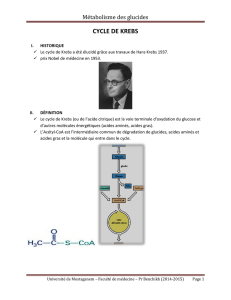
Différentes souces de l`acétyl CoA

Energétique cellulaire
B- Différentes sources de lʼacétyl-CoA
1
A
A -
-ROLE CENTRAL DE L
ROLE CENTRAL DE L ’
’ATP
ATP
B
B -
-DIFFERENTES SOURCES DE L
DIFFERENTES SOURCES DE L ’
’ACETYL
ACETYL-
-CoA
CoA
I - Décarboxylation oxydative du pyruvate
II - !
!!!-oxydation des acides gras
III - Formation et utilisation des corps cétoniques
IV - Dégradation des protéines et acides aminés
C -
-CYCLE DE KREBS
CYCLE DE KREBS
D
D –
–OXYDATIONS PHOSPHORYLANTES
OXYDATIONS PHOSPHORYLANTES
ENERGETIQUE CELLULAIRE
ENERGETIQUE CELLULAIRE
Glucides Lipides Protéines
Digestion et absorption
Glucides simples
(surtout glucose)
Acides gras
+ glycérol Acides aminés
Acétyl-CoA
Cycle de
l’acide
citrique
Cha
Chaî
îne respiratoire
ne respiratoire
xH yATP
2 CO
2
Pyruvate
Pyruvate
DIFFERENTES SOURCES DE L
DIFFERENTES SOURCES DE L’
’ACETYL
ACETYL-
-CoA
CoA
I
I -
-D
Dé
écarboxylation oxydative du pyruvate en
carboxylation oxydative du pyruvate en ac
acé
étyl
tyl-
-CoA
CoA
L’acétyl-CoA n’est produit que dans la mitochondrie:
Nécessité pour le pyruvate d’être transporté du cytoplasme
vers la mitochondrie: transporteur spécifique MCT
Complexe de la pyruvate
Complexe de la pyruvate deshydrog
deshydrogé
énase
nase:
:
!
!!!
!
!!!3 prot
3 proté
éines enzymatiques et 5 coenzymes
ines enzymatiques et 5 coenzymes
E1 - TDP (Thiamine diphosphate)
E2 – Lipoamide (Acide lipoïque lié à l’enzyme)
E3 – FAD
!
!!!Ainsi que le NAD
+
et le HS-CoA (à l’état libre)
CH
3
-CO-COOH
CO
2
TDP-E1 CO CH
3
E2-L
SH
S~
HSCoA
CH
3
-C
~
SCoA
CH
3
-CHOH-TDP
E1 O
E3-FADH
2
E2-L
S
S
E2-L
SH
S
H
E3-FAD
NAD
+
NADH + H
+
a
ab
bc
c
d
d
e
e
a)
a) R
Ré
éaction de d
action de dé
écarboxylation
carboxylation
b)
b) R
Ré
éaction d
action d’
’oxydation
oxydation
c) Formation de l
c) Formation de l ’
’ac
acé
étyl
tyl-
-CoA
CoA
d)
d) R
Ré
éoxydation
oxydation de la
de la dihydrolipoamide
dihydrolipoamide
e) Transfert des e
e) Transfert des e
-
-
sur NAD
sur NAD
+
+
Ac
Acé
étyl
tyl-
-CoA
CoA
Ac
Ac pyruvique
pyruvique
R
Ré
éaction tr
action trè
ès complexe
s complexe
avec de multiples
avec de multiples é
étapes
tapes
!
!!!
!
!!!R
Ré
éaction irr
action irré
éversible repr
versible repré
ésentant le lien entre la glycolyse et le cycle de Krebs
sentant le lien entre la glycolyse et le cycle de Krebs
Acétyl CoA est la forme activé de l'acétate.
C'est un carrefour métabolique.
Pour le glucose, on a une étape intermédiaire par le pyruvate.
A partir des lipides, dégradation des acides gras qui donnent de l'acetylCoA
Les protéines, par dégradation donnent des acides aminés, normalement ce ne sont pas
des sources d'énergie. On a une dégradation des protéines lorsque on a une régime hyper
protéique, ou quand on fait un jeun.
L'acetylCoA est dégradé dans un cycle: cycle de Krebs pour former des composés qui
vont rejoindre la chaine respiratoire.
"
I- Décarboxylation oxydative du pyruvate en acétylCoA
Lʼacétyl-CoA nʼest produit que dans la mitochondrie : Nécessité pour le pyruvate dʼetre
transporté du cytoplasme vers la mitochondrie : transporteur spécifique MCT.
Complexe de la pyruvate deshydrogénase : 3 protéines enzymatiques et 5 coenzymes :
- E1-TDF (Thiamine diphosphate)
- E2-Lipoamide (Acide lipoique lié à lʼenzyme)
- E3-FAD
Ainsi que le NAD+ et le HS-CoA (à lʼétat libre)

1
A
A -
-ROLE CENTRAL DE L
ROLE CENTRAL DE L ’
’ATP
ATP
B
B -
-DIFFERENTES SOURCES DE L
DIFFERENTES SOURCES DE L ’
’ACETYL
ACETYL-
-CoA
CoA
I - Décarboxylation oxydative du pyruvate
II - !
!!!-oxydation des acides gras
III - Formation et utilisation des corps cétoniques
IV - Dégradation des protéines et acides aminés
C -
-CYCLE DE KREBS
CYCLE DE KREBS
D
D –
–OXYDATIONS PHOSPHORYLANTES
OXYDATIONS PHOSPHORYLANTES
ENERGETIQUE CELLULAIRE
ENERGETIQUE CELLULAIRE
Glucides Lipides Protéines
Digestion et absorption
Glucides simples
(surtout glucose)
Acides gras
+ glycérol Acides aminés
Acétyl-CoA
Cycle de
l’acide
citrique
Cha
Chaî
îne respiratoire
ne respiratoire
xH yATP
2 CO
2
Pyruvate
Pyruvate
DIFFERENTES SOURCES DE L
DIFFERENTES SOURCES DE L’
’ACETYL
ACETYL-
-CoA
CoA
I
I -
-D
Dé
écarboxylation oxydative du pyruvate en
carboxylation oxydative du pyruvate en ac
acé
étyl
tyl-
-CoA
CoA
L’acétyl-CoA n’est produit que dans la mitochondrie:
Nécessité pour le pyruvate d’être transporté du cytoplasme
vers la mitochondrie: transporteur spécifique MCT
Complexe de la pyruvate
Complexe de la pyruvate deshydrog
deshydrogé
énase
nase:
:
!
!!!
!
!!!3 prot
3 proté
éines enzymatiques et 5 coenzymes
ines enzymatiques et 5 coenzymes
E1 - TDP (Thiamine diphosphate)
E2 – Lipoamide (Acide lipoïque lié à l’enzyme)
E3 – FAD
!
!!!Ainsi que le NAD
+
et le HS-CoA (à l’état libre)
CH
3
-CO-COOH
CO
2
TDP-E1 CO CH
3
E2-L
SH
S~
HSCoA
CH
3
-C
~
SCoA
CH
3
-CHOH-TDP
E1 O
E3-FADH
2
E2-L
S
S
E2-L
SH
S
H
E3-FAD
NAD
+
NADH + H
+
a
ab
bc
c
d
d
e
e
a)
a) R
Ré
éaction de d
action de dé
écarboxylation
carboxylation
b)
b) R
Ré
éaction d
action d’
’oxydation
oxydation
c) Formation de l
c) Formation de l ’
’ac
acé
étyl
tyl-
-CoA
CoA
d)
d) R
Ré
éoxydation
oxydation de la
de la dihydrolipoamide
dihydrolipoamide
e) Transfert des e
e) Transfert des e
-
-
sur NAD
sur NAD
+
+
Ac
Acé
étyl
tyl-
-CoA
CoA
Ac
Ac pyruvique
pyruvique
R
Ré
éaction tr
action trè
ès complexe
s complexe
avec de multiples
avec de multiples é
étapes
tapes
!
!!!
!
!!!R
Ré
éaction irr
action irré
éversible repr
versible repré
ésentant le lien entre la glycolyse et le cycle de Krebs
sentant le lien entre la glycolyse et le cycle de Krebs
On a le pyruvate, première réaction de décarboxylation: transfert du radical dicarboné sur
le complexe E1-TDP.
Libération de CO2.
Réaction d'oxydation, qui fait intervenir transfert de l'unité dicarboné sur l'acide lipoïque.
(qui devient sous forme réduite).
L'unité dicarbonée devient un acétyl.
Transfert de l'actyl sur le Coenzyme A. on conserve cette liaison a haut potentiel
d'hydrolyse, et on libère E2 lipoamide sous forme réduite. L'acetylCoA est libérée, il faut
ensuite ré-oxyder la lipoamide, au dépend du FAD lié a E3: on régénère le complexe E2.
Enfin, transfert des électrons sur le NAD+: fourniture de NADH + H+
Cette réaction a deux intérêts:
➔"formation de NADH, composé réduit qui va permettre de former de l'ATP sur la chaine
respiratoire.
➔"Formation d'un groupement acéthyl sous forme activé (acetyl CoA) qui pourra être
transféré, et qui va rentrer dans le cycle de krebs.
II- Béta oxydation des acides gras
1- Introduction : sources des acides gras
2
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
Introduction: source des acides gras
Introduction: source des acides gras
R
2
C
O
O
3 H
2
O
CH
2
CH
CH
2
C
O
R
1
O
C
O
R
3
OCH
2
OH
CHOH
CH
2
OH
+
3 AG
Glyc
Glycé
érol
rol
•
•TG exog
TG exogè
ènes
nes
-
-Emulsification
Emulsification par les sels biliaires
par les sels biliaires
-
-lipase pancr
lipase pancré
éatique
atique
-
-lipoprot
lipoproté
éine lipase des capillaires sanguins
ine lipase des capillaires sanguins
* TG endog
* TG endogè
ènes
nes
-
-triglyc
triglycé
éride lipase
ride lipase hormono
hormono-
-sensible
sensible du tissu adipeux
du tissu adipeux
(activation par adr
(activation par adré
énaline et glucagon par la cascade de l
naline et glucagon par la cascade de l’
’AMPc
AMPc)
)
Triglyc
Triglycé
éride ou TG
ride ou TG
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCS-CoA
O
HS-CoA
Acyl
Acyl-
-CoA
CoA
+
AMP
1°- Activation sous forme d’acyl-CoA
RC
O-
O
+
ATP
Enzyme:
Enzyme: Acyl
Acyl-
-CoA
CoA synth
synthé
étase (ME de la mitochondrie)
tase (ME de la mitochondrie)
RC
AMP
O
2 Pi
Acyl
Acyl-
-ad
adé
énylate
nylate
Exemple d
Exemple d’
’un
un ac
ac gras
gras à
àlongue cha
longue chaî
îne: C16:0 (acide palmitique)
ne: C16:0 (acide palmitique)
Acide gras
Acide gras
R
Ré
éaction globale :
action globale :
Ac
Ac. gras +
. gras + HS
HS-
-CoA
CoA + ATP
+ ATP acyl
acyl-
-CoA
CoA + AMP + 2Pi
+ AMP + 2Pi
!
!!!
!
!!!L
L’é
’équivalent de 2 ATP en ADP sont consomm
quivalent de 2 ATP en ADP sont consommé
és
s
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
les acides gras proviennent des tryglycérides d'origine exogène ou endogène
pour les triglycérides endogène, on a une emulsification dans l'intestin par les sels biliaire
puis lipase pancréatique qui libère des acides gras et du glycérol
TG + 3H2O = glycérol + 3AG
+ lipoprotéine lipase des capillaires sanguins.

Triglycérides endogènes
tissus adipeux
mobilisés par la tryglycéride lipase, hormono sensible car elle est activé par le glucagon
ou l'AMPc.
2- Activation sous forme dʼacyl-CoA
2
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
Introduction: source des acides gras
Introduction: source des acides gras
R
2
C
O
O
3 H
2
O
CH
2
CH
CH
2
C
O
R
1
O
C
O
R
3
OCH
2
OH
CHOH
CH
2
OH
+
3 AG
Glyc
Glycé
érol
rol
•
•TG exog
TG exogè
ènes
nes
-
-Emulsification
Emulsification par les sels biliaires
par les sels biliaires
-
-lipase pancr
lipase pancré
éatique
atique
-
-lipoprot
lipoproté
éine lipase des capillaires sanguins
ine lipase des capillaires sanguins
* TG endog
* TG endogè
ènes
nes
-
-triglyc
triglycé
éride lipase
ride lipase hormono
hormono-
-sensible
sensible du tissu adipeux
du tissu adipeux
(activation par adr
(activation par adré
énaline et glucagon par la cascade de l
naline et glucagon par la cascade de l’
’AMPc
AMPc)
)
Triglyc
Triglycé
éride ou TG
ride ou TG
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCS-CoA
O
HS-CoA
Acyl
Acyl-
-CoA
CoA
+
AMP
1°- Activation sous forme d’acyl-CoA
RC
O-
O
+
ATP
Enzyme:
Enzyme: Acyl
Acyl-
-CoA
CoA synth
synthé
étase (ME de la mitochondrie)
tase (ME de la mitochondrie)
RC
AMP
O
2 Pi
Acyl
Acyl-
-ad
adé
énylate
nylate
Exemple d
Exemple d’
’un
un ac
ac gras
gras à
àlongue cha
longue chaî
îne: C16:0 (acide palmitique)
ne: C16:0 (acide palmitique)
Acide gras
Acide gras
R
Ré
éaction globale :
action globale :
Ac
Ac. gras +
. gras + HS
HS-
-CoA
CoA + ATP
+ ATP acyl
acyl-
-CoA
CoA + AMP + 2Pi
+ AMP + 2Pi
!
!!!
!
!!!L
L’é
’équivalent de 2 ATP en ADP sont consomm
quivalent de 2 ATP en ADP sont consommé
és
s
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
Réaction d'activation de l'acylCoA qui demande de l'énergie, intervention de l'ATP et du
coenzyme A.
Activation: condensation de l'AMP sur l'acide gras, pour former le RCOAMP, au dépend de
l'AMP qui est hydrolysé sous forme de pyrophosphate.
Le composé RCOAMP (composé intermédiaire) , récupère le coenzyme A qui remplace
l'AMP, on obtient l'acyl-CoA.
Puis formation d'acy-CoA.
Enzyme: acyl-CoA synthétase, qui est au niveau de la membrane externe de la
mitochondrie.
2
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
Introduction: source des acides gras
Introduction: source des acides gras
R
2
C
O
O
3 H
2
O
CH
2
CH
CH
2
C
O
R
1
O
C
O
R
3
OCH
2
OH
CHOH
CH
2
OH
+
3 AG
Glyc
Glycé
érol
rol
•
•TG exog
TG exogè
ènes
nes
-
-Emulsification
Emulsification par les sels biliaires
par les sels biliaires
-
-lipase pancr
lipase pancré
éatique
atique
-
-lipoprot
lipoproté
éine lipase des capillaires sanguins
ine lipase des capillaires sanguins
* TG endog
* TG endogè
ènes
nes
-
-triglyc
triglycé
éride lipase
ride lipase hormono
hormono-
-sensible
sensible du tissu adipeux
du tissu adipeux
(activation par adr
(activation par adré
énaline et glucagon par la cascade de l
naline et glucagon par la cascade de l’
’AMPc
AMPc)
)
Triglyc
Triglycé
éride ou TG
ride ou TG
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCS-CoA
O
HS-CoA
Acyl
Acyl-
-CoA
CoA
+
AMP
1°- Activation sous forme d’acyl-CoA
RC
O-
O
+
ATP
Enzyme:
Enzyme: Acyl
Acyl-
-CoA
CoA synth
synthé
étase (ME de la mitochondrie)
tase (ME de la mitochondrie)
RC
AMP
O
2 Pi
Acyl
Acyl-
-ad
adé
énylate
nylate
Exemple d
Exemple d’
’un
un ac
ac gras
gras à
àlongue cha
longue chaî
îne: C16:0 (acide palmitique)
ne: C16:0 (acide palmitique)
Acide gras
Acide gras
R
Ré
éaction globale :
action globale :
Ac
Ac. gras +
. gras + HS
HS-
-CoA
CoA + ATP
+ ATP acyl
acyl-
-CoA
CoA + AMP + 2Pi
+ AMP + 2Pi
!
!!!
!
!!!L
L’é
’équivalent de 2 ATP en ADP sont consomm
quivalent de 2 ATP en ADP sont consommé
és
s
II
II -
-!
!!!
!
!!!-
-Oxydation des acides gras en
Oxydation des acides gras en ac
acé
étyl
tyl-
-CoA
CoA
1°- Activation sous forme d’acyl-CoA
2°- Transfert des A. gras du cytosol dans la mitochondrie
Transfert des A. gras du cytosol dans la mitochondrie
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
On consomme une molécule d'ATP, formation d'une molécule d'AMP. On a deux Pi libérés.
On a besoin de deux liaisons a haut potentiels d'énergie: L'équivalent de deux molécules
d'ATP en ADP sont consommés.
II- Transfert des acides gras du cytosol dans la mitochondrie
3
ACYL-CoA
SYNTHETASE CARNITINE
ACYL-TRANSFERASE I (CAT1)
CARNITINE
ACYL-TRANSFERASE II (CATII)
CARNITINE
ACYL-CARNITINE
TRANSLOCASE
CoA
ATP
2Pi + AMP
CYTOSOL
CYTOSOL
MEMBRANE
MEMBRANE
EXTERNE
EXTERNE
MEMBRANE
MEMBRANE
INTERNE
INTERNE
Acyl-CoA
carnitine
Acyl-carnitine
carnitine
HSCoA
Acyl-CoA
!
!!!
!
!!!-
-OXYDATION
OXYDATION
MATRICE
MATRICE
MITOCHONDRIALE
MITOCHONDRIALE
Acide gras
Acide gras
HSCoA
Acyl-carnitine
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCH
2
CH
2
CH
2
C S CoA
O
Acyl-CoA
FAD
FADH
2
Acyl
Acyl-
-CoA
CoA
deshydrog
deshydrogé
énase
nase
a)
a)
b)
b)
RCH
2
C C C S CoA
O
H
HH
2
O
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
hydratase
hydratase
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
2
21
1
RCH
2
CSCoA
O
d)
d)
CH
2
C
O
3
3-
-c
cé
éto
to-
-acyl
acyl-
-CoA
CoA
CoA-SH
R’ CSCoA
O
+ CH
3
C
O
SCoA
(3
(3-
-c
cé
éto
to-
-acyl
acyl-
-CoA)
CoA) thiolase
thiolase
Acyl
Acyl-
-CoA
CoA
(amput
(amputé
éde 2 C)
de 2 C)
Ac
Acé
étyl
tyl-
-CoA
CoA
RCH
2
C C C S CoA
O
H
HH
OH
3
32
21
1
NAD
+
NADH + H
+
L-3-OH-acyl-CoA
L
L-
-3
3-
-OH
OH-
-acyl
acyl
CoA
CoA-
-deshydrog
deshydrogé
énase
nase
c)
c)
très longue
22
24
26
Acide béhénique
Acide lignocérique
Acide cérotique
longue
14
16
18
20
Acide myristique
Acide palmitique
Acide palmitique
Acide st
Acide sté
éarique
arique
Acide arachidique
moyenne
8
10
12
Acide caprylique
Acide caprique
Acide laurique
courte
4
6
Acide butyrique
Acide caproïque
longueur de la
chaîne
nombre de
carbones
nom de l’acide gras
Classification des acides gras saturés
Il faut transformé l'acyl-CoA.
Membrane externe: L'alcoran synthétase (car met en jeu l'ATP contrairement a une
synthase). Permet de transformer l'acide gras en AcylCoA. Ce dernier se retrouve dans

l'espace intermembranaire, Il n'est pas capable de traverser la membrane interne, il
s'associe à la carnitine, transfert de la carnitine sur l'acyl, qui donne de l'acyl carnitine
coenzyme A, puis est pris en charge par une translocase, elle se retrouve au niveau de la
matrice, libération de la carnitine par une carnitine aceyl tranferase.
1- Oxydation proprement dite
Suite de réactions, oxydation, hydratation, oxydation et réaction de clivage (thiolyse).
a- Oxydation qui porte sur le C2
Enzyme: acyl-CoA deshydrogénase + FAD (on récupère du FADH2)
double liaison entre le C2 et le C3
3
ACYL-CoA
SYNTHETASE CARNITINE
ACYL-TRANSFERASE I (CAT1)
CARNITINE
ACYL-TRANSFERASE II (CATII)
CARNITINE
ACYL-CARNITINE
TRANSLOCASE
CoA
ATP
2Pi + AMP
CYTOSOL
CYTOSOL
MEMBRANE
MEMBRANE
EXTERNE
EXTERNE
MEMBRANE
MEMBRANE
INTERNE
INTERNE
Acyl-CoA
carnitine
Acyl-carnitine
carnitine
HSCoA
Acyl-CoA
!
!!!
!
!!!-
-OXYDATION
OXYDATION
MATRICE
MATRICE
MITOCHONDRIALE
MITOCHONDRIALE
Acide gras
Acide gras
HSCoA
Acyl-carnitine
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCH
2
CH
2
CH
2
C S CoA
O
Acyl-CoA
FAD
FADH
2
Acyl
Acyl-
-CoA
CoA
deshydrog
deshydrogé
énase
nase
a)
a)
b)
b)
RCH
2
C C C S CoA
O
H
HH
2
O
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
hydratase
hydratase
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
2
21
1
RCH
2
CSCoA
O
d)
d)
CH
2
C
O
3
3-
-c
cé
éto
to-
-acyl
acyl-
-CoA
CoA
CoA-SH
R’ CSCoA
O
+ CH
3
C
O
SCoA
(3
(3-
-c
cé
éto
to-
-acyl
acyl-
-CoA)
CoA) thiolase
thiolase
Acyl
Acyl-
-CoA
CoA
(amput
(amputé
éde 2 C)
de 2 C)
Ac
Acé
étyl
tyl-
-CoA
CoA
RCH
2
C C C S CoA
O
H
HH
OH
3
32
21
1
NAD
+
NADH + H
+
L-3-OH-acyl-CoA
L
L-
-3
3-
-OH
OH-
-acyl
acyl
CoA
CoA-
-deshydrog
deshydrogé
énase
nase
c)
c)
très longue
22
24
26
Acide béhénique
Acide lignocérique
Acide cérotique
longue
14
16
18
20
Acide myristique
Acide palmitique
Acide palmitique
Acide st
Acide sté
éarique
arique
Acide arachidique
moyenne
8
10
12
Acide caprylique
Acide caprique
Acide laurique
courte
4
6
Acide butyrique
Acide caproïque
longueur de la
chaîne
nombre de
carbones
nom de l’acide gras
Classification des acides gras saturés
b- Réaction d'hydratation au niveau de la double liaison, la composé formé qui est le L 3
OH acyl CoA.
enzyme: delta2 Enoyl CoA hydratase
c- Nouvelle oxydation, portant sur le C3, formation de L 3 céto acyl CoA
enzyme:L 3 OH acyl CoA deshydrogénase avec NADH
3
ACYL-CoA
SYNTHETASE CARNITINE
ACYL-TRANSFERASE I (CAT1)
CARNITINE
ACYL-TRANSFERASE II (CATII)
CARNITINE
ACYL-CARNITINE
TRANSLOCASE
CoA
ATP
2Pi + AMP
CYTOSOL
CYTOSOL
MEMBRANE
MEMBRANE
EXTERNE
EXTERNE
MEMBRANE
MEMBRANE
INTERNE
INTERNE
Acyl-CoA
carnitine
Acyl-carnitine
carnitine
HSCoA
Acyl-CoA
!
!!!
!
!!!-
-OXYDATION
OXYDATION
MATRICE
MATRICE
MITOCHONDRIALE
MITOCHONDRIALE
Acide gras
Acide gras
HSCoA
Acyl-carnitine
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCH
2
CH
2
CH
2
C S CoA
O
Acyl-CoA
FAD
FADH
2
Acyl
Acyl-
-CoA
CoA
deshydrog
deshydrogé
énase
nase
a)
a)
b)
b)
RCH
2
C C C S CoA
O
H
HH
2
O
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
hydratase
hydratase
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
2
21
1
RCH
2
CSCoA
O
d)
d)
CH
2
C
O
3
3-
-c
cé
éto
to-
-acyl
acyl-
-CoA
CoA
CoA-SH
R’ CSCoA
O
+ CH
3
C
O
SCoA
(3
(3-
-c
cé
éto
to-
-acyl
acyl-
-CoA)
CoA) thiolase
thiolase
Acyl
Acyl-
-CoA
CoA
(amput
(amputé
éde 2 C)
de 2 C)
Ac
Acé
étyl
tyl-
-CoA
CoA
RCH
2
C C C S CoA
O
H
HH
OH
3
32
21
1
NAD
+
NADH + H
+
L-3-OH-acyl-CoA
L
L-
-3
3-
-OH
OH-
-acyl
acyl
CoA
CoA-
-deshydrog
deshydrogé
énase
nase
c)
c)
très longue
22
24
26
Acide béhénique
Acide lignocérique
Acide cérotique
longue
14
16
18
20
Acide myristique
Acide palmitique
Acide palmitique
Acide st
Acide sté
éarique
arique
Acide arachidique
moyenne
8
10
12
Acide caprylique
Acide caprique
Acide laurique
courte
4
6
Acide butyrique
Acide caproïque
longueur de la
chaîne
nombre de
carbones
nom de l’acide gras
Classification des acides gras saturés
d- Puis clivage (thiolyse) avec une thiolase on récupère deux molécules: l'acétyl CoA et
l'acétyl-CoA amputé de deux C (= forme activé de l'acyl).
On fait une suite successive de cette suite de réaction.
Connaître l'acide palmitique (C16) et l'acide stéarique (C18)
A partir de ces acides gras, on a avoir une série de libération d'acetyl CoA

3
ACYL-CoA
SYNTHETASE CARNITINE
ACYL-TRANSFERASE I (CAT1)
CARNITINE
ACYL-TRANSFERASE II (CATII)
CARNITINE
ACYL-CARNITINE
TRANSLOCASE
CoA
ATP
2Pi + AMP
CYTOSOL
CYTOSOL
MEMBRANE
MEMBRANE
EXTERNE
EXTERNE
MEMBRANE
MEMBRANE
INTERNE
INTERNE
Acyl-CoA
carnitine
Acyl-carnitine
carnitine
HSCoA
Acyl-CoA
!
!!!
!
!!!-
-OXYDATION
OXYDATION
MATRICE
MATRICE
MITOCHONDRIALE
MITOCHONDRIALE
Acide gras
Acide gras
HSCoA
Acyl-carnitine
3
3°
°-
-Oxydation proprement dite
Oxydation proprement dite
RCH
2
CH
2
CH
2
C S CoA
O
Acyl-CoA
FAD
FADH
2
Acyl
Acyl-
-CoA
CoA
deshydrog
deshydrogé
énase
nase
a)
a)
b)
b)
RCH
2
C C C S CoA
O
H
HH
2
O
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
hydratase
hydratase
"
"""
"
"""2
2-
-Enoyl
Enoyl-
-CoA
CoA
2
21
1
RCH
2
CSCoA
O
d)
d)
CH
2
C
O
3
3-
-c
cé
éto
to-
-acyl
acyl-
-CoA
CoA
CoA-SH
R’ CSCoA
O
+ CH
3
C
O
SCoA
(3
(3-
-c
cé
éto
to-
-acyl
acyl-
-CoA)
CoA) thiolase
thiolase
Acyl
Acyl-
-CoA
CoA
(amput
(amputé
éde 2 C)
de 2 C)
Ac
Acé
étyl
tyl-
-CoA
CoA
RCH
2
C C C S CoA
O
H
HH
OH
3
32
21
1
NAD
+
NADH + H
+
L-3-OH-acyl-CoA
L
L-
-3
3-
-OH
OH-
-acyl
acyl
CoA
CoA-
-deshydrog
deshydrogé
énase
nase
c)
c)
très longue
22
24
26
Acide béhénique
Acide lignocérique
Acide cérotique
longue
14
16
18
20
Acide myristique
Acide palmitique
Acide palmitique
Acide st
Acide sté
éarique
arique
Acide arachidique
moyenne
8
10
12
Acide caprylique
Acide caprique
Acide laurique
courte
4
6
Acide butyrique
Acide caproïque
longueur de la
chaîne
nombre de
carbones
nom de l’acide gras
Classification des acides gras saturés
Ex: 7 tours de spires pour un composé qui est un C16, on obtient 8 acétyl-CoA.
4
C
C
16
16
(
(palmitoyl
palmitoyl-
-CoA
CoA)
)
C
14
C
12
C
10
C
8
C
6
C
4
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Ac
Acé
étyl
tyl-
-CoA
CoA
TOTAL:
TOTAL:
7 tours de spire
7 tours de spire
Equation globale de la
Equation globale de la !
!!!
!
!!!-
-oxydation
oxydation
Palmitoyl-CoA + 7 CoASH + 7 FAD + 7 NAD
+
+ 7 H
2
O
8 Acétyl-CoA + 7 FADH
2
+ 7 NADH + 7 H
+
4
4°
°-
-Bilan
Bilan é
énerg
nergé
étique :
tique :
Pour chaque tour de spire :
1 FADH
2
et 1 NADH + H
+
Activation
7 passages à travers la !
!!!-oxydation:
Activation
8 passages à travers la !
!!!-oxydation:
•
8 FADH
2
+ 8 NADH + 8 H
+
•9 acétyl-CoAdégradés dans cycle de Krebs etchaîne respiratoire
*A partir du st
*A partir du sté
éarate (C18): 120 ATP
arate (C18): 120 ATP
•
7 FADH
2
+ 7 NADH + 7 H
+
•
8 acétyl-CoA dégradés dans cycle de Krebs et chaîne respiratoire
*A partir du palmitate (C16): 106 ATP
*A partir du palmitate (C16): 106 ATP
Bilan
Bilan é
énerg
nergé
étique de la d
tique de la dé
égradation d'une mol
gradation d'une molé
écule de palmitate
cule de palmitate
!
La respiration mitochondriale produit 1,5 ATP
par FADH
2
oxydé et 2,5 ATP par NADH oxydé.
Différentes étapes ou enzymes Nombre de
NADH ou de
FADH
2
formés
Nombre
d'ATP formés
àpartir d'ADP
Activation du palmitate
Acyl-CoA deshydrogénase
!
!!!-OH-acyl-CoA deshydrogénase
-
7FADH
2
7NADH
-2
10,5
17,5
Isocitrate deshydrogénase
"
"""-Cétoglutarate deshydrogénase
Succinyl-CoA synthétase
Succinate deshydrogénase
Malate deshydrogénase
8NADH
8NADH
–
8FADH
2
8NADH
20
20
8
12
20
TOTAL 106
Au niveau du C4(dernier tour): on obtient deux acetyl-CoA.
Pour le calcul énergétique: on va calculer le nombre de NADH et de FAD produit.
A chaque tour de spire un FAD et un NAD intervient.
Équation globale de la béta oxydation pour C16:
4
C
C
16
16
(
(palmitoyl
palmitoyl-
-CoA
CoA)
)
C
14
C
12
C
10
C
8
C
6
C
4
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Acétyl-CoA
Ac
Acé
étyl
tyl-
-CoA
CoA
TOTAL:
TOTAL:
7 tours de spire
7 tours de spire
Equation globale de la
Equation globale de la !
!!!
!
!!!-
-oxydation
oxydation
Palmitoyl-CoA + 7 CoASH + 7 FAD + 7 NAD
+
+ 7 H
2
O
8 Acétyl-CoA + 7 FADH
2
+ 7 NADH + 7 H
+
4
4°
°-
-Bilan
Bilan é
énerg
nergé
étique :
tique :
Pour chaque tour de spire :
1 FADH
2
et 1 NADH + H
+
Activation
7 passages à travers la !
!!!-oxydation:
Activation
8 passages à travers la !
!!!-oxydation:
•
8 FADH
2
+ 8 NADH + 8 H
+
•9 acétyl-CoAdégradés dans cycle de Krebs etchaîne respiratoire
*A partir du st
*A partir du sté
éarate (C18): 120 ATP
arate (C18): 120 ATP
•
7 FADH
2
+ 7 NADH + 7 H
+
•
8 acétyl-CoA dégradés dans cycle de Krebs et chaîne respiratoire
*A partir du palmitate (C16): 106 ATP
*A partir du palmitate (C16): 106 ATP
Bilan
Bilan é
énerg
nergé
étique de la d
tique de la dé
égradation d'une mol
gradation d'une molé
écule de palmitate
cule de palmitate
!
La respiration mitochondriale produit 1,5 ATP
par FADH
2
oxydé et 2,5 ATP par NADH oxydé.
Différentes étapes ou enzymes Nombre de
NADH ou de
FADH
2
formés
Nombre
d'ATP formés
àpartir d'ADP
Activation du palmitate
Acyl-CoA deshydrogénase
!
!!!-OH-acyl-CoA deshydrogénase
-
7FADH
2
7NADH
-2
10,5
17,5
Isocitrate deshydrogénase
"
"""-Cétoglutarate deshydrogénase
Succinyl-CoA synthétase
Succinate deshydrogénase
Malate deshydrogénase
8NADH
8NADH
–
8FADH
2
8NADH
20
20
8
12
20
TOTAL 106
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%