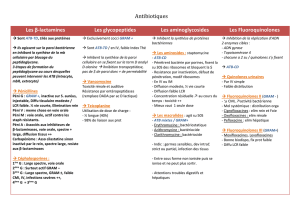
TP - Espace d`authentification univ

TP Introduction à la microbiologie – L1
Introduction
Quatre manip. de TP
! Etat frais : Mobilité
! Coloration de Gram : Morphologie
! Isolement
! Frottis sur yaourt
Les outils
! Travailler en conditions stériles
! Utilisation d’un microscope
Les consignes de sécurité

2
INTRODUCTION: importance des microorganismes…
1014 cellules dans un
corps humain.
% de bactéries?
% d’ADN humain?
Photo: nature.com

3
INTRODUCTION: importance des microorganismes…
10.000.000.000.000.000.000.000.000.000
(1028)
BACTERIES ET ARCHÉES DANS LES OCEANS
100 million de fois plus que d’étoiles dans le ciel…
Photo https://labs.eemb.ucsb.edu/carlson

4
INTRODUCTION: importance des microorganismes…
Photo: wikimedia
Qu’est-ce qu’on connaît des microorganismes?
Seulement ~10.000 espèces décrites sur +1.000.000
10-20 % de l’ADN sur terre est séquencé.

Examen de la mobilité à l’état frais
- Péritriche: mouvement assez fluide (tous les flagelles vont dans le même sens)
- Polaire: « zig-zag »
- Préparation: lame / lamelle + colonie et vernis autour
Attention aux mouvements browniens (chaleur lampe) – vraie mobilité dans
lorsque déplacements dans plusieurs sens.
Ex. Vibrio sp.
Ex. Pseudomonas sp.
Ex. E. coli
A-Monotriche
B-Lophotriche
C-Amphitriche
D-Péritriche
Mobilité
polaire
Mobilité
péritriche
De nombreux bacilles sont mobiles alors que quelques coques
seulement le sont (ex Enterococcus gallinarum, E. casseliflavus)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%