P2-UE8-Lebarbenchon

UE8- De l’agent infectieux à l’hôte
Camille Lebarbenchon
25 Janvier 2017 8h30-10h30
2016-2017 Camille Lebarbenchon
DEIBER Elodie
RAZAFINDRAMAMBA Ando
EPIDEMIOLOGIE DES MALADIES TRANSMIS-
SIBLES
I- Histoire des épidémies
II- La chaîne de contagion
III-Indicateurs et surveillance
IV- Dynamiques épidémiques!
sur 128

Epidémiologie: science qui étudie, au sein de populations (humaines, animales, végétales), la fréquence et
la répartition des problèmes de santé dans le temps et dans l'espace, ainsi que le rôle des facteurs qui les dé-
terminent.
Maladie transmissible : maladie qui se transmet d'un individu infectieux (qui peut transmettre l'infection) à
un individu qui n'est pas infecté.
Epidémie : développement d'une maladie qui atteint simultanément de nombreux individus repartis sur un
territoire plus ou moins étendu.
Il y a des maladies qui sont non transmissibles qui ont aussi des comportements épidémiques, exemple le
diabète : on peut parler d’épidémie car on a 360 millions de personnes qui souffrent du diabète, on a donc
un impact global au niveau de la population.
Dans le cours, on va rester uniquement sur les maladies transmissibles.
I- Histoire des épidémies
A. Pandémies historiques
Pandémie : épidémie étendue à toute la population d'un continent, voire au monde entier.
Il y a plusieurs pandémies qui ont sévi dans le passé.
Exemple de pandémie : la peste(1ère pandémie qui a lieu vers 5-6 ème siècle), le choléra( 6 grandes pan-
démies ont été répertorié, on a toujours entre 1 et 4 millions de cas d’infection par an dans le monde. On
parle plus de pandémie à l’heure actuelle parce que c’est des foyers épidemiques qui vont être relativement
localisés d’un point de vue géographique, mais il y a toujours des cas de choléra et de peste, ce ne sont pas
des maladies éradiquées, ce sont des maladies qui sévissent à l’heure actuelle), la grippe( 3 grandes pan-
démies de grippe au 20ème siècle: la grippe espagnole en 1918 qui a causé 40 millions de mort, 2 autres
grandes pandémies de grippe en 1947 et en 1958 : grippe de Hong Kong et grippe asiatique), SIDA.
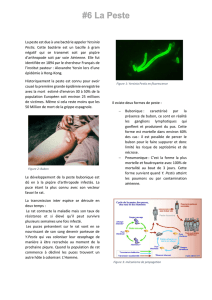
B. La peste"
Généralités:
- La peste peut être une maladie très grave chez l’être humain, avec un taux de létalité de 30 à 60% en l’ab-
sence de traitement. (C’est la maladie la plus mortifère - cad qui a entrainé le plus de mort- dans l’his-
toire).
- On l’a connue sous le nom de peste noire ou de «mort noire» pendant le XIVe siècle, au cours duquel elle
a provoqué 50 millions de morts selon les estimations.
- La peste est une zoonose bactérienne, due à Yersinia pestis qui infecte habituellement les petits animaux
et les puces qui les parasitent.
sur 228

- Les personnes infectées développent des symptômes de type grippal après une période d’incubation de
trois à sept jours.
-Trois formes de peste:
- la peste bubonique (la plus commune)
- septicémique (qui va se propager au niveau du système sanguin et qui va envahir l’ensemble de l’or-
ganisme, en général c’est une peste bubonique qui va se transformer en peste septicémique si jamais
elle est pas traité à temps, au stade avancé on va donc retrouvé la bactérie directement dans le sang)
-et pulmonaire (la forme la plus virulente, là encore c’est une peste bubonique qui va commencer à en-
vahir l’organisme qui va affecter les voies respiratoires, la transmission va pouvoir se faire par l’in-
termédiaire des aérosols, et donc la contamination va pouvoir se faire d’homme à homme, directement
par voie aérienne, c’est une peste qui a un taux de létalité très élevé par rapport à la peste bubonique).
- La forme bubonique, caractérisée par une tuméfaction douloureuse des ganglions lymphatiques appelés
« bubons », est la plus courante.
Mode de transmission : rongeurs qui vont se faire piquer par des puces et ce sont ces puces qui vont aller
contaminer l’homme, donc c’est un agent infectieux zoonotique car le réservoir est animal et on a une
transmission qui va se faire par l’intermédiaire des puces.
Histoire des épidémies de peste
On a très peu d’informations sur la manière dont se déroulait les épidémies, au VIème siècle on n’avait pas
de médias, d’internet, de télé, de radios… donc les seules données sur lesquelles on pouvait se baser pour
comprendre comment ces épidémies fonctionnaient vont être des écrits, et en particulier des écrits religieux,
ici par exemple c’est un évêque qui écrivait un peu ce qui se passait…
Première mention confirmée de la maladie au VIème siècle :
« [...] on compta, un dimanche, dans une basilique de Saint Pierre, trois cents corps morts. La mort était su-
bite ; il naissait dans l’aine ou dans l’aisselle une plaie semblable à la morsure d’un serpent ; et ce venin
agissait tellement sur les hommes qu’ils rendaient l’esprit le lendemain ou le troisième jour ; et la force du
venin leur ôtait entièrement le sens. »
(Grégoire de Tours; Histoire des Francs).
Ce qu’il faut comprendre globalement c’est que vous avez au niveau de l’aine ou de l’aisselle une plaie,
c’est bien ces formes de peste bubonique qui apparaissent, avec une mortalité qui est relativement rapide
puisqu’à partir de 1 à 3 jours les personnes qui étaient contaminées allaient décéder. Finalement c’est un
peu le seul type de témoin qu’on a des épidémies de peste dans l’histoire, on est obligé de se baser sur ce
type d’écrit et vous comprendrez bien que ça pose un problème d’un point de vue scientifique, c’est qu’on ne
quantifie pas les choses et on a des informations qui sont relativement limitées.
Trois grandes pandémies
•Peste de Justinien (VI - VIII ème Siècle) : première épidémie dont Yersinia pestis est confirmé comme
étant l'agent responsable de la maladie. Sévi dans tout le bassin méditerranéen. Pourrait avoir une origine
asiatique (foyer en Asie centrale) et un introduction par l'intermédiaire de la route de la soie.
sur 328

•Peste noire (XIV- XVIII ème siècle) : origine Asiatique, expansion au Moyen-Orient puis en Afrique du
Nord et en Europe. Aurait décimé 30% à 50% de la population européenne en cinq ans. Nombreuses ré-
émergence dans les pays touchés (cad que la maladie a relativement disparu et puis soudainement,
quelques dizaines d’années, elle réapparait au même endroit, donc on a ces phases d’extinction et de ré-
apparition de la maladie pendant toute la durée de l’épidémie). Conséquences multiples sur la
civilisation : économiques, sociales, religieuses et démographiques (car si on perd 50 % de la population
ça va poser un réel problème en terme de structure démographique, en terme de production alimentaire, il
va y a voir une désertification qui va se faire dans les villes mais aussi dans les champs, l’approvisionne-
ment en nourriture va être perturbé, c’est une des premières conséquences, on va finalement voir appa-
raitre des événements de famines qui vont être liées à cette épidémie de peste et au fait qu’on a de moins
en moins de gens dans la population). A cette époque on a aucune idée de l’origine de l’infection, on sait
pas comment les gens tombent malade, on sait pas comment les maladies se transmettent et une des expli-
cations proposées était que cette maladie était un châtiment divin contre les pêchés commis par les hu-
mains.
- Désertification des villes et abandons des villages. Terres arables en friches et expansion des forêts.
- Formation de groupes de flagellants. L'épidémie est interprétée comme un châtiment divin contre les pê-
chés commis par les humains.
- Persécution des juifs, suspectés par la population d'empoisonner les puits et les fontaines.
Peste noire : 50 millions de mort au début de l’épidémie, c’est celle qui a causé l’impact le plus important.
Peste de Marseille (1720)
!
Scène de la peste au quartier de la Tourette. Tableau de Michel Serre (musée Atger, Montpellier)
A Marseille, on a eu environ 40.000 décès sur 90.000 personnes dans la ville
sur 428

•Peste de Chine ( fin XIXè - début XXè siècle) : début de l'épidémie à Hong-Kong en 1894. Se repends
dans le monde entier par l'intermédiaire du développement des moyens de communication (train, bateaux).
Première apparition en Amérique et en Australie. Découverte de la bactérie responsable de la maladie par
Alexandre Yersin en 1894.
La peste aujourd’hui :
Une maladie « ré-émergente »
Quelques chiffres pour dire qu’on n’a plus de pandémies de peste à l’heure actuelle, clairement on n’a plus
une circulation mondiale de la peste mais on a encore des cas, c’est pas du tout une maladie éradiquée si
vous regardez les chiffres sur le site de l’OMS.
Depuis les années 1990 :
-En 2013, 783 cas enregistrés dans le monde, avec 126 décès."
-Epidémies de peste en Afrique, en Asie et en Amérique du Sud principalement.
-Les trois principaux pays d’endémie sont Madagascar, la République démocratique du Congo et le Pérou.
Ce sont 3 foyers de peste qui se maintiennent, on a régulièrement des cas qui vont apparaitre
(zone d’endémie= maladie va se maintenir durablement dans ces zones)
Distribution mondiale des cas de peste. OMS
!
Nombre de cas aux Etats-Unis. CDC
Malgré tout, on a aussi des cas dans des pays de l’hémisphère Nord, aux USA en particulier, on a réguliè-
rement des cas de peste. On ne sait pas vraiment quel est le réservoir de la maladie aux USA, c’est proba-
blement des petits rongeurs comme les écureuils…qui contractent la maladie et la transmettent aussi par
l’intermédiaire des puces soit directement à l’homme, soit par les animaux de compagnies (exemple chien
ou chat)
sur 528
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%