LA CHIMIE ORGANIQUE II-La liaison de covalence (rappels et

LA CHIMIE ORGANIQUE
I- Introduction à la Chimie organique
(activité internet ; revoir polycopié)
La chimie organique est la chimie des composés du carbone d’origines naturelle ou synthétique
Les molécules organiques contiennent principalement les éléments C,H, O, N
(d’autres éléments sont parfois présents: métaux Ca, Mg, Fe, ... ; halogènes F, Cl, Br, I)
II-La liaison de covalence (rappels et compléments)
1) Définition
- Deux atomes liés par covalence simple mettent chacun 1électron de la couche externe en commun :
Les 2électrons en commun forment un doublet liant appartenant aux 2 atomes qui reçoivent
donc chacun un électron : H° °Cl ----> H °° Cl ----> H–Cl
-Une molécule est un assemblage d’atomes liés par covalence
Remarque : les atomes métalliques ont tendance à céder un ou plusieurs électrons donc
ne peuvent pas mettre en commun d’électrons pour former des liaisons de covalence
2) Règles du duet et de l’octet
- Les atomes à Z <= 4 tendent à avoir 2 électrons (duet= doublet) sur leur couche externe
- Les atomes à Z >= 5 tendent à avoir 8 électrons (octet= 4 doublets) sur leur couche externe
3) Nombres de liaisons de covalence d’un atome (non métallique)
C’est le nombre d’électrons manquant à un atome non métallique pour compléter sa couche externe
( et par conséquent c’est aussi le nombre d’électrons externes qu’il va apporter )
1H : (K)1donc 2 - 1 = 1 liaison ou 1 électron liant
6C : (K)2(L)4donc 8 - 4 = 4 liaisons ou 4 électrons liants
4) Formule de Lewis et formule développée d’une molécule
Molécule CH4Cl N
Atomes
Structure
électronique
Nbr d’électrons
externes
Nbr d’électrons
liants ou de liaisons
Nbr
d’électrons
non-liants
1
H
(K)
1
1
2
-
1=1
1
-
1=0
6
C
(K)
2
(L)
4
4
8
-
4=4
4
-
4=0
7
N
(K)
2
(L)
5
5
8
-
5=3
5
-
3=2
17
Cl
(K)
2
(L)
8
(M)
7
7
8
-
7=1
7
-
1=6
Dans la molécule :
Total doublets électroniques : (4x1 + 4 + 5 + 7) / 2 = 10
Total doublets liants(liaisons) :(4 x1 + 4 + 3 + 1) / 2 = 6
Total doublets non liants : (2 + 6) / 2 = 4
La règle de l’octet doit être satisfaite pour chaque atome autre que H (4 doublets)
H H
formule | -formule | _
de Lewis |Cl –C–N–H développée Cl –C–N–H
| | | |
H H H H
Remarques : C tétravalent, N trivalent, O divalent

5) Géométries des liaisons de l’atome de carbone
a) géométrie tétraédrique (carbone tétragonal)
représentation
spatiale
H H la répulsion minimale entre les
Idoublets conduit à une structure
méthane H - C –H C tétraèdrique régulière avec des
CH4|H H angles entre liaisons de 109°
H H ___ liaison dans le plan
---- liaison en arrière
liaison en avant
H H
éthane I I
C2H6H–C - C - H 2 conformations de l’éthane
I I (parmi une infinité) du fait
H H de la libre rotation de chaque
groupe CH3autour de l’axe
de la liaison CC.
b) géométrie plane (carbone trigonal)
éthène H H La répulsion minimale entre les doublets conduit
(éthylène) C = C à une molécule plane avec des angles entre
C2H4H H liaisons de 120°. La double liaison C = C
bloque la libre rotation autour de l’axe CC
c) géométrie linéaire (carbone digonal)
Une triple liaison s’établit entre les atomes C
éthyne H - C C - H la répulsion minimale entre les doublets
(acétylène) conduit à une molécule linéaire
C2H2
Exercices : 7, 10, 11, 12, 14, 15, (16,17) page 147
III-Le squelette carboné d’ une molécule
1) Les divers squelettes carbonés
Le squelette carboné (ou chaîne carbonée ) est l’enchaînement des atomes de carbone constituant une
molécule organique.
Les différentes structures de squelettes carbonés :
Les molécules à chaîne ouverte qui ne contiennent pas de « boucles » ou cycles
Les molécules cycliques
Les molécules linéaires qui ne comportent qu’une seule chaîne ouverte)
Les molécules ramifiées dont le squelette carboné comprend au moins deux chaînes ouvertes
( la chaîne principale étant la chaîne ouverte la plus longue)
Les molécules saturées ne contenant que des liaisons carbone-carbone simples .
(une molécule est insaturée si au moins une de ses liaisons carbone-carbone est double ou triple)

Remarque : On utilise parfois l’écriture topologique des molécules pour rendre compte de la chaîne
carbonée ; on écrit la chaîne carbonée sous forme d’une ligne en zig-zag et on n’écrit pas les
atomes de carbone et d’hydrogène .
Exercices : 4, 5, 6, 8 pages 166 et 167
2) L’isomérie de constitution
Deux molécules isomères de constitution ont la même formule brute mais une chaîne carbonée
différente. Il faut donc adopter une nomenclature qui permette de nommer de façon unique et sans
équivoque une molécule donnée et de la différencier des molécules isomères :
Le nom d’une molécule de la chimie organique est basé:
Sur la structure de son squelette carboné
Sur la longueur de sa chaîne principale
Exercice : 7 page 167
IV- La famille des hydrocarbures :
1) Les alcanes
En complément sur l’étude documentaire faite en TP
a) Généralités
Les alcanes sont des hydrocarbures dans lesquels toutes les liaisons sont des liaisons simples.
On dit que ce sont des hydrocarbures saturés. Leur formule brute générale est CnH2n+2.
Les huit premiers alcanes linéaires ( à connaître par cœur )
méthane ; éthane ; propane ; butane ; pentane ; hexane ; heptane ; octane
CH4C2H6C3H8C4H10 C5H12 C6H14 C7H16 C8H18
Isomères de constitution et nomenclature
Lorsque deux alcanes ont la même formule brute, mais une formule développée différente, ils sont
isomères de constitution. (Les chaînes carbonées présentent alors des ramifications)
Règles de nomenclature :
La chaîne carbonée la plus longue impose son nom à l’alcane
Le(s) nom(s) des groupes alkyles greffés sur cette chaîne principale sont indiqués en préfixe
( par ordre alphabétique, en enlevant le e).
principaux groupes alkyles :
- CH3:méthyle ; -C2H5:éthyle ; -CH2-CH2-CH3:propyle
-CH2-CH2-CH2-CH3:butyle ; - CH(CH3)-CH3:isopropyle
L’emplacement du groupe alkyle est repéré en numérotant la chaîne carbonée principale, afin
d’affecter le plus petitnombre au carbone portant le groupe. Le nombre est placé devant le nom
du groupe alkyle correspondant.
S’il y a plusieurs groupes alkyles identiques, on l’indique avec le préfixe di-, tri- ou tétra-
devant le nom du groupe.
Remarque : Les cyclanes sont des alcanes à chaîne non ouverte ( cyclique ) ; leur formule brute
générale est CnH2n et leur nom est obtenu en mettant le préfixe cyclo- devant le nom de l’alcane
correspondant
cyclohexane :
formule brute : C6H12 ; semi-développée : ; topologique
Exercices : 9 (a-b-c-d) ; 10(a-b-e) ; 11(a-b) page 167
CH
2
–
CH
2
CH2CH2
CH
2
–
CH
2

b) Propriétés physiques :
États physiques des alcanes
Pour les alcanes linéaires, quand la longueur de la chaîne carbonée augmente, les températures de
fusion et d’ébullition des alcanes augmentent.
A température ambiante , les alcanes sont gazeux de n = 1 à 4, liquides de n = 5 à 20, solides au-delà.
Un alcane linéaire a une température d’ébullition plus élevée que ses isomères ramifiés.
Exercices :Températures d’ébullition: 24 page 169
Distillation d’un mélange d’alcanes: 25 page 169
Marées noires : 26 page 169
Solubilité et densité
Les alcanes sont solubles entre eux et non miscibles dans l’eau.
Les alcanes sont moins denses que l’eau ( d<1); la densité augmente avec le nombre de carbones.
Combustion des alcanes :
- Écrire l’équation de combustion complète du butane dans le dioxygène:
C4H10 +
13
2
O24 CO2+ 5 H2O
2 C4H10 + 13 O28 CO2+ 10 H2O
- Déterminer
Volume dioxygène
Volume butane
dans l’état initial afin que les réactifs réagissent totalement :
Pour un gaz la qt de matière est proportionnelle au volume (V = n.Vm)
donc dans les proportions stœchiométriques (réaction totale):
n(O2)/n(C4H10) = V(O2)/V(C4H10) = 13 / 2 = 6,5
(gaz introduits dans une éprouvette par déplacement d’eau)
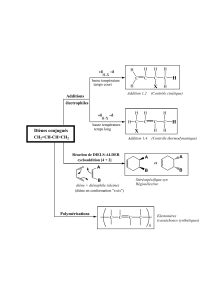
c) Généralités
Les dérivés éthyléniques
sont des hydrocarbures à chaîne ouverte insaturée, comportant au moins une
liaison double ( ex : le butadiène qui est à la base de la fabrication de caoutchoucs synthétiques )
Les alcènes
sont des hydrocarbures à chaîne ouverte insaturée, comportant une seule liaison double.
Leur formule brute générale est CnH2n. ( ex : l’éthène ou éthylène C2H4qui est à la base de
nombreuses synthèses industrielles )
d) Nomenclature
La nomenclature des alcènes se déduit de celle des alcanes en remplaçant le suffixe –ane par -ène .
À partir de n = 4 ( butène), il faut indiquer la place de la double liaison. On le fait de façon à attribuer
aux atomes de carbone portant la double liaison les plus petits numéros.
e) Stéréoisomérie
Deux alcènes qui possèdent des formules
brutes et semi-développées identiques, mais
des formules développées différentes sont
appelés des stéréo isomères.
Ils se différencient par la position
respective des groupes situés de part et
d’autre de la double liaison.
f) test caractéristique d’une molécule insaturée
L’eau de dibrome, de couleur jaune orangée, se décolore en présence d’une molécule insaturée ( voir le
chapitre suivant )
Exercices : Nomenclature : 9(e), 10(c-d), 11( c-d) page 167
Stéréoisomérie : 12 page 168
C
HH
C
A B ATTENTION :
les groupes A et
B ne sont pas
des atomes
d’hydrogène
Stéréoisomère Z :« Zusammen »
les groupes A et B sont situés du
même coté de la double liaison
Stéréoisomère E :« Entgegen »
les groupes A et B sont situés du
même coté de la double liaison
C
B
H
C
AH
butane
eau
dioxygène
détonation

V- Modification du squelette carboné
1) La chimie du pétrole
(lire page 174 du livre)
Raffinage:
- distillation du pétrole : séparation grossière des hydrocarbures en fonction de leurs
températures d’ébullition et de leurs densités (gaz, essences légères et lourdes, huiles,
paraffines, bitume)
-craquage et réformage des hydrocarbures
2) Procédés de modification du squelette carboné
(lire pages 175-178 du livre)
a) Craquage thermique (400-800°C) : On casse la molécule
R–CH2–CH2–CH2–R’ CH2= CH –CH3+ R –R’ (R = groupe alkyle)
(Vapeur d’eau)
CH3–CH2–CH2–CH32 CH2= CH2+ H2(vapocraquage)
b) Réformage : On modifie l’enchainement des atomes de carbone
CH2–CH2
R- CH2–CH2–CH2–CH2–CH2-R’ R–CH | + R’ –H(cyclisation)
CH2–CH2
R- CH2–CH2–CH2–CH2–CH2-R’ R- CH2–CH –CH2–CH2-R’(isomérisation)
|
(benzène) CH3
(hexane)
+4 H2(déshydrocyclisation)
C6H14 C6H6
c) Polyaddition ou polymérisation : On allonge la chaine carbonée
... + CH2= CH + CH2= CH + ... ... - CH2–CH –CH2- CH - ...
| | | |
R R R R
n additions entre monomères polymère
n = indice de polymérisation (103à 106)
exemples : polyéthylène (PE) avec R: H ; polypropylène (PP) avec R : CH3
polystyrène (PS) avec R : C6H5(phényle)
polychlorure de vinyle (PVC) avec R = Cl
polytétrafluoréthylène (téflon) avec monomère CF2= CF2
 6
6
 7
7
1
/
7
100%