Document

Organisation des enseignements Chimie
en S3 et S4
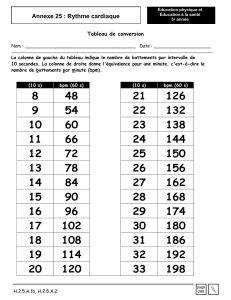
● Modules d'enseignements de Chimie
►M3303 : Techniques Spectroscopiques (Johan ALAUZUN S3)
►M4104 : Analyses Électrochimiques (Olivier FONTAINE fin S3) et Méthodes
Chromatographiques (Christelle NGUEFACK début S3)
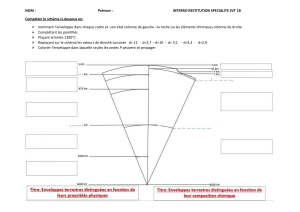
● Organisation des TP (bâtiment H Chimie, RDC)
►Responsables TP : Stella LACOUR (stella.lacour-cartier@umontpellier.fr) puis Olivier
FONTAINE
►Fonctionnement en groupes TP, séance une semaine sur 2 pour chaque groupe TP voir
l'EDT
►Série 1 'Spectro/Chromato' : 4 TP tournants (4h) puis 1 partiel pratique de 2h /étudiant
démarrage début S3 (amener blouse/lunettes/propipette)
►Série 2 'Électrochimie' : 4 TP tournants (4h) puis 1 partiel pratique de 2h /étudiant
milieu S3 et début S4.

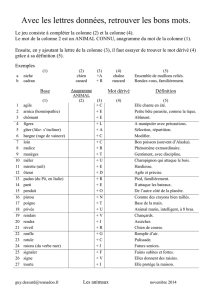
Chromatographie = séparation, identification et dosage des constituants
chimiques d'un mélange complexe
→ Analyse qualitative et quantitative
Autres méthodes
9%
RMN
7%
UV-Visible
7%
HPLC 30%
CPG 17%
Autres méthodes
chromatographiques
5%
Spectrométrie de
masse
14%
Infra-rouge
11%
INTRODUCTION AUX METHODES CHROMATOGRAPHIQUES

I. Aspects Généraux
1- Principe de la Chromatographie
A + B BAB
A
A
B
B
Phase Mobile = Eluant
Détecteur
Phase Stationnaire
Chromatogramme
t0t1t2t3t4
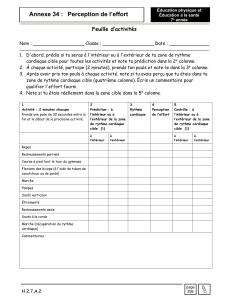
Un chromatogramme est caractérisé par :
La position des pics Facteurs de Rétention
La largeur des pics Facteurs de Résolution

2- Facteurs de Rétention
S phase mobile S phase stationnaire
KNernst = Cm
Cs =Conc. du soluté dans la phase stationnaire
Conc. du soluté dans la phase mobile
= Coefficient de distribution de Nernst
tM = temps mort ou temps nécessaire pour
qu’un soluté non retenu traverse la colonne
tR = temps de rétention idéal
t’R = temps de rétention réel = tR - tM
k = tR - tM
tM
t’R
=tM
kA==kB
t’RA
t’RB
Facteur de Rétention k Facteur de Séparation

3- Facteurs de Résolution
a) Efficacité d’une colonne : Modèle des plateaux
L : longueur de la colonne,
N : nombre de plateaux théoriques
H : hauteur équivalente à un plateau théorique (HEPT)
H = L
N
N = 16 = 5.54
tRtR
tR , et en unité de temps.
: largeur du pic à sa base,
: largeur du pic à mi-hauteur.
( ( ))
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
1
/
31
100%