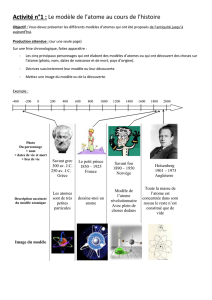
Les niveaux d`énergie dans les atomes à plusieurs électrons

10
L’atome et les échanges d’énergie entre l’atome et l’extérieur
I - les niveaux d’énergie de l’atome d’Hydrogène
→ Analogie entre le système terre/corps, pesanteur et l’atome
Système terre/corps pesant
Système noyau électrons (atome)
Force de gravitation
Attraction coulombienne
Il faut apporter de l’énergie pour soulever
un corps pesant car son énergie Potentielle
augmente
Apport d’énergie pour éloigné l’électron du
noyau
Un corps qui tombe dégage de l’énergie
Quand un électron se rapproche du noyau
de l’énergie s’en dégage
On observe que pour des échanges d’énergie : le niveau zéro de l’énergie est arbitraire
On choisit le niveau zéro de l’énergie quand
l’électron est très éloigné du noyau
Remarque il s’agit d’une analogie simpliste, cela tient compte que de l’énergie potentielle et
jamais de l’énergie cinétique, mais cela ne change rien qualitativement.
Noyau + électrons → atome : libération
d’énergie
Atome → noyau + électrons (séparés),
absorption d’énergie.
= E de liaison (ou d’ionisation) :
énergie nécessaire pour arracher un
électron ou énergie libérée quand
l’électron arrive.

11
Electrons peu lié → électrons plus lié, quand départ d’énergie (E1)
Electrons lié → électrons peu lié, quand apport d’énergie (E2)
→ Cette énergie correspond à l’énergie d’excitation :
Le niveau d’énergie zéro
→ choisi arbitrairement
→ E(noyau + électrons séparés)=0
→ L’énergie de l’atome est donc négative.
La quantification de l’énergie
→ On a découvert que l’énergie du système noyau/électrons est quantifiée cad que la
formule donnant sa valeur fait intervenir des nombres entiers.
→ L’énergie pour un électron dépend de 4 nombre entiers :
n = nombre quantique principale (forte dépendance), détermine le nombre de
couches
l = nombre quantique orbitale (faible dépendance) l détermine la sous-couche
m = nombre quantique magnétique (dans certaines circonstances)
s= nombre quantique de spin (dans certaines circonstances)
→ Pour l’atome d’hydrogène en ne tenant compte que de n :
E(n)ev= - 13.6
n
1
2
3
4
…
infini
Couche
K
L
M
N
Energie
-13.6
-3.4
-1.5
-0.85
0
Position de
l’électron
proche
éloigné
infini
Etat
fondamental
excité
excité
excité
excité
ionisé

12
Position possible pour les électrons
II -Les niveaux d’énergie dans les atomes à plusieurs électrons
→ Z= nombre atomique = nombre de charge du noyau
→ E(Z,n)= énergie d’un électron sur une couche au nombre quantique principal n
→ Cette formule est approximative voire fausse.
→Même postions relatives des niveaux d’énergie que pour H mais les valeurs peuvent être
très différentes.
n=1
n=2
n=3
n=4
H
Z=1
-13.6
-3.4
-1.5
-0.85
Ca
Z=20
-5442
-1360
-604
-340
W
Z=74
-74504
-18626
-8278
-4656

13
Pourquoi ces exemples ?
H : un des 4 éléments de la matière organique
Ca le plus abondant des éléments non légers, présents dans l’os
Tungstène : utilisé dans la plupart des tubes à rayons X
Importance des nombres quantiques en chimie
→ Les électrons se répartissent sur les couches et les sous-couches en fonctions du principe
de Pauli. Ceci est essentiel pour comprendre la classification et les propriétés chimiques des
éléments.
III- les transmissions entre les niveaux d’énergie et l’atome
1- Absorption d’énergie par un atome
L’excitation de l’atome
Energie absorbée = , en valeur absolue pour éviter les problèmes de signes.
Les différentes origines de l’énergie apportée à un atome
Photon
Energie cinétique d’un autre sous l’effet de l’agitation thermique
Choc par une particule chargée.

14
L’absorption d’un photon par un atome
hf= Il faut que hf doit parfaitement
égale au niveau d’énergie nécessaire d’un électron
pour l’excité.
Ionisation d’un atome
E absorbé=
L’ionisation d’un atome par un photon (=effet photoélectrique)
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%