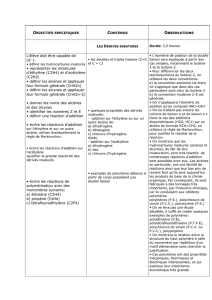
A3 - Du pétrole à la glycérine et au PVC

Document d’accompagnement – Chimie / classe de première S © CNDP
La chimie créatrice
A3
Du pétrole à la glycérine et au PVC
Objectifs
• Reconnaître des groupes caractéristiques.
• Utiliser à bon escient les termes addition, substitution, élimination.
• Se familiariser avec l'écriture topologique des molécules.
• Écrire l'équation d'une réaction de polyaddition.
À propos de la glycérine
Pendant des années, la production de glycérine a été également répartie entre glycérine naturelle
(provenant de la saponification des graisses) et glycérine synthétique. La diminution de la production
du savon a imposé une augmentation de la production en glycérine de synthèse. La glycérine est
utilisée dans l'industrie alimentaire et pharmaceutique, dans les industries du tabac, des
cosmétiques et des peintures (résines
glycérophtaliques) comme agent humectant, lubrifiant et/ou épaississant. Le trinitrate de glycérine
est un explosif puissant : la nitroglycérine ; très sensible aux chocs, la nitroglycérine est “ diluée ”
avec une terre siliceuse ou de la sciure de bois (dynamite).
Synthèse : procédé Shell, à partir du propène
Schéma de la synthèse en quatre étapes :
A
Cl
B
Cl Cl
OH
C
Cl2,
Cl
D
OOH OH
OH
E : glycérine
HOCl base NaOH/H2O
Questionnement possible
À partir du schéma de synthèse proposé :
1. Donner les formules semi-développées planes et les formules brutes des composés A à E.
2. À quelle famille de composé appartiennent les composés A et B ?
3. Entourer les groupes caractéristiques et les nommer dans les molécules B et E.
4. Expliquer par une phrase comment on passe de A à B, de B à C, de C à D et de D à E en
employant le terme approprié : addition, substitution ou élimination.
5. Rechercher comment est synthétisé le propène (matière première et mise en œuvre) ?
À propos du PVC
Le polychlorure de vinyle est un polymère très utilisé dont les principales applications sont : tuyaux,
profilés pour fenêtres, gainages de fils, blisters pharmaceutiques, etc.). Le chlorure de vinyle
(chloroéthène) peut subir une polymérisation analogue à celle que subit l'éthylène.
Synthèse du chlorure de vinyle à partir de l'éthylène

Document d’accompagnement – Chimie / classe de première S © CNDP
Le chloroethène, appelé aussi chlorure de vinyle, est obtenu à partir de l'éthylène (ou éthène) en
deux étapes :
– la première est la réaction de l'éthylène sur du chlorure d'hydrogène et du dioxygène, appelée
oxychloration de l'éthylène. Il se forme majoritairement du 1,2-dichloroéthane et de l'eau, mais il est
possible d'effectuer la chloration directe de l'éthylène ;
– la seconde est la décomposition par la chaleur (pyrolyse) du 1,2-dichloroéthène qui produit du
chloroéthène et du chlorure d'hydrogène.
Questionnement possible
1. Écrire les formules topologiques puis développées des différentes molécules organiques citées
dans cette synthèse.
2. Indiquer s'il s'agit d'une addition ou d'une élimination.
3. Par analogie avec le schéma de polymérisation de l'éthylène, donner le motif du polychlorure de
vinyle. Schéma de la polymérisation de l'éthylène
C C
H
HH
H
C
H
H
C
H
Hn
C
H
H
C
H
H
n
représente le motif du polyéthylène :
groupement d'atomes qui se répètent un grand nombre de
fois (n fois) pour donner un polymère (ou macromolécule).
Commentaire
Signaler qu'en chimie organique, on indique souvent, au-dessus de la flèche de transformation
A B, les conditions expérimentales : réactifs utilisés, chauffage (symbolisé par , etc.
1
/
2
100%