Le système des carbonates dans l`océan

L’altération des roches Thème : L’ eau
Chap. 1 Eau et environnement
ASDS : Les différents types d’érosion / Le système des carbonates 1 C.Grange-Reynas
L’altération des roches - CORRECTION
Mots-clefs : Erosion ; dissolution ; concrétion.
Contexte du sujet :
Le climat a fortement évolué depuis la formation de la Terre.
Comment l’altération des roches par l’eau peut-elle modifier le climat à l’échelle des temps géologiques ?
ANALYSE ET SYNTHESE DE DOCUMENTS SCIENTIFIQUES
Les différents types d’érosion
Le système des carbonates dans l’océan
L’érosion est le phénomène par lequel la surface du sol se transforme.
À l’échelle de temps géologique, la pluie et le vent suffisent à araser les plus hautes montagnes. Toute la matière les
constituant se trouve ainsi progressivement transportée. L’altérabilité du sol dépend de sa nature chimique de son
état de surface (lisse, il résiste mieux qu’une concrétion friable et trouée), et du type d’érosion auquel il est soumis
(tableau ci-dessous).
Une concrétion est une réunion de différents corps qui se solidifient ensemble.
Érosion
Agent
Effet de l’érosion
Facteur aggravant
Mécanique
vent, eau liquide, glace
sol entrainé
force du vent, pente de
ruissellement
Chimique
eau
dissolution du sol
pH, température
Biochimique
animaux, végétaux,
bactéries
échange de matière entre le sol et les
organismes vivants
densité et activité des
organismes vivants
1/ L’érosion est-elle un phénomène naturel ou anthropique (causé par l’homme) ?
Il s’agit essentiellement d’un phénomène naturel, au départ, mais influencé tout de même par l’activité humaine
(pluies acides, effet de serre, …).
Document 1 : L’altération des roches
Certaines formations géologiques sont dues à l’altération des roches (érosion). C’est par exemple le cas des karsts,
structures géologiques formées par dissolution des roches calcaires au contact d’une eau riche en dioxyde de
carbone : CaCO3 (s) + CO2 (g) + H2O (l) = Ca2+ (aq) + 2 HCO3- (aq)
L’érosion d’un basalte conduit à l’altération de l’anorthite
(minéral silicaté) en kaolinite. Cette érosion consomme elle
aussi du dioxyde de carbone : CaAl2Si2O8 (s) + 2 CO2 (g) +
3H2O (l) = Al2Si2O5(OH)4 (s) + Ca2+ + 2HCO3- (aq)
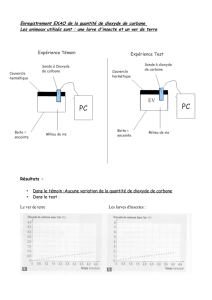
Les ions et minéraux produits sont conduits, grâce aux
rivières, dans l’océan. Les ions Ca2+ et HCO3- s’accumulent
dans l’eau de mer et précipitent dès que la limite de
solubilité du carbonate de calcium est atteinte. Cette
précipitation s’accompagne d’une libération de dioxyde de
carbone. (Voir ci-contre)
L’érosion des roches sur les continents et la précipitation
des ions carbonate dans l’océan s’opposent donc en
termes de bilan d’espèces chimiques produites et
consommées.
Ca2+ (aq) + 2 HCO3- (aq) →
CaCO3 (s) + CO2 (g) + H2O (l)

L’altération des roches Thème : L’ eau
Chap. 1 Eau et environnement
ASDS : Les différents types d’érosion / Le système des carbonates 2 C.Grange-Reynas
La limite de solubilité d’une espèce est la concentration à partir de laquelle cette espèce ne se dissout plus dans
l’eau. Cette limite dépend de la température.
1. En raisonnant sur les équations de réactions, faire le bilan de la quantité de dioxyde de carbone consommée
ou produite dans le cas de l’érosion continentale de calcaire suivie de la précipitation dans l’océan des ions
carbonate.
Bilan du carbone dans le cas de l’érosion continentale du calcaire suivie de la précipitation dans l’océan.
Dissolution du calcaire : CaCO3(s) + CO2(g) + H2O(l) Ca2+(aq) + 2 HCO3-(aq)
Précipitation des carbonates : Ca2+(aq) + 2 HCO3-(aq) CaCO3(s) + CO2(g) + H2O(l)
La dissolution consomme 1 mole de CO2, la précipitation en produit 1 mole. Le bilan est donc nul.
2. Réaliser de même le bilan de la quantité de dioxyde de carbone consommée ou produite dans le cas de
l’érosion continentale de basalte, riche en anorthite, suivie de la précipitation dans l’océan des ions
carbonate.
Bilan du carbone dans le cas de l’érosion continentale du basalte suivie de la précipitation dans l’océan.
Altération des silicates : CaAl2Si2O8(s) + 2 CO2(g) + 3 H2O(l) Al2Si2O5(OH)4(s) + Ca2+(aq)+ 2 HCO3-(aq)
Précipitation des carbonates : Ca2+(aq) + 2 HCO3
-(aq) CaCO3(s) + CO2(g) + H2O(l)
L’altération consomme 2 moles de CO2, la précipitation en produit 1 mole. Le bilan est donc négatif : l’altération
chimique des silicates consomme deux fois plus de dioxyde de carbone de l’atmosphère que la précipitation du
calcaire n’en libère dans l’océan.
3. Laquelle de ces deux érosions influe le plus sur la teneur en dioxyde de carbone dans l’atmosphère ?
L’altération des silicates influence directement les variations de la teneur en dioxyde de carbone atmosphérique. Sur
l’échelle des temps géologiques, il faut donc considérer ce phénomène comme essentiel pour expliquer la diminution
en dioxyde de carbone atmosphérique. Le dioxyde de carbone atmosphérique se retrouve aujourd’hui « séquestré »
dans le carbone lithosphérique (calcaire).
Document 2 : L’érosion par l’eau en milieu désertique.
Contrairement aux idées reçues, les milieux désertiques ne sont pas à l’abri
de l’érosion par l’eau. Comment l’eau peut-elle sculpter des paysages
arides ?
Dans les milieux désertiques, les rares précipitations sont brèves et
particulièrement fortes (plus de 1 mm/min).
Le ruissellement de l’eau sur les roches est donc très intense ; l’eau charrie
alors les matériaux et érode le sol. Par ailleurs, en l’absence de couverture
végétale, les gouttes de pluie ne sont pas ralenties et possèdent une énergie
cinétique suffisante pour désagréger le sol. En tombant, les gouttes
projettent en l’air les éléments les plus fins, tout en déchaussant les éléments
les plus gros (on parle d’effet Splash). Ces derniers sont ensuite entraînés par
le ruissellement de l’eau.
La glace constitue également un agent érosif dans les milieux désertiques. En saison froide, les températures
peuvent être basses et le gel fragmente la roche : on parle alors de cryoclastie (ou de gélifraction). Ce phénomène
résulte soit d’une différence thermique entre les températures diurnes et nocturnes, soit du gel de l’eau présente
dans les fissures.

L’altération des roches Thème : L’ eau
Chap. 1 Eau et environnement
ASDS : Les différents types d’érosion / Le système des carbonates 3 C.Grange-Reynas
Les pluies sont classées suivant leur intensité I, qui correspond
à la hauteur d’eau précipitée par unité de temps :
I = h
t
,
avec h en mm, t en h et I en mm/h.
Exemples
Pluie faible
I < 3 mm/h
Pluie modérée
3 mm/h < I < 8 mm/h
Pluie forte
I > 8 mm/h
1. Quels sont les deux principaux agents érosifs en milieu désertique ? Ce sont les pluies et la glace.
2. Quelle forme d’énergie possèdent les gouttes d’eau en touchant le sol ?
Elles possèdent de l’énergie cinétique : Ec = ½ m v2.
3. Expliquer pourquoi les pluies en milieu désertique sont qualifiées de « pluies fortes ».
I = h / t = 1 / (1 / 60) = 60 mm / h > 8, donc on peut les qualifier de « pluies fortes ».
4. Quel changement d’état de l’eau intervient lors du phénomène de cryoclastie ? Il s’agit de la solidification.
5. La densité de la glace étant plus faible que celle de l’eau liquide, comment évolue le volume de l’eau
lorsqu’elle gèle ?
ρglace < ρeau. Soit pour une même masse d’eau, vglace = m / ρglace > veau = m / ρeau.
Il y a donc augmentation du volume lorsque l’eau gèle.
6. En quoi ce phénomène contribue-t-il à l’érosion de la roche ?
L’eau liquide s’infiltre dans les fissures, et lorsque les températures chutent, elle gèle, prend plus de place, ce
qui provoque l’éclatement de la roche.
Document 3 : Le système des carbonates dans l'océan
Dissolution du dioxyde de carbone dans l’océan.
Du fait de l’activité humaine, la concentration atmosphérique en dioxyde de carbone
CO2
atm
augmente. Une grande
partie est piégée dans les océans. Le flux de dioxyde de carbone entre l’eau et l’atmosphère dépend de la différence
entre la pression du dioxyde de carbone atmosphérique (
PCO2
atm
) et celle dans l’eau de mer (
PCO2
océan
). On dit que
l’état d’équilibre est atteint lorsque
PCO2
atm
=
PCO2
océan
.
Le dioxyde de carbone atmosphérique
CO2
atm
se dissout dans les océans et devient l’acide carbonique CO2,H2O(aq).
La solubilité du dioxyde de carbone dans l’eau de mer diminue lorsque la température augmente ou lorsque la
pression
PCO2
atm
du dioxyde de carbone dans l’air diminue.
Ainsi, les eaux froides de l’Atlantique Nord ont tendance à absorber du dioxyde de carbone ; puis, lorsque ces eaux
refont surface dans les eaux chaudes du Pacifique et de l’océan Indien, grâce à la circulation thermohaline, elles ont
tendance à le libérer dans l’atmosphère.
Différents équilibre acido-basiques dans l’océan.
L’acide carbonique CO2, H2O(aq) dissout, réagit avec l’eau, car il est l’acide du couple
CO2, H2O(aq) / HCO3- (aq). L’ion hydrogénocarbonate ainsi formé réagit à son tour avec l’eau,
car il est l’acide du couple HCO3- (aq) / CO32- (aq). L’acide carbonique en excès, quand
PCO2
atm
augmente, et l’ion carbonate réagissent ensemble selon un autre équilibre chimique.
Les constantes d’acidité des 2 premiers couples sont respectivement :
KA1 = HCO3
——(aq)
é
ëù
ûéqH3O+(aq)
é
ëù
ûéq
CO2, H2O(aq)
é
ëù
ûéq
= 1,4 x 10—6 ;
KA2 = CO3
2—(aq)
é
ëù
ûéqH3O+(aq)
é
ëù
ûéq
HCO3
—— (aq)
é
ëù
ûéq
= 1,2 x 10—9.
Le pH de l’océan est voisin de 8,0.

L’altération des roches Thème : L’ eau
Chap. 1 Eau et environnement
ASDS : Les différents types d’érosion / Le système des carbonates 4 C.Grange-Reynas
La croissance des coraux dans l’océan.
Les coraux fabriquent leur squelette à partir des ions carbonate CO32- (aq) et calcium Ca2+ (aq), dissous dans l’eau de
mer, selon la réaction d’équation : CO32- (aq) + Ca2+ (aq) CaCO3 (s)
Ce solide se forme si, dans l’eau de mer, [CO32- (aq)] [Ca2+ (aq)] ≥ 4,47 x 10—7.
Dans les océans, la concentration [Ca2+ (aq)] peut être considérée comme constante.
Aide : formulaire du manuel TS spécifique Bordas page 333.
1. Comment varie la concentration en gaz carbonique dans l’eau *CO2, H2O(aq)], si la pression de ce gaz
PCO2
atm
augmente dans l’atmosphère ?
Si
PCO2
atm
augmente, alors [CO2, H2O(aq)] augmente dans les eaux froides.
Mais si
PCO2
atm
augmente, les eaux chaudes rejettent alors moins de CO2 dans l’atmosphère, car
PCO2
atm
=
PCO2
océan
puisque qu’il s’établit un état d’équilibre.
Ainsi, dans tous les océans, [CO2, H2O(aq)] augmente : ils stockent donc le CO2.
2. Ecrire les deux demi-équations acido-basiques, puis l’équation-bilan correspondant à la réaction entre l’acide
carbonique et l’eau.
CO2, H2O(aq) / HCO3
- (aq) CO2, H2O(aq) HCO3
- (aq) + H+(aq)
H3O+(aq) / H2O(l) H2O(l) + H+ H3O+ (aq)
CO2, H2O(aq) + H2O(l) HCO3- (aq) + H3O+ (aq)

L’altération des roches Thème : L’ eau
Chap. 1 Eau et environnement
ASDS : Les différents types d’érosion / Le système des carbonates 5 C.Grange-Reynas
3. Ecrire les deux demi-équations acido-basiques, puis l’équation-bilan correspondant à la réaction entre l’ion
hydrogénocarbonate et l’eau.
HCO3- (aq) / CO32- (aq) HCO3- (aq) CO32- (aq) + H+(aq)
H3O+(aq) / H2O(l) H2O(l) + H+ H3O+ (aq)
HCO3- (aq) + H2O(l) CO32- (aq) + H3O+ (aq)
4. Calculer les pKA des 2 couples acido-basiques.
pKA1 = - log KA1 = - log (3,98.10-7) = 6,4 et pKA2 = - log KA2 = - log (5,01.10-11) = 10,3
5. Tracer un axe pH sur lequel apparaissent les valeurs des pKA et les domaines où les espèces conjuguées
prédominent.
6. Quelle espèce dissoute, parmi les 3 précédentes, prédomine dans les océans ?
A pH = 8,0, c’est l’ion hydrogénocarbonate HCO3-(aq).
7. Déduire l’équation-bilan de la réaction qui a lieu entre CO2, H2O(aq) en excès et CO32-(aq).
CO2, H2O(aq) / HCO3- (aq) CO2, H2O(aq) HCO3- (aq) + H+(aq)
HCO3
- (aq) / CO3
2- (aq) CO3
2- (aq) + H+(aq) HCO3
- (aq)
CO2, H2O(aq) + CO32- (aq) 2 HCO3- (aq)
8. Quel est l’effet d’une augmentation importante de la concentration en dioxyde de carbone de l’atmosphère
PCO2
atm
sur le squelette des coraux ?
Si
PCO2
atm
augmente, [CO2, H2O(aq)] augmente, donc il y a davantage de CO2, H2O(aq) en excès ; la réaction vue en 7/
montre alors que la quantité et donc la concentration en ions carbonate [CO32- (aq)] dans les océans diminue ;
comme [Ca2+(aq)], est constante, le produit [CO3
2- (aq)][ Ca2+(aq)] peut devenir inférieur à 4,47 x 10—7. L’équilibre
CaCO3 (s) CO32- (aq) + Ca2+ (aq) se déplace à droite, et le solide CaCO3 (s), et donc les coraux, sont détruits.
L’acidification des océans, conséquence des activités humaines, va inévitablement entrainer de grands changements
de la géochimie océanique et un remodelage de la biodiversité marine. Ainsi, il y a risque d’une disparition
importante, voire totale, d’organismes calcaires (certains coraux par exemple). Des impacts plus lourds sont à
craindre car les coraux habitent des écosystèmes marins uniques et d’autres espèces dépendantes du corail risquent
de disparaitre.
16/ Que penser des conséquences de l’activité humaine sur la planète ?
Elles pourraient être désastreuses au niveau de la faune et de la flore marine notamment.
 6
6
1
/
6
100%