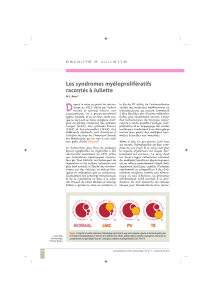
L`homozygotie de la mutation JAK2 facteur de risque de thrombose

Hématologie, vol. 13, n° 4, juillet-août 2007
226
Actualités cliniques
L’homozygotie de la mutation JAK2 facteur de risque
de thrombose et de myélofi brose dans la maladie de Vaquez
et la thrombocytémie essentielle
Régis COSTELLO
La mise en évidence des muta-
tions de JAK2 617V>F a modi-
fié l’approche diagnostique des
syndromes myéloprolifératifs Phi-
ladelphie-négatif. Elle est décelée
à l’état homozygote chez 25 à 30 %
des patients atteints de maladie de
Vaquez (PV) et 2 à 4 % des patients
atteints de thrombocythémie essen-
tielle (TE). L’une des questions
essentielles qui se pose au clinicien,
lors du diagnostic de PV ou de TE,
est l’évaluation du risque évolutif,
en particulier celui concernant les
événements thrombotiques mais
aussi la myélofibrose.
Une étude italienne [1] apporte un
début de réponse à ces questions. Il
s’agit d’une étude rétrospective et
multicentrique, ce qui permet aux
auteurs d’analyser une population
importante de 118 patients homo-
zygotes pour la mutation JAK2
617V>F et de 587 patients hétéro-
zygotes pour cette même mutation.
Par la seule distinction homozygotie/
hétérozygotie, les auteurs mettent en
l’imatinib pour l’hydroxyurée. Dans
les trois autres cas, compte tenu
d’une hyperleucocytose importante,
une LMC a d’emblée été évoquée et
confirmée par cytogénétique et/ou
biologie moléculaire.
Si les observations rapportées par
Inami et al. [3] et par Krämer et al.
[4] présentaient des éléments peu
habituels (hématocrite à 49 % dans le
premier cas, fibrose médullaire dans
le second), celle de Hussein [5] est
une présentation classique de LMC
accélérée. C’est sur une évolution
hématologique inhabituelle, malgré
un traitement efficace de la LMC,
qu’une association à un autre SMP
a été suspectée : augmentation de la
masse érythrocytaire nécessitant des
saignées pour le patient d’Inami,
fibrose médullaire évolutive pour les
deux autres cas, avec retentissement
clinicobiologique dans le cas de
Krämer (splénomégalie, hyperleu-
cocytose, érythro-myélémie). Dans
ces trois cas, une mutation JAK2-
V617F a pu être mise en évidence
au moment de l’évolution inhabi-
tuelle. Les analyses rétrospectives
des échantillons antérieurs ont dans
tous les cas montré la présence de la
mutation dès le diagnostic.
Ainsi, ces cinq observations mon-
trent qu’une association entre deux
syndromes myéloprolifératifs et
deux anomalies moléculaires spé-
cifiques, bien que rare, est possible.
Ces cas sont éclairants à plusieurs
titres. Tout d’abord, ils permettent
de faire des hypothèses physiopa-
thologiques intéressantes. Tous les
auteurs concluent à la grande proba-
bilité que ces associations ne soient
pas le fruit du hasard. Ces deux ano-
malies semblent plutôt liées à une
sensibilité plus grande des cellules
de ces patients aux altérations géni-
ques. Les études réalisées après tris
et cultures cellulaires par le groupe
de Bornhauser [2] retrouvent la
fusion BCR-ABL dans les CFU-GM
mais pas dans les BFU-E tandis que
la mutation JAK2 est présente dans
les deux types de cellules. Ils en
concluent que la translocation 9;22
est survenue secondairement à la
mutation JAK2, au stade d’un pro-
géniteur plus engagé. Si des LMC
secondaires ont été décrites après
exposition à des chimiothérapies, on
peut aussi envisager qu’une LMC
soit secondaire à un autre SMP, bien
qu’ici, sans exposition aux drogues
cytotoxiques. Les cinétiques d’évo-
lution de la charge BCR-ABL et de
la charge JAK2 dans ces différentes
études sont toutes cohérentes avec
cette hypothèse. Il reste à établir de
façon formelle que les deux ano-
malies coexistent dans une même
cellule. Par ailleurs, ces histoires
cliniques doivent nous amener à
évoquer la possibilité d’un second
SMP associé en cas d’évolution cli-
nique inhabituelle d’un SMP traité,
soit pour mettre en évidence une
mutation JAK2 au décours d’une
LMC en réponse à l’imatinib, même
s’il n’y a guère de sanction théra-
peutique, soit surtout pour découvrir
un clone porteur d’un chromosome
Philadelphie dans l’évolution d’un
SMP à JAK2 muté.
Références
1. Curtin NJ, Campbell PJ, Green AR.
The Philadelphia translocation and pre-
existing myeloproliferative disorders. Br J
Haematol 2005 ; 128 : 734-6.
2. Bornhäuser M, Mohr B, Oelschlaegel U,
et al. Concurrent JAK2(V617F) muta-
tion and BCR-ABL translocation within
committed myeloid progenitors in myelo-
fibrosis. Leukemia 2007 ; 21 : 1824-6.
3. Inami M, Inokuchi K, Okabe M,
et al. Polycythemia associated with the
JAK2V617F mutation emerged during
treatment of chronic myelogenous leuke-
mia. Leukemia 2007 ; 21 : 1103-4.
4. Krämer A, Reiter A, Kruth J, et al.
JAK2-V617F mutation in a patient with
Philadelphia-chromosome-positive
chronic myeloid leukaemia. Lancet Oncol
2007 ; 8 : 658-60.
5. Hussein K, Bock O, Seegers A, et al.
Myelofibrosis evolving during imatinib
treatment of a chronic myeloproliferative
disease with coexisting BCR-ABL trans-
location and JAK2V617F mutation. Blood
2007 ; 109 : 4106-7.
jlehma00240_cor4.indd 226jlehma00240_cor4.indd 226 9/18/2007 7:02:50 PM9/18/2007 7:02:50 PM
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

Hématologie, vol. 13, n° 4, juillet-août 2007
227
Actualités cliniques
Sarcomes à cellules folliculaires dendritiques :
il faut modifi er et intensifi er les traitements
Janine DUMONT
Cela fait plus de 20 ans que
l’utilisation des anticorps sur
coupes, plus encore que la mor-
phologie, a permis de bien distinguer
des lymphomes les tumeurs dévelop-
pées à partir des cellules folliculaires
dendritiques, même si leur localisa-
tion, le plus souvent ganglionnaire,
pourrait évoquer cliniquement une
forme particulière de lymphome.
La première individualisation de ces
tumeurs date de 1986 [1], et quel-
ques « grandes » séries rassemblées
plus tard [2-4] ont confirmé leur
aspect histologique particulier, les
moyens d’en affirmer le diagnostic
grâce à quelques marqueurs spé-
cifiques, et aussi très vite leur fort
potentiel de malignité. Le terme de
« sarcome » a prévalu alors, et son
usage a le mérite, tout en insistant
sur la gravité de ces tumeurs, d’in-
viter les cliniciens à sortir des sché-
mas thérapeutiques efficaces dans
les lymphomes, souvent employés
ici et trop souvent décevants.
Le principal mérite de la série du
MD Anderson Cancer Center [5],
qui vient d’être publiée, ne tient pas
tant au nombre des cas (cela reste
vraiment une tumeur rare), mais au
détail des traitements et du suivi de
ces 14 malades observés entre 1995
et 2005.
Les 14 cas ont fait l’objet d’un dia-
gnostic histologique confirmé par
les marqueurs monoclonaux : CD 21
et CD 23, CD 35, CD 68, mais aussi
EGFR retrouvé 10 fois sur 11, ce qui
représente une piste de réflexion inté-
ressante après la publication de Sun
et al. [6] décrivant l’hyper-expres-
sion de ce facteur dans les sarcomes
à cellules folliculaires dendritiques
(et non dans les cellules folliculai-
res dendritiques normales) et aussi,
à un moindre degré, dans la mala-
die de Castelman. On peut imaginer
pour l’avenir que cette constatation
amène à envisager des traitements
ciblés susceptibles d’améliorer le
pronostic de ces sarcomes. Celui-ci
est en effet loin d’être favorable, et
la description de ces 14 tumeurs, à
la fois ganglionnaires et extra-gan-
glionnaires (dont deux du naso-pha-
rynx), le confirme bien.
Malgré une moyenne d’âge relative-
ment jeune (48 ans), un PS moyen à 1,
et 2/14 seulement de symptomes B,
les rémissions complètes, lorsqu’el-
les sont obtenues, sont dans l’en-
semble de courte durée et il n’y a
qu’un seul patient apparemment
guéri à long terme. Deux facteurs
de mauvais pronostic peuvent inter-
venir : une taille tumorale supé-
rieure à 3 cm dans 9 cas sur 11, et
une extension viscérale dépassant
le stade locorégional dans la moi-
tié des cas. Il n’est pas précisé si
le degré de malignité histologique
(pourtant décrit en trois stades dif-
férents) influence la réponse au
traitement.
Celle-ci est décrite à la fois au stade
initial et lors des rechutes, préci-
sions qui n’existent dans aucune
des séries précédentes. Les conclu-
sions thérapeutiques à en tirer, sous
réserve du petit nombre de malades,
sont importantes :
1. La chimiothérapie seule – ici
toujours par CHOP – n’a jamais
entraîné de rémission complète, et
même, pas de réponse du tout, puis-
que dans 3 cas il y a une progression
sous ce traitement initial.
2. La chirurgie seule, ou complétée
par une radiothérapie locale, peut
entraîner une rémission, mais de
courte durée.
3. Les seuls cas ayant eu une lon-
gue rémission complète (29 mois
à 8 ans) l’ont été après un triple
traitement : chirurgie, puis CHOP,
puis radiothérapie, et c’est dans ce
groupe que s’observe le seul patient
sans maladie visible à plus de 8 ans
du diagnostic.
4. Dans le rattrapage des rechu-
tes, une rémission complète a été
évidence, indépendamment du dia-
gnostic de PV ou de TE, deux popu-
lations de patients différents : les
patients homozygotes sont plus âgés,
ont des leucocytes et un hématocrite
plus élevés, une splénomégalie plus
importante, ainsi qu’une tendance
plus marquée à évoluer vers la myé-
lofibrose. Chez les patients présen-
tant une PV, l’homozygotie n’est
pas un facteur de risque thromboti-
que. Par contre, les patients atteints
de TE et homozygotes ont 1,5 fois
plus de chance de présenter un évé-
nement cardiovasculaire que les
hétéro zygotes, et 4 fois plus que les
TE sans la mutation JAK2 617V>F.
Finalement, une chimiothérapie
est plus volontiers utilisée chez les
patients homozygotes pour contrô-
ler leur maladie.
Ces données rendent la détection des
mutations de JAK2 nécessaire, non
seulement pour le diagnostic mais
aussi pour la prise en charge thé-
rapeutique des patients. Les études
prospectives devront intégrer cette
recherche afin de mieux classer les
patients en fonction de leur risque
thrombotique et d’évolution vers la
myélofibrose.
Référence
1. Vannucchi AM, Antonioli E,
Guglielmelli P, et al. Clinical profile of
homozygous JAK2 617V>F mutation in
patients with polycythemia vera or essen-
tial thrombocytemia. Blood 2007 ; 110 :
840-6.
jlehma00240_cor4.indd 227jlehma00240_cor4.indd 227 9/18/2007 7:02:50 PM9/18/2007 7:02:50 PM
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.
1
/
2
100%