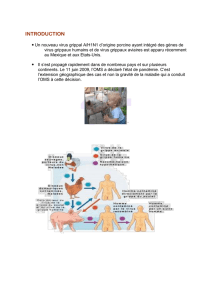
Deux cas graves d`infection grippale A/H1N1 2009 en Aquitaine

▲ Figure 1. Suivi clinique et virologique des patients 1 et 2 au cours des mois de juillet et août 2009.
Patiente 1
Patient 2
Oseltamivir
150 mg/j
Oseltamivir
300 mg/j
Oseltamivir
300 mg/j
Syndrome
grippal
Syndrome
grippal
A/H1N1v
NP+
A/H1N1v
NP+
A/H1N1v
NP+
LBA+ A/H1N1v
LBA–
EBV
12 100 copies/ml
Sang total
EBV
2 330 copies/ml
Sang total
25 juillet 30 juillet 2 août 4 août 5 août 14 août 20 août
La Lettre de l’Infectiologue • Tome XXIV - n° 4 - juillet-août 2009 | 133
Mots-clés
A/H1N1 2009 – SDRA – France
Keywords
A/H1N1 2009 – ARDS – France
Deux cas graves d’infection grippale
A/H1N1 2009 en Aquitaine
Two cases of severe flu A(H1N1) 2009 infection in Aquitaine, France
S. Burrel1, J. Youssef2, C. Balick-Weber3, H. Roze4, S. Fourcade5, A.C. Jeannot1, L. Roncin1, P. Blanco6, H. Fleury1
1 Laboratoire de virologie, CHU de Bordeaux ; EA 2968, université Victor-Segalen – Bordeaux-2,
Bordeaux.
2 Service de réanimation, hôpital Saint-André, CHU de Bordeaux.
3 Service de réanimation, hôpital Pellegrin, CHU de Bordeaux.
4 Service de réanimation thoracique, hôpital du Haut-Lévèque, CHU de Bordeaux.
5 Fédération des urgences, centre hospitalier de Mont-de-Marsan.
6 Laboratoire d’immunologie, CHU de Bordeaux.
D
epuis fin avril 2009, un nouveau virus grippal d’origine porcine,
A/H1N1 2009, s’est propagé de façon pandémique grâce à
son fort pouvoir de transmission interhumaine (1). À ce jour
(6 septembre 2009), l’Organisation mondiale de la santé confirme
un total de 277 207 cas avérés dans le monde entier, dont au moins
3 205 décès (2). En France, la circulation du virus est confirmée sur
l’ensemble du territoire. Si la plupart des personnes infectées sont
atteintes de formes cliniques modérées, quelques cas d’infection
plus sévères sont observés. En France, l’Institut de veille sanitaire
recense, depuis le début de l’épidémie, 129 patients hospitalisés
dont 17 dans un état jugé préoccupant (3). Six patients ont
présenté un syndrome de détresse respiratoire aigu (SDRA)
dont 4 sont encore hospitalisés en service de soins intensifs.
Nous rapportons ici 2 cas de SDRA hospitalisés au CHU de
Bordeaux. Le suivi clinique et virologique des 2 patients est
présenté dans la figure 1.
Cas 1
La patiente 1, âgée de 27 ans, a passé la soirée du 21 juillet 2009
en Espagne. Elle y a été victime d’un accident de baignade :
une noyade de stade 1 (caractérisée par la présence d’eau dans
l’estomac, sans inhalation) avec traumatisme thoracique et
lombaire à la suite d’un choc sur un rocher. De retour en France,
le 22 juillet, elle consulte un urgentiste du centre hospita-
CAS CLINIQUE

▲ Figure 2. Radiographies successives du 2 au 11 août 2009 de la patiente 1.
134 | La Lettre de l’Infectiologue • Tome XXIV - n° 4 - juillet-août 2009
lier général (CHG) de Mont-de-Marsan qui prescrit des examens
radiologiques ne révélant aucune fracture. La patiente rentre à
domicile avec une prescription d’anti-inflammatoire stéroïdien. Le
25 juillet, elle est de nouveau adressée aux urgences du CHG de
Mont-de-Marsan pour un début de syndrome grippal avec fièvre
à 41 °C, toux et courbatures. En l’absence de signes de gravité, il
est conseillé à la patiente de rester chez elle en isolement respira-
toire ; un traitement médicamenteux par tétrazépam (Myolastan
®
),
paracétamol (Doliprane®), aspirine (Aspégic®) et un sirop antitussif
(Toplexil®) lui sont prescrits.
Le 30 juillet, la patiente est de nouveau admise aux urgences du
CHG de Mont-de-Marsan pour cause d’altération de l’état général,
de fièvre (38 °C) avec détresse respiratoire, mais également à la
suite de 2 malaises avec courte perte de connaissance. Devant
ce tableau clinique, le service de réanimation prend en charge la
patiente sous ventilation mécanique. Un traitement associant
céfotaxime (Claforan
®
), spiramycine (Rovamycine
®
) et oseltamivir
(Tamiflu
®
75 mg x 2/j) est mis en place. Un prélèvement naso-
pharyngé, envoyé au laboratoire de virologie du CHU de Bordeaux,
permet de mettre en évidence la présence de virus A/ H1N1 2009 ;
la présence du nouveau virus porcin est également confirmée par
une analyse virologique effectuée chez le compagnon de la patiente.
Celle-ci est transférée, le 1er août, dans le service de réanimation
de l’hôpital Pellegrin du CHU de Bordeaux. L’examen d’entrée
témoigne d’une fièvre à 39,5 °C et d’un SDRA avec des aspirations
peu abondantes et des râles bronchiques diffus à l’auscultation
pulmonaire. La radiographie thoracique du 2 août montre des
images d’opacités alvéolaires bilatérales diffuses (figure 2). La
patiente présente par ailleurs une obésité modérée avec un indice
de masse corporelle (IMC) de 34,6 (100 kg pour 1,70 m). Le bilan
biologique rapporte une légère leucopénie (3 800/mm
3
), une
forte rhabdomyolyse (CPK : 1 362 UI/l), une procalcitonine (PCT)
augmentée (1,69 µg/l), un taux de LDH augmenté à 332 UI/l, une
cholestase et une cytolyse hépatique modérées (ASAT = 200 UI/l ;
ALAT = 100 UI/l ; PAL = 230 UI/l ; GGT = 270 UI/l).
La patiente est de nouveau mise sous ventilation mécanique et
mise sous sédation par midazolam (Hypnovel®), sulfentanil et
Nimbex
®
. L’antibiothérapie probabiliste est remplacée par pipé-
racilline-tazobactam (Tazocilline
®
), amikacine (Amiklin
®
) et spira-
mycine (Rovamycine
®
). Le traitement par oseltamivir est poursuivi
à la dose classique.
Le 2 août, dans un prélèvement respiratoire de sécrétions profondes
envoyé en virologie, le virus A/H1N1 2009 est de nouveau retrouvé.
À noter que le prélèvement nasal réalisé simultanément est négatif.
Le 3 août, le signal viral persistant, la dose d’oseltamivir est doublée
(150 mg x 2/j). L’état instable de la patiente nécessite sa mise sous
oxygénateur extracorporel à membrane (extracorporeal membrane
oxygenation [ECMO]).
Le 4 août, la patiente présente un état de choc septique avec
progression du syndrome alvéolo-interstitiel et hyperleucocy-
tose (12 600/mm
3
). Une suspicion de pneumopathie acquise
sous ventilation motive le changement d’antibiothérapie pour
imipénem-cilastatine (Tienam
®
), linézolide (Zyvoxid
®
) et amikacine
(Amiklin®). Pour des raisons de logistique, la patiente est transférée
par le SAMU, sous ECMO, dans le service de réanimation thora-
cique de l’hôpital du Haut-Lévèque au CHU de Bordeaux. Cette
CAS CLINIQUE

La Lettre de l’Infectiologue • Tome XXIV - n° 4 - juillet-août 2009 | 135
patiente a des antécédents d’infection à répétition, notamment
d’angines sévères avec phlegmons. Le bilan immunitaire révèle
l’existence d’une hypogammaglobulinémie (IgG totales = 4,97 g/l),
d’une lymphopénie T CD4+ sans inversion du rapport CD4/CD8
(CD4+ = 481/mm3 ; CD8+ = 329/mm3, le 4 août). Le bilan viro-
logique est complété de sérologies et de recherches par biologie
moléculaire de la présence d’autres virus. Les sérologies du virus
de l’immunodéficience humaine (VIH), du virus de l’hépatite B
(VHB) et du VHC sont négatives. Le statut sérologique vis-à-vis
des herpès virus est le suivant : EBV IgM négatives et IgG 52 U/ml ;
CMV IgM négatives et IgG 22 UA/ml ; HSV IgM négatives et IgG <
6 UA ; VZV IgM négatives et IgG 189 mUI/ml. Les recherches en
biologie moléculaire des virus EBV, CMV et HHV6 se sont révélées
négatives dans le sang total. Sur les prélèvements respiratoires,
aucun autre virus n’a pu être mis en évidence (HSV, VZV, adéno-
virus et VRS). L’analyse bactériologique de divers prélèvements
respiratoires (crachats, liquide broncho-alvéolaires, sécrétions) n’a
pas démontré de surinfection bactérienne. Le 6 août, la patiente
est toujours sous ECMO ; un œdème lésionnel alvéolaire majeur
est mis en évidence à la radiographie pulmonaire (figure 2), et
un petit épanchement pleural bilatéral à l’échographie thora-
cique. Cet état nécessite la mise en place d’une hémofiltration
rénale afin de réduire sa masse hydrique. Le 7 août, il est décidé
de tenter de stimuler ses défenses immunitaires en administrant
des immunoglobulines polyvalentes (160 g) et de l’interféron-α
à la dose de 3 millions d’unités 3 fois par semaine. L’état de la
patiente s’améliore ensuite quotidiennement sur le plan respi-
ratoire, comme en témoignent les radiographies pulmonaires
(figure 2), et l’ECMO est retirée après 10 jours d’utilisation. Le
lendemain, la patiente est réveillée, consciente et orientée. Deux
jours après, elle commencera à respirer de manière spontanée. La
lymphopénie T se corrige (CD4+ = 961/mm3, CD8+ = 583/mm3,
le 12 août). Aucune phase de virémie du virus grippal n’a pu être
mise en évidence chez la patiente, cette recherche ayant pour but
d’objectiver une éventuelle dissémination virale. Au total, le virus
A/H1N1 2009 est détecté quotidiennement dans les prélèvements
respiratoires profonds pendant 21 jours malgré le traitement par
oseltamivir. Il est important de signaler que cette souche était
sensible à l’oseltamivir. En effet, le séquençage du gène de la
neuraminidase N1 ne fait pas apparaître la mutation H274Y (4).
Cas 2
Le patient 2, âgé de 51 ans, contrôleur à la Sécurité sociale, n’a
aucun antécédent médical connu. Le 25 juillet 2009, il a présenté
un début de syndrome grippal typique avec fièvre à 40 °C, frissons
et myalgies motivant une consultation chez son médecin traitant.
Il n’a eu aucun contact avec un sujet porteur de la grippe porcine
avéré et n’a pas voyagé à l’étranger les mois précédents. En l’ab-
sence de signes de gravité, il rentre chez lui avec un traitement
symptomatique par paracétamol (Doliprane
®
) et des consignes
de repos mais également de mesures d’isolement. Le patient ne
présente aucun facteur de risque cardio-vasculaire hormis un
IMC à 32 (1,74 m, 97 kg), témoin d’une obésité modérée. Il ne
fume pas. Sept jours après le début des symptômes, une toux
sèche et un syndrome respiratoire s’ajoutent au tableau clinique,
ainsi qu’une dyspnée mineure, présente notamment à l’effort. La
suspicion d’une surinfection bactérienne entraîne la mise sous
antibiothérapie par amoxicilline-acide clavulanique (Augmentin
®
)
puis par ceftriaxone (Rocéphine®) après 48 heures. Le 3 août,
le patient est admis aux urgences de l’hôpital Saint-André du
CHU de Bordeaux pour cause d’une altération de l’état général
avec une aggravation de la dyspnée et une asthénie importante.
L’examen d’entrée montre une fièvre élevée à 40 °C et des signes
de détresse respiratoire. La radiographie thoracique fait apparaître
des opacités alvéolaires bilatérales diffuses, compatibles avec
un œdème pulmonaire. Le patient ne présente aucun trouble
cardiaque associé. L’échographie cardiaque montre une fonction
ventriculaire gauche normale (fraction d’éjection de 60 %). L’hy-
poxie est sévère et résistante à l’oxygénothérapie seule (PaO2 =
41,3 mmHg sous air ambiant). Le patient est alors transféré dans le
service de réanimation du même hôpital, 6 heures après son arrivée
aux urgences. Il est intubé et placé sous ventilation mécanique. Le
4 août, devant ce tableau de SDRA et dans un contexte de suspi-
cion de grippe, un écouvillonnage naso-pharyngé est réalisé. La
présence d’une souche A/H1N1 2009 est détectée au laboratoire
de virologie du CHU de Bordeaux. Eu égard au poids du patient
et à la gravité du tableau clinique, un traitement par oseltamivir
(Tamiflu®) à double dose (150 mg x 2/j) est instauré. Un traitement
antibiotique par ceftriaxone (Rocéphine®) et spiramycine (Rova-
mycine®) est instauré de façon probabiliste. Le bilan biologique
relevait une lymphopénie T (CD4+ = 675/ mm
3
, CD8+ = 81/mm
3
,
le 4 août ; CD4+ = 793/mm3, CD8+ = 110/mm3, le 7 août ; CD4+
= 1154/mm3, CD8+ = 164/mm3, le 11 août), un bilan hépatique
légèrement perturbé (ASAT = 69 UI/l, ALAT = 60 UI/l, PAL = 37 UI/l,
GGT = 95 UI/l), une rhabdomyolyse (CPK = 739 UI/l) et un taux
de LDH élevé à 340 UI/l. La CRP atteint 265 mg/l le 5 août et la
PCT est à 0,38 µg/l. Il n’a pas été observé de virémie grippale (PCR
A/ H1N1 2009 négative sur sang total recueilli sur EDTA). Les séro-
logies virales des hépatites B et C et du VIH sont négatives. Sur sang
total, la PCR CMV est négative, alors que la charge virale EBV est
de 12 100 copies/ ml le 5 août, puis de 2 330 copies/ml le 14 août.
Le traitement par oseltamivir est poursuivi jusqu’à la négativation
des prélèvements respiratoires, le 10 août. Le génotypage de la
souche par biologie moléculaire permet de confirmer l’efficacité
clinique de l’oseltamivir, puisque la souche A/H1N1 2009 isolée est
sensible à ce médicament (absence de mutation en position 274
de la neuraminidase N1) [4]. L’amélioration clinique est franche
et l’état du patient se stabilise. Une suspicion de phlébite évoquée
devant une jambe rouge et gonflée est rapidement confirmée par
un doppler des membres inférieurs. Un angioscanner thoracique
réalisé le 11 août révèle une embolie pulmonaire sous-segmentaire
droite et des plages de verre dépoli diffuses en rapport avec un
SDRA diffus. L’étude d’un LBA non hématique met en évidence une
alvéolite constituée de lymphocytes T CD8+ (56 % des lympho-
cytes du LBA) dans les poumons. Le 12 août, une fièvre élevée fait
suspecter une infection bactérienne nosocomiale. L’instauration
d’une antibiothérapie probabiliste par céfépime (Axepim®) et
amikacine (Amiklin
®
) permet une régression des symptômes et
la diminution du syndrome inflammatoire. L’évolution est ensuite
favorable, permettant de débuter un sevrage respiratoire.
CAS CLINIQUE

136 | La Lettre de l’Infectiologue • Tome XXIV - n° 4 - juillet-août 2009
Discussion
Le bulletin Morbidity and Mortality Weekly Report (MMWR) du
Center for Disease Control (CDC) d’Atlanta, datant de juin 2009,
rapporte 10 cas d’infections sévères par le nouveau virus A/H1N1
2009, pris en charge dans des services de réanimation aux États-
Unis, dont 3 sont décédés (5). Ce rapport résume les caractéris-
tiques et l’évolution clinique de ces 10 patients admis pour cause
d’hypoxémie sévère, de SDRA ou de défaillance respiratoire. L’âge
médian était de 46 ans (21-53 ans). Neuf patients avaient un IMC
supérieur ou égal à 30. L’obésité n’a jamais été rapportée jusqu’à
présent comme un facteur de risque de complications des infections
grippales saisonnières. Cependant, selon cette étude, il convient
de la considérer comme un éventuel facteur de comorbidité non
négligeable chez les patients infectés par la souche A/ H1N1 2009.
De nouvelles données sont donc nécessaires pour confirmer le rôle
précis de l’obésité. La moitié des patients a fait un épisode d’em-
bolie pulmonaire. L’état de défaillance pulmonaire aggravé chez
2 patients a nécessité la mise sous ECMO. L’épuration extrarénale
continue (EERC) fut mise en place chez 6 patients pour pallier une
insuffisance rénale aiguë (IRA). La valeur médiane des transami-
nases ASAT pour les 10 patients était de 83,5 UI/l (41-109 UI/l).
Six patients sur 9 testés avaient une élévation significative du
taux de CPK, avec une valeur médiane de 999 UI/l (51-6 572 UI/l).
Une étude rétrospective de cas de pneumonie et de défaillance
respiratoire dans des cas d’infection par la souche A/H1N1 2009
à Mexico a également rapporté l’existence d’un taux de CPK élevé
chez 62 % des patients testés. Une lymphopénie était retrouvée
chez 61 % des malades. Tous les patients de l’étude avaient un
taux de LDH élevé (6).
Sur le plan virologique, l’instauration précoce d’un traitement
par inhibiteur de neuraminidase (oseltamivir ou zanamivir) est
recommandée pour une efficacité optimale. Il est à noter qu’aucun
des 2 patients n’a reçu d’oseltamivir dans les 48 premières heures
suivant le début des symptômes. Un traitement par oseltamivir
à plus forte dose et pendant une durée allongée par rapport à la
prise en charge classique a déjà été suggéré pour les infections
compliquées de grippe aviaire A/H5N1. Un schéma posologique à
double dose d’oseltamivir (150 mg x 2/j par voie orale) est actuelle-
ment envisagé chez les patients infectés par le virus A/H1N1 2009
présentant une forme clinique sévère (5, 7).
Les 2 patients de notre étude présentaient des tableaux cliniques
ressemblant à ceux des cas décrits aux États-Unis et au Mexique :
en effet, l’obésité, caractéristique quasi constante chez les sujets
de l’étude du CDC, est également retrouvée chez nos 2 patients.
Les épisodes de rhabdomyolyse, d’augmentation du taux de LDH
et de lymphopénie T correspondent aux descriptions de patients
présentant des formes cliniques sévères d’infection grippale par la
nouvelle souche A/H1N1 2009 (5, 6). En outre, nous précisons dans
notre observation qu’il n’y a ni inversion du rapport CD4/CD8, ni
signes d’activation du compartiment CD8. La patiente 1 a reçu un
traitement atypique à base d’interféron-α et d’immunoglobulines
polyvalentes dans un contexte de grippe sévère. L’hypothèse d’une
action synergique de l’effet antiviral de l’interféron-α et de l’ad-
ministration d’immunoglobulines polyvalentes pourrait expliquer
l’évolution favorable de l’état clinique de cette patiente. L’embolie
pulmonaire qui aggrave la situation clinique du patient 2 est a
priori inhérente à la phlébite du membre inférieur diagnostiquée
par doppler. Cependant, l’agent grippal pourrait potentiellement
être une étiologie favorisante : en effet, la série du Michigan, aux
États-Unis (5), fait état de l’apparition d’une embolie pulmonaire
chez 50 % des patients présentant une infection sévère à A/H1N1
2009. ■
1. Novel Swine-Origin Influenza A(H1N1) Virus Investigation Team, Dawood FS,
Jain S et al. Emergence of a novel swine-origin influenza A (H1N1) virus in humans.
N Engl J Med 2009;360(25):2605-15.
2. World Health Organization, Pandemic (H1N1) 2009 - update 65. http://www.
who.int/csr/don/2009_09_11/en/index.html
3. Institut de veille sanitaire, Bulletin épidémiologique Grippe A(H1N1) 2009.
Point de la situation au 8 septembre 2009. http://www.invs.sante.fr/display/
?doc=surveillance/grippe_dossier/points_h1n1/grippe_A_h1n1_090909/index.html
4. Ferraris O, Lina B. Mutations of neuraminidase implicated in neuraminidase in-
hibitors resistance. J Clin Virol 2008;41(1):13-9.
5. Centers for Disease Control and Prevention (CDC). Intensive-care patients with
severe novel influenza A (H1N1) virus infection - Michigan, June 2009. MMWR
Morb Mortal Wkly Rep 2009;58(27):749-52.
6. Perez-Padilla R, de la Rosa-Zamboni D, Ponce de Leon S et al. Pneumonia and
respiratory failure from swine-origin influenza A (H1N1) in Mexico. N Engl J Med
2009;361(7):680-9.
7. Abdel-Ghafar AN, Chotpitayasunondh T, GaoZ et al. Update on avian influenza A
(H5N1) virus infection in humans. N Engl J Med 2008;358(3):261-73.
Références bibliographiques
CAS CLINIQUE
1
/
4
100%