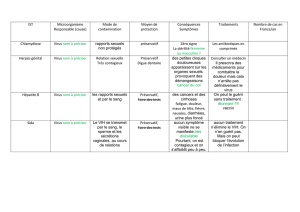
COURS N° 7b : PHYSIOPATHOLOGIE DES INFECTIONS VIRALES

!"#
$%&'$()*
$"+$,-%.
/#-01 2#3#*##* 345

Table des matières
67**8#(!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6#))9!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6((!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!:
56#*;!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!:
5!6<#*#(9)#*#9#*8#3**8)3=!!!!!!:
5!6 2#3#*#*8)3=!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
:6#*3!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
:!6/#9*8)3/!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
:!6#9',>!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
:!6,#*>3?!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6)3#((@*8#!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!6$#*8*3****!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!68)#*3!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!6',>!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!56##*!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6<33(@*)3#((!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6()((#***!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
6A(#?*(!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!633!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
!6##()*2(3#2B/"'C!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!5
Le Professeur Morinet a relu ce cours et m'a précisé que sur ses deux cours (celui-ci et «le monde
des virus et des prions») il proposera uniquement des QCMs aux responsables de l'enseignement.
/#-01 2#3#*##* 345

1 - Le rôle de l'environnement :
##?23#)9!8#(#9#(!
'##(3*D)#E@
•# *)198#33**B**
-)C!/(*##*3289*8+#((*
-)!
/3##9?)(#98)#*#(#**!
•# )19833*** BF-*#*C!
.##(G-*+#H*)))#!
/##(!(#(#9@*8>#((!39
*8#I*(#9#(*(#939*8>#((*#(@#
#!
/#(( * # # (I * 3 *89 J# (3))
8#383(33(3*!
A3*IJK3#)I#3##1)3*!
•(3J) 9)#',>6!
2 - Le fond génétique :
-##((3#3**3#3*##(*I8#!
(3*I##*(3##6)8#L(!
'#5(3*
•A*//$:',>! *#9*)#',>!***I**)3
9*(#*)*%/A5!,* *#*(#3#****%3
(#*)*/A5!
#*I*)#6)3*(#*)*//$:B/2)/2)$)3:C!
/(#*)*3)**2(3#2%/A5*(#3!
A*(L#)I*#9*8##*',>#)!"I#3I
43#83(3//$:@*****#6)3()I
*2#3*(898#33***//$:!
A#4#)@*8#3*',>!
• ? 6 # = *3# = #(( )3 *8?
#3 ! 3# ) # )(! 3#
83(3 #)@#*!
•&6 - ## *3#2*?&3(*#3I=I>
M@****)3)****!/*9
3##3#1*(1* 3*##9#*(L
#6)! K 3( *8? @ * * ***
)3)****#98*#))!
K##))##3)3*##!
/#-01 2#3#*##* 345

•.- ,)#N6>)3/ B.- F**#3#*2(#3(C!
*2*?*O)#*(1I#()(#?
3#*2(#3(1/6/!3#//PB#(#J2#3#*1//C
(#?I#@3#31*8)*(**8)3/!
'##98)#*)**(!
/83',>P9)()*)(;(2)*#QB#*(*
(#**C!**(#*8)**(#**(983(3*#6
)3//$:!
#98#*2)3#1#*#9I#**I*)3#****
)3#(#*!
!"#$$%&'()*#%'%B#1C
/*3)***%@))*8)#((!
/J*3)3(#**#//$:B*//$:C#3!+3
*2(3#2#(#*8?/"'B2#()*#C!
.*)3#*2(3#2%3)R*22?8)#((!
I#3*****2(3#2#(*8?',>!+#*#9*
* O# R #I * 3 8 3 )3# *2(3#2 % 9 ?
*O)#(()3#@*(*#3*',>!
A#I*)3#83*I898*823*3)*8#(!
+!"#$$%&'(),#-(%
+3#5393)*3#)*9#))3*#3!
6*88)(#3#F)(83',>9)#*
3#))3#)*1*!
II56##98*2(#(#1#*L2)(#(#
8#331*#S*3#)',>!
FFT#./'%(%/&%$0#%*%()#1%22&#)-($&'&&)3!
*33#1!
#I83)39933#(**3!
/#-01 2#3#*##* 3545
4!"#$$*,%15%6
+3 ##1
393)**
*!+3*##9**6
U8# @ * *
(#**#//$:!

3 - Le statut immunitaire
%#(3*
•*(#)3) 9*)(!#3*##
*##*))I*2)#%('&)!/@9)*#33
◦(@>3?.(3*'I
◦#3#@'$.B'$3#.2*C93##9
1##*!
•%3*# 8# B/AC 3 9 # # )*I #
--#)(#''%-2()*()73#98*L3*#!
•',>B/A5C $-)#()$89'%()$-(&*#:!
3*#8#*',>S9*)*%5%()$#
•='B3=C*2(3#(=
•>>'6#(V3#
•33**#(#(B*8I**I#*)C!
4 - Les infections virales aiguës :
(3*'*8)3=
%(#
•3#I#((*##(
•3#**
•(#(?6*(?)3*9*@I*2
1#38A-1#383#)9)(#*)3*#
98#33***8?>=*(#*#K!
I*(9)3*##1I*(#89K!
,*)#236>!
4.1 - Évolution des marqueurs sérologiques au cours de l'infection par le
virus de l'hépatite B
/#-01 2#3#*##* 3:45
ADN C
.
A-*
>=
>=
/6>=
/>=
/!+3#*8A-3**(#1*1I
*3B>=C9*8*#33B>1I3#
C!
/6>=
S10 S12 S24 S36
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%