physiologie de la procréation - Univ

Biologie
PHYSIOLOGIE DE
LA PROCRÉATION
Mars 2008
CUEEP - USTL
DÉPARTEMENT SCIENCES
JACQUES COGET


Table des matières
Table des matières 3
I - Introduction 5
II - Considérations préliminaires 7
A. Observation N°1..............................................................................7
B. Observation N°2..............................................................................8
C. Observation N°3..............................................................................9
III - Du sexe génétique au sexe phénotypique 13
A. Du sexe génétique au sexe phénotypique..........................................13
B. Exercice d'application......................................................................15
IV - Activité génitale et production hormonale 17
A. Chez l'homme................................................................................17
B. Chez la femme...............................................................................19
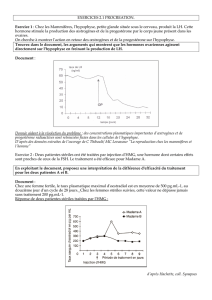
C. Exercice d'application 1...................................................................24
D. Exercice d'application 2...................................................................25
V - Activité génitale et régulation centrale 27
A. Le complexe hypothalamo-hypophysaire............................................27
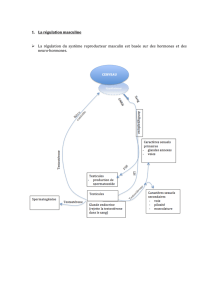
B. Régulation hormonale chez l'homme.................................................30
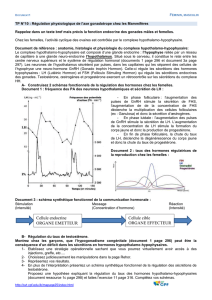
C. Régulation hormonale chez la femme................................................32
D. Exercice d'application N°1...............................................................35
E. Exercice d'application N°2................................................................36
CUEEP/USTL 3

VI - De la fécondation à la parturition 39
A. Segmentation, migration et nidation.................................................39
B. Le développement embryonnaire......................................................41
C. Hormones et gestation....................................................................45
D. Exercice d'application N°1...............................................................47
E. Exercice d'application n°2................................................................48
VII - La lactation 51
A. La lactation...................................................................................51
B. Exercice d'application......................................................................53
VIII - La contraception hormonale 55
A. La contraception hormonale.............................................................55
B. Exercice d'application......................................................................57
Solution des exercices de TD 59
CUEEP/USTL
4

I - Introduction I
Du latin «procreare» (= engendrer), la procréation regroupe l'ensemble des
processus qui permettent à deux individus sexués (un mâle et une femelle) de
donner naissance à un nouvel individu.
Bien que le terme soit en principe réservé à l'espèce humaine, il faut toutefois noter
que la plupart des animaux, et notamment les mammifères, procréent plus qu'ils ne
se reproduisent dans la mesure où l'être nouvellement conçu est toujours unique et
qu'il diffère de ses géniteurs en raison du brassage génétique qui s'opère lors de la
fabrication des gamètes (méiose) et de leur rencontre (fécondation).
Méiose, gamétogenèse et fécondation étant supposés connus (cf. EC III du
Bio 9), nous ne nous intéresserons ici qu'aux mécanismes génétiques et hormonaux
qui permettent le bon déroulement de la procréation, à savoir :
yle déterminisme du sexe,
yla mise en place de l'activité génitale et sa régulation,
yles principales étapes de la grossesse,
yla lactation.
Enfin, une dernière partie sera consacrée à la maîtrise de la procréation par
contraception hormonale.
CUEEP/USTL 5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
1
/
65
100%