Lire l`article complet

L
a prévalence élevée (16 à 28 %, [1, 2]) de l’alcoolo-
dépendance parmi les patients hospitalisés (quel que
soit le motif) impose une attention particulière des cli-
niciens sur le risque d’ap p a r ition d’un syndrome de sev rage
alcoolique (SSA). Chez les sujets dépendants non traités (parce
que bien souvent non repérés initialement comme malades de
l’alcool), la survenue de symptômes de sevrage ne pose généra-
lement pas de problème thérapeutique. On estime en effet que
moins de la moitié de ces patients développe des fo rmes mineure s
(anxiété, sueurs, tachycardie) du SSA spontanément résolutives
ou à l’aide d’un traitement (benzodiazépines ou carbamates) (3).
Bien que plus rare, l’évolution vers des formes majeures du SSA
est redoutée par sa rapidité d’installation et les difficultés de
contrôle d’une symptomatologie galopante conduisant parfois,
malgré la mise en place d’un traitement, à un tableau de delirium
tremens. Ainsi, la prise en charge thérapeutique du SSA était jus-
qu’à présent axée autour d’une prévention systématique utilisant
divers tranquillisants. La conférence de consensus de 1999 et les
recommandations de l’ANAES qui en sont issues (4) ont permis
de clarifier la pertinence d’une attitude thérapeutique plus adap-
tée à la situation clinique du patient et à son niveau de risque.
Nous réalisons ici une synthèse de ces données en proposant un
protocole de prévention du SSA en milieu hospitalier.
ÉPIDÉMIOLOGIE DU SSA
C o n t r a i rem ent à une idée encore trop répandue,la dépendance phy-
sique est inconstante chez le sujet alcoolodépendant ( 5 , 6 ). Sa phy-
s i o p at h o l ogie est liée à une réponse neuro a m i n e r gique cérébra l e
ex c i t a t rice destinée à compenser les effets globalement sédatifs de
l ’ a l c o o l i s ation ch ronique consécutifs à une modifi c ation fo n c t i o n-
nelle de la membrane neuronale ( 7 ). La fréquence du SSA a été
d i ve r sement estimée dans des enquêtes épidémiologiques rap p o r-
tant des prévalences de 30 à 60 % pour la surve n ue de symptômes
m i n e u rs dans les heures qui suivent l’arrêt des boissons alcooliques
( 8 , 9 ). L’ i n f luence du sexe (sur- rep r é s e n t ation du SSA chez les
hommes) est discutée ( 1 0 , 1 1 ) a l o rs qu’un âge supérieur à 40 a n s
s e m ble influencer la surve nue d’un SSA. La fo rme majeure asso-
ciant une agi t ation quasi constante et un état hallucinat o i re cl a s s i-
quement dénommé “ d e l i rium tre m e n s ” est plus ra re (4 %) ( 1 2 ).
Prise en charge du syndrome de sevrage alcoolique
en milieu hospitalier
Management of alcohol withdrawal syndrome
●S. Balester-Mouret*, P. Batel*
* Unité de traitement des maladies addictives, hôpital Beaujon, Clichy.
■
La prise en charge des sujets alcoolodépendants est une
problématique fréquente à l’hôpital.
■
Parmi les nombreux patients alcoolodépendants hospita-
l i s é s , seule une moitié va développer un syndrome de sev rage
a l c o o l i q u e. L’ é vol ution rapide ve rs une fo rme sévère de
sevrage est possible,conduisant parfois à un tableau de deli-
rium tremens.
■
Il apparaît donc nécessaire d’adopter une attitude théra-
peutique ciblée selon la situation clinique,évaluée périodi-
quement grâce à un score de sevrage. On déterminera ainsi
un niveau de risque afin de juger de la nécessité d’entre-
prendre un traitement préventif.
■
La prise en charge thérapeutique repose essentiellement
sur les benzodiazépines à posologie suffisante et dégressive,
l ’ hy d rat a tion et la vitaminothérap i e,c e rta ins tra i t e m e n t s
a d j u vants. La surveillance de la symptomat o l o gie perm e t
d ’ a d apt er le traitement à l’évo l u t i o n , le but étant d’éviter
l’aggravation de la situation. En cas de delirium tremens, le
transfert en unité de soins intensifs s’avère nécessaire.
■
Grâce à une stratégie de soins ciblée sur l’évolution cli-
nique, il est possible d’éviter le traitement systématique de
p atients qui ne le nécessitent pas et de contrôler la quasi-
totalité des syndromes de sevrage en évitant les accidents de
sevrage.
P O I N T S F O R T S
P O I N T S F O R T S
DO S S I E R T H É M A T I Q U E
La lettre de l’hépato-gastroentérologue - n° 2 - vol. VII - mars-avril 2004
82

FACTEURS DE RISQUE DE SSA
La sensibilité neuronale à développer un SSA est probablement
génétiquement déterm i n é e. A i n s i , l ’ a s s o c i ati on d’un allèle du
gène codant pour le transporteur de la sérotonine a été mise en
évidence comme facteur de risque de surve nue d’une cri s e
c o nv u l s i ve généralisée ou d’un delirium tremens ( 1 3 ). La pré-
sence d’un allèle du gène codant pour la sous-unité bêta2 du
récepteur GABA a été associée au risque de survenue de formes
sévères de SSA (14). Des facteurs de stress peuvent également
intervenir dans l’initiation comme dans l’accélération de l’évo-
lution ve rs des fo rmes sévères ( 1 5 , 1 6 ). Chez des sujets aya n t
déjà présenté un épisode comitial, la fréquence de récidive des
crises convulsives généralisées lors d’un nouveau sevrage (odds-
ratio : 16) (9) serait liée à une sensibilisation induite par un phé-
nomène d’embrasement cérébral dénommé kindling en anglais
(17, 18).
CLINIQUE
La symptomatologie du SSA regroupe divers signes peu spéci-
fiques dont l’intensité va ri able peut être très rapidement pro-
gre s s ive. Les pre m i e rs symptômes surviennent hab i t u e l l e m e n t
dans les 24 heures qui suivent la consommation du dernier verre
de boisson alcoolique et très rarement au-delà de 72 heures. Tou-
tefois, l’initiation tardive d’un SSA a été décrite en cas de trai-
tement préalable par bêtabloqueurs ou benzodiazépines au long
cours, en cas de traitement inadapté (posologie insuffisante) ou
d’anesthésie générale dans les heures suivant le sev rage ( 1 9 ) . Les
symptômes sont variablement regroupés en trois pôles syndro-
miques :
✓un syndrome adrénergique associant des tremblements inté-
ressant initialement les extrémités et qui ont tendance à se géné-
raliser à l’ensemble du corps, une tachycardie et une hyperten-
sion artérielle ;
✓des troubles neurovégétatifs associant sueurs, nausées, vomis-
sements, voire hyperthermie dans les formes plus sévères ;
✓des tro u b les neuro p s y ch i a t r i q u e s qui évoluent de fo r m e s
m i n e u res (anxiété, i rri t ab i l i t é , i n s o m n i e,i nve rsion du cy cle ny c-
t h é m é ra l , d é a m bu l at i o n , illusions tra n s i t o i r es) à des fo rmes plus
s é v è res (attaques de panique, c o n f u s i o n , agi t at i o n , t ro u b les de
la perc eption : h a l l u c i n ations sensori e l l e s , visuelles et/ou audi-
t ives). Dans les fo rmes ab o u t i e s , la composante délirante est
a u - d evant du tabl e a u , constituant la fo rme clinique du deliri u m
t re m e n s .
En fait, ces trois formes cliniques cohabitent dans un véritable
gradient d’intensité. Cette continuité évolutive de la symptoma-
tologie peut prendre des formes fulgurantes en cas d’existence
d’un facteur de stress physique ou psychologique et lorsque le
SSA a été inauguré par une crise convulsive généralisée (6 % des
cas) (6). Ainsi, la stratégie thérapeutique du SSA doit prioritai-
rement reposer sur la prévention précoce de la surve nue des
formes sévères.
TRAITEMENT
Compte tenu de la relative rareté des formes sévères et de l’ab-
sence de symptomatologie de sevrage chez plus de la moitié des
alcoolodépendants, il paraît peu licite de proposer un traitement
s y s t é m a tique à tous les malades repérés. C’est la raison pour
laquelle des “stratégies ciblées ” (20-22) sur les patients à risque
élevé de développement de SSA sévère (antécédents d’accidents
de sevrage) ont été proposées. Le schéma d’administration peut
ainsi utiliser un produit à doses fixes ou bien adapté à la symp-
t o m at o l ogie selon un pro t o c o l e. Dans tous les cas, il s’agit de
désamorcer un processus physiopathologique cérébral en préve-
nant la rapidité d’évolution des formes mineures vers les formes
majeures. Ainsi, un dispositif de surveillance et d’évaluation doit
être mis en place pour permettre une grande adaptabilité du trai-
tement.
Évaluation et surveillance du SSA
P l u s i e u rs instruments d’éva l u ation ont été développés pour mesu-
rer l’intensité d’un SSA ( 2 3 ). Ces échelles comportent un nombre
d’items va ri able regroupant des modifi c ations phy s i o l ogiques ou
des manifestations comportementales en rapport avec la réponse
a d r é n e rgique du sev rage, les signes neurov é g é t at i f s , la confusion,
l’agitation ou les phénomènes dysperceptifs ou hallucinatoires.
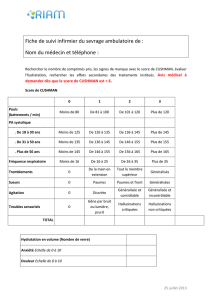
Parmi ces outils cliniques, dont la plupart ont été mis au point
pour des sev rages progra m m é s , le score de Cushman ap p a ra î t
comme le plus performant à utiliser en pratique quotidienne : il
s’agit d’un score d’utilisation aisément reproductible,sensible et
s p é c i f ique ( t abl eau I) ( 2 4 ) . En cas de traitement par alpha ou
b ê t a bl o q u a n t , le score de sev rage est diminué en moyenne de
deux points.
Traitement préventif du syndrome de sevrage
compliqué (tableau II)
La fréquence élevée de l’alcoolodépendance chez les sujets hos-
pitalisés quel qu’en soit le motif d’admission conduit à envisa-
ger systématiquement l’éventualité de ce diagnostic.
●Traitement de base
Dans ce cas, un traitement de base sera mis en place et associe
un accueil bienveillant dans un lieu calme afin de diminuer les
s t i m uli sonores et visuels. L’ hy d rat ation sera suffi s a n t e, à la
demande, sans être trop abondante pour éviter les risques d’hy-
p o n a trémie iat rogène (source de confusion) ou d’œdème aigu
pulmonaire. La voie orale sera privilégiée. Seuls des troubles de
la déglutition, de la conscience ou de déshydratation requièrent
la voie parentérale. Dans ce cas, on évitera les sérums glucosés
favorisant la carence en thiamine. L’association de vitamine B1
(500 mg par jour), vitamine B6 (250 mg par jour) et vitamine PP
( 2 5 0 mg par jour) sera pre s c rite par voie orale pour trois semaines
en évitant les prises vespérales, compte tenu de leur caractère sti-
mulant. L’ a d m i n i s t rat ion pare n t é ra l e, de préférence par perfu-
sion intraveineuse, est préconisée en cas de signes cliniques de
La lettre de l’hépato-gastroentérologue - n° 2 - vol. VII - mars-avril 2004 83
DO S S I E R T H É M A T I Q U E

c a r ence en thiamine (poly n é v ri t e,e n c é p h a l o p athie de Gaye t - We r-
nicke et béribéri cardiaque) (25). La surveillance de la sympto-
m at o l o gie de sev rage dev ra être continue grâce au score de
sevrage clinique :toutes les six heures pendant 24 à 48 heures.
L’évaluation de la sévérité du SSA par le score de Cushman doit
être systématique dès l’arrivée dans le service ou aux urgences
de tout patient suspecté d’alcoolodépendance et elle devra être
répétée lors du suivi. L’ i n t e r rogat o i re et l’examen clinique re ch e r-
cheront des pathologies associées ou de potentielles contre-indi-
c ations aux traitements à mettre en place. Une attention part i -
c u l i è re sera portée aux sujets à risque de développer un SSA
(antécédents de crise convulsive généralisée de sevrage et/ou de
delirium tremens). Chez ces sujets à risque, un traitement d’en-
tretien sera systématiquement instauré.
●Traitement d’entretien
La conférence de consensus sur le sevrage a validé l’utilisation
en pre m i è r e intention des benzodiazépines ( 4 ) . Le choix se
p o r t e ra sur une molécule à demi-vie longue (présentant un poten-
tiel d’abus moins élevé et prévenant mieux les crises comitiales),
utilisée par voie orale (la voie intraveineuse ne devant pas être
utilisée sans les moyens de surveillance et de réanimation adé-
quats) selon un schéma à posologie dégressive (4) :par exemple,
le diazépam 10 m g, un comprimé toutes les 4 h e u r es pendant
2 4 h e u res à diminuer progre s s ivement de manière quotidienne
jusqu’à l’arrêt en 5 à 7 j o u rs. Des équivalences posologi q u e s
(tableau III) existent entre les différentes benzodiazépines, avec
t o u t e f ois des diff é rences concernant l’efficacité en raison des dis-
parités de demi-vie.
.../...
La lettre de l’hépato-gastroentérologue - n° 2 - vol. VII - mars-avril 2004
84
DO S S I E R T H É M A T I Q U E
Tableau I. Score de Cushman (d’après [3, 24, 26]).
0 1 2 3
Pouls < 80 81-100 101-120 > 120
PA systolique < 135 136-145 146-155 > 155
Fréquence respiratoire < 16 16-25 26-35 > 35
Tremblements 0De la main en extension Tout le MS Généralisés
Sueurs 0 Paumes Paumes et front Généralisées
Agitation 0Discrète Généralisée/contrôlable Généralisée/incontrôlable
Troubles sensoriels 0Gêne par bruit ou lumière,Hallucinations critiquées Hallucinations non critiquées
prurit
Score 0-7* 8-14 15-21
Intensité Minime Moyen Sévère
* Le score est considéré comme minime seulement jusqu’à 6 chez les patients sous alpha- ou bêtabloquants.
Tableau II. Tableau décisionnel.
H0 : interrogatoire et examen clinique Évaluation 6 heures après l’arrivée
Score de sevrage < 8* “Traitement de base” Score < 8* Base
(si pas de CCG et/ou DT) Score/6 h Score 8* Base + Charge
Score 15 Réa
Antécédents de CCG et/ou DT “Traitement de base” Score < 8* Base + Entretien
“Traitement d’entretien” Score 8* Base + Charge
Score/4 h Score 15 Réa
Score de sevrage 8* “Traitement de base” Score < 8* Base + Entretien
“Traitement de charge” Score 8* Base + Entretien + Corticoïdes
Score/6 h Score 15 Réa
Score de sevrage 15 Réanimation
* Une valeur de 6 est retenue chez les patients sous alpha- ou bêtabloquants.

.../...
La surveillance du score de sevrage clinique sera alors plus fré-
q u e n t e, toutes les 4 h e u r es pendant 24 h e u r es puis toutes les
8heures par la suite,permettant une adaptation de la thérapeu-
tique à l’évolution. On pourra associer, en dehors des contre - i n d i-
cations habituelles, un bêtabloquant (par exemple le propanolol
1 6 0 m g LP/jour pendant 7 j o u rs) ( 2 6 ). Ce traitement adjuva n t ,
qui permet de contrôler les signes adrénergiques, diminuerait la
quantité de benzodiazépines nécessaire.
Lorsque l’évolution du SSA devient défavorable, attestée par le
f ra n chi ssement du seuil critique de 8 au score de Cushman, i l
convient de mettre en place un traitement plus incisif. Ce traite-
ment de ch a rge aura pour but d’éviter l’aggravation ve rs une situa-
tion clinique incontrôlable.
●Traitement de charge
On s’assure ra de la continuité des modalités du traitement de base
concernant l’installation du patient, son hydratation correcte, la
vitaminothérapie et un traitement bêtabloquant adjuvant.
Le traitement par benzodiazépines dev ra dans ce cas être
prescrit à dose de charge (27) par voie orale de préférence. On
p riv i l é gi e ra l’administration d’une dose importante dans un délai
c o u rt (six prises hora i res de 10 mg de diazépam en l’ab s e n c e
d’endormissement). Cette modalité d’administration aura pour
but l’obtention d’un état calme et le contrôle des symptômes du
SSA en évitant les surd o s a ges éventuels pouvant être re s p o n-
s ables de détresse re s p i rat o i re. La rééva l u ation de la situation cl i-
nique à la sixième heure permettra d’adapter la prise en charge
aux deux éventualités possibles.
Si le traitement de charge a permis l’amélioration de la situation,
le traitement par benzodiazépines sera pours u i vi à posologi e
d é c roissante selon les modalités du traitement d’entretien. Ce
t raitement dev r a être maintenu jusqu’à l’arrêt en 5 à 7 j o u rs ,
même si l’état du malade est très amélioré, en poursuivant une
surveillance clinique régulière.
Si la symptomat o l ogie n’a pu être améliorée et que le score
de Cushman est toujours au-delà du seuil critique de 8 , i l
c o nv i e n d ra de pours u iv r e un traitement par benzo d i a z é p i n e s
à posologie suffi s a n t e. Par ailleurs , on pourra env i s a ger l’ad-
jonction d’un traitement par corticoïde d’action rap i d e,s u s -
c e p t i b le de contrôler le syndrome adrénergique (dex a m é t h a -
sone 4 mg vo i e i . v. toutes les 12 h e u r es pendant 72 h e u r e s )
( 2 8 ) . La surveillance du score de sev rage se fe r a de manière
très rap p ro c hée toutes les heures jusqu’à une amélioration cl i -
nique stabl e .
Que faire en cas de SSA sévère
(score de Cushman 15) ?
À tout moment de l’évolution du SSA, la progression rapide de
la sévérité de la situation clinique est à craindre. Lorsque le score
de Cushman est au-delà de 15, la situation clinique impose une
prise en charge en unité de soins intensifs car elle nécessite une
sédation requérant des moyens de surveillance et de réanimation
adaptés.
Le traitement repose alors sur le maintien dans un état calme
p ro che du coma médicamenteux en utilisant des benzo d i a z é p i n e s
à fortes doses, par voie parentérale. Le flunitrazépam ou le mida-
zolam par voie i.v. sont recommandés, sans que l’on puisse stan-
dardiser les posologies en raison de grandes différences interin-
d ividuelles. Les autres mesures thérapeutiques nécessaires sero n t
e n t rep r ises para l l è l e m e n t :r é é q u i l i b rat ion hy d ro é l e c t r o ly t i q u e,
prévention des troubles ioniques, prévention du collapsus, ven-
t i l ation assistée si nécessaire, a n t i b i o t i q u e s , v i t a m i n o t h é r apie sys-
tématique.
En association aux benzodiazépines, on pourra utiliser un neu-
roleptique pour contrôler l’agitation importante ou le syndrome
h a l l u c i n at o i r e, l ’ h a l o p é ridol étant la molécule la plus validée dans
cette indication.
Cas des crises convulsives
Les crises conv u l s ives généralisées (CCG) surviennent généra-
lement dès la sixième heure qui suit la prise du dernier ve rre,
5 0 % dans les 24 p r e m i è res heures et 95 % dans les 72 h e u re s
( 2 9 ) . Une crise conv u l s i ve généralisée de sev rag e peut s’asso-
cier au delirium tremens et le précédera dans 30 % des cas ( 3 0 ) .
E n fi n , la présence d’une alcoolémie positive n’élimine pas l’étio-
l ogie de sev rage alcoolique d’une comitialité ; des CCG ont été
o b s e rvé es chez des sujets dont l’alcoolémie avait chuté très bru-
talement sans être négat ive . Une pat h o l ogie cérébrale sous-
jacente (tra u m at i s m e ,m é n i n g i t e, accident va s c u l a i r e) sera
re c h e rchée par une analyse clinique et anamnestique complète.
L’ é ven tualité d’une CCG impose de commencer un tra i t e m e n t
p r é ven tif du syndrome de sev rage par benzodiazépines dès l’ad-
mission du patient. En dehors des maladies épileptiques ou des
é t ats de mal comitial, elles ne nécessitent pas de traitement anti-
c o m i t i a l .
La lettre de l’hépato-gastroentérologue - n° 2 - vol. VII - mars-avril 2004 85
DO S S I E R T H É M A T I Q U E
Tableau III. Équivalences de posologie des benzodiazépines.
DCI Équivalence (mg) Demi-vie (h)
Oxazépam 25 8 à 10
Bromazépam 68 à 20
Lorazépam 110 à 12
Alprazolam 0,5 10 à 12
Prazépam 20 30 à 90
Clorazépate 20 30 à 90
Diazépam 10 30 à 90

La lettre de l’hépato-gastroentérologue - n° 2 - vol. VII - mars-avril 2004
86
DO S S I E R T H É M A T I Q U E
CONCLUSION
La prise en charge du syndrome du SSA en milieu hospitalier a
pour objectif essentiel de prévenir les formes sévères évoluant
ve rs un delirium tremens. Inconstant chez les sujets alcoolo-
dépendants en phase d’abstinence récente,le SSA ne nécessite
pas de manière systématique un traitement si la surveillance de
l’évolution est possible de manière satisfaisante et très régulière.
Une fois la phase de sevrage contrôlée,il est important d’évaluer
avec le sujet alcoolodépendant son degré d’implication dans un
projet d’abstinence au long cours et de mettre en place un projet
thérapeutique cohérent pour l’aider à le réaliser.
■
M o t s - c l é s .
Alcoolodépendance - Syndrome de sevrage -
Crises convulsives.
Key w o rd s .
Alcohol dependence - Alcohol withdrawal syn-
d rome - Epilepsy.
R
É F É R E N C E S B I B L I O G R A P H I Q U E S
1.
Ramirez D,Darné B, Lombrail P et al. Prévalence des maladies alcooliques
dans un hôpital universitaire de la banlieue parisienne. La Presse Médicale
1990 ; 19 :1571-5.
2.
Acquaviva E, Beaujouan L, Nuss P et al. Prévalence de l’abus d’alcool dans
un hôpital de l’AP-HP.Alcoologie et Addictologie 2003 ; 25 (3) : 201-7.
3.
Rueff B.Alcoologie clinique. Paris : Flammarion Médecine/Sciences, 1989.
4.
ANAES. Conférence de consensus : objectifs, indications et modalités du
sevrage du patient alcoolodépendant. Alcoologie 1999 ; 21 (Suppl. 2) : 80-90.
5.
Kraus ML, Segal SR, Sanguineti V et al. Ambulatory alcohol detoxification :
an alternative. Conn Med 1986 ; 50 (11) :717-20.
6.
Whitfield CL, Thompson G,Lamb A et al. Detoxification of 1 024 alcoholic
patients without psychoactive drugs. JAMA 1978 ; 239 (14) :1409-10.
7.
Paille F. Comment devient-on physiquement dépendant de l’alcool ? Rev
Prat Med Gen 1996 ; 10 (334) : 64-72.
8.
Gippini Perez A, Rodriguez Lopez I, Torre Carballada A et al. Alcohol with-
drawal syndrome at the internal medicine department of a general hospital ;
epidemiology and hospital costs. Ann Med Intern 1990 ; 7 (4) : 171-3.
9.
Hillbom M, Pieninkeroinen I, Leone M. Seizures in alcohol-dependent
patients : epidemiology, pathophysiology and management. CNS Drugs 2003 ;
17 (14) :1013-30.
10.
Callaghan RC, Cunningham JA. Gender differences in detoxification : pre-
dictors of completion and re-admission. J Subst Abuse Treat 2002 ; 23 (4) :
399-407.
11.
Deshmukh A, Rosenbloom MJ,Sassoon S et al. Alcoholic men endorse
more DSM-IV withdrawal symptoms than alcoholic women matched in drinking
history. J Stud Alcohol 2003 ; 64 (3) : 375-9.
12.
Fiellin DA, O’Connor PG,Holmboe ES,Horwitz RI. Risk for delirium tre-
mens in patients with alcohol withdrawal syndrome. Subst Abus 2002 ; 23 (2) :
83-94.
1 3 .
G o r wood P, Limosin F, B atel P et al. The A9 allele of the dopamine tra n s-
p o rter gene is associated with delirium tremens and alcohol-withdrawal seizure.
Biol Psychiatry 2003 ; 53 (1) : 85-92.
14.
Hood HM, Buck KJ.Allelic variation in the GABAA receptor gamma2
subunit is associated with genetic susceptibility to ethanol-induced motor
incoordination and hypothermia, conditioned taste aversion, and withdrawal
in BXD/Ty recombinant inbred mice.Alcohol Clin Exp Res 2000 ; 24 (9) :
1327-34.
15.
Hokenson P.Assessment of the patient at risk for acute alcohol withdrawal.
Medsurg Nurs 1994 ; 3 (3) : 211-7.
16.
Ferguson JA, Suelzer CJ, Eckert GJ et al. Risk factors for delirium tremens
development. J Gen Intern Med 1996 ; 11 (7) : 410-4.
17.
Glue P,Nutt D. Overexcitement and disinhibition. Dynamic neurotransmit-
ter interactions in alcohol withdrawal. Br J Psychiatry 1990 ; 157 : 491-9.
18.
Batel P, Lariviere P. [Late-onset alcohol withdrawal syndrome]. Ann Med
Interne (Paris) 2000 ; 151 (suppl. B) :B27-9.
19.
Daeppen JB, Gache P,Landry U et al. Symptom-triggered vs fixed-sche-
dule doses of benzodiazepine for alcohol withdrawal : a randomized treatment
trial. Arch Intern Med 2002 ; 162 (10) :1117-21.
20.
Lange-Asschenfeldt C, Muller MJ, Szegedi A et al. Symptom-triggered ver-
sus standard chlormethiazole treatment of inpatient alcohol withdrawal: clini-
cal implications from a chart analysis. Eur Addict Res 2003 ; 9 (1) : 1-7.
21.
Hiraman D,Su M, Howland MA, Hoffman RS. Symptom-triggered therapy
for alcohol withdrawal syndrome in medical inpatients. Mayo Clin Proc 2001 ;
76 (12) :1275-7.
22.
Williams D, Lewis J,McBride A. A comparison of rating scales for the
alcohol-withdrawal syndrome. Alcohol Alcohol 2001; 36(2):104-8.
23.
Cushman P Jr, Forbes R, Lerner W, Stewart M. Alcohol withdrawal syn-
dromes : clinical management with lofexidine.Alcohol Clin Exp Res 1985 ; 9
(2) : 103-8.
24.
Batel P. Encéphalopathie de Gayet-Wernicke. In PG, ed. Traité de médeci-
ne. Paris : Flammarion Médecine-Sciences 1998 ; 2427-8.
25.
Worner TM. Relative kindling effect of readmissions in alcoholics. Alcohol
Alcohol 1996 ; 31 :375-80.
26.
Kraus ML, Gottlieb LD,Horwitz RI, Anscher M. Randomized clinical trial
of atenolol in patients with alcohol withdrawal. N Engl J Med 1985 ; 313 (15) :
905-9.
27.
Sellers EM, Naranjo CA, Harrison M et al. Diazepam loading :simplified
treatment of alcohol withdrawal. Clin Pharmacol Ther 1983 ; 34 (6) : 822-6.
28.
Pol S,Nalpas B,Berthelot P. Dexamethasone for alcohol withdrawal. Ann
Intern Med 1991 ; 114 (8) : 705-6.
29.
Chan AW. Alcoholism and epilepsy. Epilepsia 1985 ; 26 (4) :323-33.
30.
Bouget J,David C, Saussey E. Accident de sevrage alcoolique. Le pro-
blèmes des crises convulsives. Alcoologie 1999 ; 21 (1S) : 1-6.
1
/
5
100%