Stratégie de synthèse et sélectivité en chimie

Lycée Paul CEZANNE – Aix-en-Provence Terminale S – Réforme 2012 http://www.stardustlabs.fr
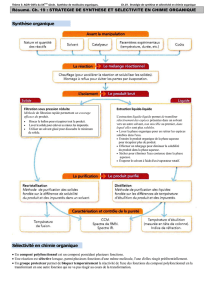
Partie III - Agir 19 – Stratégie de synthèse et sélectivité en chimie organique
Avant d’effectuer la réaction à proprement parler, il faut réfléchir aux différentes conditions permettant sa mise
en œuvre optimale :
- Choix des bons réactifs et de leurs quantités ;
- Choix du solvant ;
- Choix du catalyseur ;
- Choix du montage et des paramètres expérimentaux (température, durée, etc.) ;
- Aspects environnementaux et sécurité (impact sur la santé) ;
- Et enfin le coût.
La plupart des réactions ont besoin d’être effectuées avec chauffage pour en augmenter la
vitesse. On utilise alors un montage de chauffage à reflux, qui permet de chauffer tout en évitant
les pertes par évaporation (des produits et des réactifs).
Document 1 : montage de synthèse organique (chauffage à reflux)
- L’ampoule de coulée permet d’introduire le deuxième réactif progressivement ;
- La pierre ponce favorise une ébullition douce ;
- Le réfrigérant (à air, de Liebig ou à boules) permet de liquéfier les vapeurs des réactifs et des produits ;
ces dernières retombent alors dans le milieu réactionnel.
Il est nécessaire d’isoler le produit que l’on cherche à synthétiser du reste du milieu réactionnel
(réactifs en excès, solvant, sous-produits de réactions parasites). En effet, ces espèces chimiques
sont au minimum indésirables, elles peuvent au pire des cas être toxiques.
On dit qu’on obtient alors un produit brut.
Deux cas de figure se présentent : le produit de réaction que l’on veut récupérer est soit solide, soit liquide.
Sortie d’eau
Entrée d’eau
Ampoule de coulée
contenant le réactif n°2
Ballon bicol contenant le
réactif n°1 et la pierre ponce
Support élévateur
Réfrigérant à boule
Chauffe-ballon

Lycée Paul CEZANNE – Aix-en-Provence Terminale S – Réforme 2012 http://www.stardustlabs.fr
Partie III - Agir 19 – Stratégie de synthèse et sélectivité en chimie organique
a. Cas d’un solide
Pour récupérer le produit brut solide, on utilise la filtration sous vide à l’aide d’une fiole à vide munie d’un
entonnoir Büchner.
Document 2 : principe de la filtration Büchner
Il est souvent nécessaire de rincer le solide avec de l’eau (glacée), pour éliminer les traces d’espèces solubles
dans l’eau.
b. Cas d’un liquide
L’extraction liquide-liquide permet de transférer sélectivement des espèces présentes dans le
milieu réactionnel vers un autre solvant. L’espèce que l’on veut extraire doit être plus soluble
dans le solvant d’extraction, et celui-ci doit être non-miscible avec le solvant du milieu
réactionnel.
Document 3 : décantation
Pour améliorer la séparation, on peut procéder à un relargage : on sature la phase aqueuse en sels (chlorure
de sodium par exemple), ce qui diminue la solubilité du produit organique dans la phase aqueuse et favorise
son passage dans la phase organique.
Il faut, comme pour les espèces solides, rincer la phase organique avec de l’eau pour retirer les espèces qui
sont solubles dans l’eau.
Enfin, pour séparer le produit de la phase organique, on peut procéder à une évaporation du solvant à l’aide
d’un évaporateur rotatif.
c. Purification
Pour les solides, on procède à une recristallisation : l’opération consiste à dissoudre le produit brut dans un
solvant à chaud (les impuretés doivent être plus solubles que le produit dans le solvant).
Pour les liquides, on procède à une distillation fractionnée lorsque les températures d’ébullition du produit et
des impuretés sont différentes.
Entonnoir Büchner
Papier filtre
Fiole à vide
Aspiration forcée du
solvant par le vide
partiel dans la fiole
Phase la moins dense (le plus souvent
organique, mais pas toujours !)
Phase la plus dense (le plus
souvent aqueuse, mais pas
toujours !)
Ampoule à décanter

Lycée Paul CEZANNE – Aix-en-Provence Terminale S – Réforme 2012 http://www.stardustlabs.fr
Partie III - Agir 19 – Stratégie de synthèse et sélectivité en chimie organique
On calcule le rendement de la synthèse, il s’agit de la quantité de matière de produit récupéré à la
fin de la synthèse divisée par la quantité de matière attendue pour ce produit :
ηexp
max
n
n
On peut analyser un produit par chromatographie sur couche mince (CCM) :
Document 4 : chromatographie sur couche mince (CCM)
Si c’est un solide, on peut mesurer sa température de fusion à l’aide d’un banc Köfler : si le produit n’est pas
pur, sa température de fusion sera différente de celle indiquée dans les tables.
Document 5 : détermination de la température de fusion sur banc Köfler
Si c’est un liquide, on peut mesurer son indice de réfraction à l’aide d’un réfractomètre.
Il est aussi possible, lorsque le matériel est disponible, de réaliser le spectre IR et RMN du produit.
L’analyse du produit permet de contrôler sa pureté et de le caractériser.
Il existe des composés organiques, appelés composés polyfonctionnels, qui possèdent plusieurs groupes
caractéristiques. Or il est souvent souhaitable de n’en faire réagir qu’un pour arriver au produit désiré.
Une réaction est chimiosélective lorsque parmi plusieurs fonctions d’une même molécule, l’une
d’elle réagit préférentiellement avec le réactif considéré : ce réactif est dit alors chimiosélectif.
La sélectivité (ou non-sélectivité) d’une réaction dépend bien sûr des réactifs, mais pas
seulement : les conditions expérimentales entrent aussi en jeu (solvant, catalyseur, …).
Éluant
Plaque à CCM
Cuve à CCM
Front de
l’éluant
V J B
V J B

Lycée Paul CEZANNE – Aix-en-Provence Terminale S – Réforme 2012 http://www.stardustlabs.fr
Partie III - Agir 19 – Stratégie de synthèse et sélectivité en chimie organique
HO NH2
O
O
OHO NH
OHO
O
H2O
Document 6 : sélectivité dans la synthèse du paracétamol
O
O
OH
OH
O
O
O
25°C
O
O
OH
OH
O
O
O
100°C H2O
H2O
OH
2
Document 7 : réactions possibles de l’ion hydroxyle avec l’aspirine selon la température du milieu
Remarque : il a été vu dans le chapitre 12 des réactions sélectives, en fonction du mécanisme mis en jeu.
On souhaite partir de la molécule A pour obtenir la molécule B (représentées ci-dessous) :
Document 8 : molécule de départ (A) et molécule souhaitée (B)
Rappel : l’oxydation d’un alcool primaire conduit à l’aldéhyde puis à l’acide carboxylique (qui peut ensuite
être estérifié), l’oxydation d’un alcool secondaire conduit à une cétone.
La stratégie qui s’offre alors, c’est d’utiliser un réducteur très puissant comme
4
NaBH
(borohydrure de
sodium) ou
4
LiAlH
(tétrahydruroaluminate de lithium) : ces deux composés, en générant des ions hydrure,
permettent de réaliser les réactions inverses des oxydations d’alcools.
O
O O
O
HO
A
B

Lycée Paul CEZANNE – Aix-en-Provence Terminale S – Réforme 2012 http://www.stardustlabs.fr
Partie III - Agir 19 – Stratégie de synthèse et sélectivité en chimie organique
Le problème est que
4
NaBH
réduit très bien les aldéhydes et les cétones mais est incapable de réduire les
esters, alors que
4
LiAlH
est tellement puissant qu’il réduit indifféremment les aldéhydes, les cétones et même
les esters.
Document 9 : réductions du composé A par LiAlH4 et NaBH4
On ne souhaite pas réduire la fonction carbonyle de la molécule A, par contre on veut réduire sa fonction
ester : il faut donc protéger la fonction carbonyle afin que seule la fonction ester réagisse avec
4
LiAlH
(ici le
borohydrure de sodium ne sert à rien car il est incapable de réduire la fonction ester).
Pour protéger cette fonction carbonyle :
Étape 1 : on fait réagir la molécule A avec l’éthane-1,2-diol ;
Étape 2 : la fonction acétal créée à la place du carbonyle est insensible à
4
LiAlH
, on peut donc réduire le
groupe ester uniquement ;
Étape 3 : on rétablit la fonction carbonyle.
O
HO
O
O O
HO OH
H
O O
O
O
LiAlH4
HO
O
O
H2O H
Document 10 : protection du groupe carbonyle pour la synthèse de B
Un groupe protecteur est un groupe caractéristique volontairement créé dans la molécule d’un
composé polyfonctionnel afin de bloquer la réactivité de l’une de ses fonctions.
Cette fonction est temporairement transformée en une autre fonction.
Voir activité documentaire 6 page 496.
O
O O
LiAlH4
OH
HO
O
O O
NaBH4
OH
O O
 6
6
1
/
6
100%