Lumièressurlesneurones

Lumières sur les neurones
neurosciences |
De nouvelles techniques d’imagerie permettent de visualiser de grandes populations
de cellules nerveuses, en trois dimensions, et de mieux caractériser leurs interactions
David Larousserie
D
ésormais, dire que
l’on voitle cerveau
en activité ne sera
plus un abus de lan-
gage. En effet, les
techniques habi-
tuelles d’imagerie du cerveau com-
plet n’utilisaient jusqu’alors pas vrai-
ment l’arsenal habituel de l’optique:
lumière, lentilles ou caméras. Ainsi,
l’électroencéphalographie(EEG)enre-
gistre des signaux électriques, et
l’imagerie par résonancemagnétique
(IRM) mesuredes perturbations élec-
tromagnétiques.
Mais plusieurs équipes ont montré
récemment qu’il est enfin possible,
dans le domaine visible, d’avoir accès à
un cerveau complet, in vivo ou in
vitro, àl’échelle d’un seul neurone et
en trois dimensions. Deux d’entre
elles, indépendamment, ont enregis-
tré l’activité de dizaines de milliers de
neurones d’un vertébré vivant, le pois-
son-zébre. Une troisième aobservé la
totalité du cerveau excisé d’une souris.
Ce n’est enpratique pas simpled’uti-
liserla lumière pour observercescellu-
les. Le crâne constitue déjà un obstacle
infranchissable. En outre, àcause de la
diffusion de la lumière sur les lipides
omniprésentsdans les cellules, celle-ci
ne peut guère pénétrer profondément
dansla matière biologique.Destechni-
ques de microscopie permettent de
s’affranchiren partiede cettecontrain-
te, mais elles ne sondent qu’un seul
point àlafois pour quelques centaines
de neurones, ce qui les rend peu utiles
pour saisir les communications entre
aires cérébrales. On peut aussi obser-
ver l’échantillon en 3D, mais en le
découpant tranche par tranche…
C’est donc plusieurs tours de force
qu’ontréalisés ceschercheurs.Plus pré-
cisément, les Américains de l’Institut
médical Howard-Hughes (Virginie)
ont photographié 80 000 neurones
d’une larve de poisson-zébre, soit 80 %
du cerveau, avec un cliché toutes les
1,3seconde, comme ils l’expliquent
dans Nature Methods en ligne le
18mars.
De leurcôté, les Français del’univer-
sité Pierre-et-Marie-Curie, de l’Ecole
normalesupérieure, duCNRSetdel’In-
serm se sont limités à30% de ce cer-
veau. Mais avec des images toutes les
200 millisecondes, ce qui permet
d’étudier la dynamique des processus
cérébraux, comme ils l’exposent dans
le journal Frontiers in Neural Circuits
du 9avril.
Les techniques sont identiques
même si elles portent des noms diffé-
rents. Il s’agit d’exciterpar une lumiè-
re laser bleue des molécules fluores-
centes qui réagissent àl’arrivée de cal-
cium dans les neurones àlasuite
d’une décharge nerveuse. La lumière
émise est recueillie dans l’objectif
d’une caméra. En fait, seul un plan de
quelque 5micromètres d’épaisseur,
contenantenviron 5000 neurones,
est éclairé par le laser, le microscope
observant à90degrés la fluorescence.
Le poisson, piégé dans un gel, est auto-
matiquement déplacé afin d’éclairer
une nouvelle tranche, et ainsi de suite.
Ces«découpages»virtuelssontensui-
te rassembléspour former l’image tri-
dimensionnelle du cerveau.
«Cen’est pas un exploit, mais il fal-
lait avoir l’idée d’associer deux techni-
ques, celle des sondes calciques et celle
dite des nappes de lumière »,assure
modestement Georges Debrégeas, de
l’universitéPierre-et-Marie-Curie.«Ce
principe d’imagerie remonte à1903, et
il aété redécouvert en 2004 pour suivre
le développement de l’embryon du
poisson-zèbre»,rappelle Emmanuel
Beaurepaire, du Laboratoire optique
et biosciences àl’Ecole polytechnique,
spécialiste de ce genre de microscopie.
Alors que l’IRM ne repère que des
zones d’une centaine de neurones, ici,
chaque neurone peut être identifié et
son activité corrélée àcelle de ses voi-
sins. L’inconvénient est que cette ima-
gerie ne fonctionne que sur des cer-
veaux de petite taille –que la lumière
peut entièrementpénétrer –ettrans-
parents.
C’est ce problèmequ’une troisième
équipe arésolu aux Etats-Unis. Dans
Nature du 11 avril, Karl Deisseroth
explique comment il arendu un cer-
veau de souris transparent au point
d’identifier chaque neurone, même
lesplusprofondément enfouis. «Cette
idée peut révolutionner la capacité à
voir de gros volumes. La méthode est
élégante et inventive »,déclare Jean
Livet, de l’Institut de la vision, àParis.
L’idée générale, brevetée, est d’ôter les
lipides qui rendent opaque le cerveau.
Mais comme les lipides constituent
les membranes des cellules, cela
détruit généralement la structure
qu’on cherche àvoir. Les chercheurs
ont donc d’abord figé cet échafaudage
en injectant de l’acrylamide, qui, après
chauffage,formeungel polymèrepro-
tecteur. Un détergent détruit alors les
lipides tout en préservant les synap-
ses, les axones ou même l’ADN (seules
8%desprotéinessont perdues). La sui-
te est plus classique, qui consiste àuti-
liser des molécules fluorescentes et à
les photographier, ycompris par la
technique des nappes de lumière.
«Ces techniques pourraient permet-
tre de connaître l’architecture du
réseau de neurones. Soit de manière
fonctionnelle dans des cerveaux
vivants, comme nous le faisons, soit de
manière structurelle, dans les cerveaux
excisés,comme chezDeisseroth »,expli-
que Georges Debrégeas. Il devient en
effet possible de voir pour la première
fois quel neurone est connecté àquel
autre, comment se forment les unités
fonctionnelles de quelques neurones,
comment celles-cis’agrègent ensuite.
Ou comment le réseau évolue au cours
du développement, du conditionne-
ment…Les deux équipessurle poisson-
zèbre vont maintenant stimuler leur
cobaye pour comprendre, en obser-
vant ces milliers de petits points lumi-
neux, comment l’information senso-
rielle se propage àtravers le cerveau.
Quant àlarecette rendant le cer-
veau transparent, elle est la seule à
pouvoir fournir une carte complète
pour les gros cerveaux. Idéal pour
mieux interpréter les enregistre-
ments d’activités cérébrales ou pour
améliorer les techniques dites opto-
génétiques, quipermettent de contrô-
lerl’activitédes neuronespar la lumiè-
re et dont Karl Deisseroth est juste-
ment le pionnier.
p
Vers la fin de la malédiction du week-end pour les AVC ?
La surmortalité due aux accidents vasculaires cérébraux de fin de semaine disparaît avec une prise en charge mieux organisée
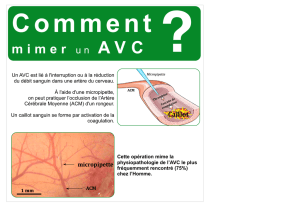
Vue tridimensionnelle de l’hippocampe d’un rat de 3mois, obtenue par une préparation rendant le cerveau transparent.
Les couleurs correspondent àdifférents marqueurs biologiques qui permettent de distinguer les neurones.
KWANGHUN CHUNG AND KARL DEISSEROTH, HOWARD HUGHES MEDICAL INSTITUTE/STANFORD UNIVERSITY
SCIENCE &TECHNO
actualité
Sandrine Cabut
C
’est une conséquence du
week-end dont les
patients se passeraient
bien. Ces dernières
années, plusieurs études ont éta-
bli que les accidents vasculaires
cérébraux (AVC) survenant en fin
de semaine ou un jour férié sont
plus meurtriers que ceux se décla-
rant un jour ouvrable.
Cet «effet week-end», constaté
aussipour les infarctus du myocar-
de, relèverait de plusieurs causes:
moindre accessibilité àdes servi-
cesspécialiséscesjours-là, prise en
charge de moins bonne qualité du
fait d’effectifs hospitaliers réduits,
et peut-être formes plus sévères.
Mais le constatn’est pas irrémédia-
ble, comme le montre une étude
française, publiée le 3avril en ligne
dans la revue European Journal of
Neurology.Les effets délétères du
week-end et desjours fériés sur la
mortalité précoce des AVC dispa-
raissent complètement lorsqu’est
mise en place une organisation
vouée àlaprise en charge de ces
pathologies, concluent Yannick
Béjot (neurologue au CHU de
Dijon) et ses collègues.
Alabase de leur travail, les don-
nées du Registre dijonnais des acci-
dents vasculaires cérébraux, qui
collectedefaçonexhaustivedepuis
1985 tous les AVC survenant dans
cette ville de 150 000habitants.
Au total, 5864 cas ont été recen-
sés entre 1985 et 2010, dont 25 %
sont survenus pendant un week-
end ou un jour férié. Les caractéris-
tiques et la gravité de ces accidents
vasculairesse sont révéléescompa-
rables, qu’ils se déclarent un jour
de semaine ou non ouvrable.
Leschercheurs ont ensuitecom-
paré le devenir des patients selon
qu’ils ontété pris en charge avant
ou après 2004. C’est en effet àpar-
tir de cette date qu’à Dijon la prise
en charge des AVC s’est structurée
autour d’une filière de soins, avec
création d’une unité hospitalière
spécialisée, dite neurovasculaire.
Les résultats sont démonstra-
tifs. Dans la première période
(entre1985 et 2003), la mortalité
trentejours après l’AVC était en
moyenneà14%si celui-ci était sur-
venu un jour ouvrable, à18% s’il
s’était déclaré un jour férié ou de
week-end. Entre2004 et 2010, ce
taux de mortalité est évalué à
8,3%, quelque soitlejourdesurve-
nue de l’AVC.
Filière spécialisée
«Notre étude permet deux types
de conclusions,explique Yannick
Béjot. D’une part, elle confirme que
le pronostic vital des accidents vas-
culaires cérébraux s’améliore ces
dernières années, une évolution
due notamment au meilleur état
de santé des patients. D’autre part,
elle montre que l’injustice de la sur-
mortalité du week-end peut être
combattue par une meilleureorga-
nisation de la prise en charge.»
ADijon, la création de la filière
spécialisée aaugmenté sensible-
ment le nombre de patients traités
par fibrinolytiques. Ces médica-
ments, qui permettent de dissou-
dre le caillot, sont un facteur essen-
tiel du pronostic des AVC. Ils doi-
vent être administrés dans les qua-
treheures trente suivantl’accident.
«C’est tout àfait le type de don-
nées qui viennent àl’appui de la
volonté du plan gouvernemental
d’organiserlaprise en charge des
AVC sur le territoire,commente le
professeur Mathieu Zuber, chef du
service de neurologie du groupe
hospitalier Saint-Joseph (Paris) et
ancien président de la Société fran-
çaise neurovasculaire. Ce plan pré-
voit la création de 140 unités neuro-
vasculairesd’icià2014, nousensom-
mes actuellement àenviron 120.»
Une autre étude, également
publiée en ligne dans European
Journal of Neurology,a,elle,évalué
le coût de priseencharge des AVC
en France. Selon Karine Chevreul
(hôpital Henri-Mondor, Créteil), il
s’élevait au total à5,3 milliards
d’euros en 2007, avec un coût
moyen de l’ordre de 17 000 euros
par patient la première année.
p
Il devient possible de voir,
pour la première fois,
quel neurone est
connecté àquel autre
Illuminer la tumeur pour mieux la cerner
G
râce àdes techniques innovantes d’imagerie cel-
lulaire, les neurochirurgiens peuvent repérer
directement des cellules cancéreuses pendant
l’intervention et optimiser un geste d’ablation d’une
tumeur cérébrale. Ainsi, la chirurgie des glioblastomes
(tumeurs malignes primitives du cerveau les plus fré-
quentes) peut être guidée par fluorescence, grâce àl’aci-
de 5-aminolévulinique (5-ALA), une molécule métabo-
lisée électivement dans ces cellules tumorales.
Classiquement, les glioblastomes sont opérés sous
microscope avec un système de neuronavigation qui, tel
un GPS, permet au chirurgien de se repérer àpartir des
clichés d’IRM préopératoires. En ajoutant une technique
de fluorescence, le but est d’aller chercher les cellules
tumorales résiduelles, systématiquement retrouvées
dans ce type de tumeur, pour compléter l’acte chirurgi-
cal et améliorer le pronostic. En pratique, le patient ingè-
re la solution de 5-ALA six heures avant l’intervention.
«Lafluorescence est visualisée sur un microscope classi-
que sur lequel est ajouté un module spécial qui filtre les
UV àune longueur d’ondes déterminée,précise le profes-
seur Philippe Metellus (CHU de Marseille), qui aopéré
plusieurs patients avec cette technique. Le 5-ALA est déjà
commercialisé mais pas remboursé. Une étude randomi-
sée, qui débute dans 16 centres français, va comparer ses
résultats àceux de l’approche classique sur le plan médico-
économique. Au total, environ 300 patients seront
inclus.» D’autres approches comme l’élastométrie, qui
détecte des cellules tumorales en fonction de leurs carac-
téristiques physiques, sont en cours d’exploration en
neurochirurgie, àdes phases plus préliminaires.
p
S. Ca.
20123
Samedi 20 avril 2013
1
/
1
100%