03 September 2011 - Basel Declaration

La maladie d‘Alzheimer
La maladie d‘Alzheimer (AD) est avant tout une ma-
ladie des personnes âgées; sa prévalence augmente
de manière presque exponentielle avec le vieillis-
sement de la population. L’AD prive les personnes
atteintes de leur mémoire, de leur personnalité, de
leur autonomie et de leur contexte social. La lente
progression de la dévastation personnelle est éga-
lement réfléchie par la charge financière imposée
aux états du monde entier. Ainsi, pour 2008, les dé-
penses du régime d’assurance maladie américain
pour la maladie d‘Alzheimer ont atteint $94 milli-
ards, un tiers de son budget total. Actuellement, il
n’existe pas de médicament commercialisé ralen-
tissant ou arrêtant la progression de la maladie. Les
médicaments disponibles traitent les symptômes,
mais uniquement de manière provisoire.
Les compagnies pharmaceutiques font des ef-
forts importants pour essayer de sortir pour l’AD un
médicament modifiant la maladie. Mais au cours de
cette dernière décade, nous avons assisté à une série
d‘échecs dans la phase finale des études de phase 3.
Les raisons de ces échecs sont multiples et peuvent
inclure le choix de la mauvaise cible moléculaire
sous-jacente.
Alors que la plupart des efforts de recherche se
sont focalisés sur l’amyloïde, une nouvelle appro-
che a ciblé l’autre pathologie-clé, les emmêlements
neurofibrillaires déjà décrits par le Dr Alois Alzhei-
mer en 1906. Ce n’est toutefois que dans les années
1960 que l’équipe de Sir Martin Roth a indiqué la
corrélation entre la charge des emmêlements et le
degré clinique de démence. La nature et la compo-
sition de ces emmêlements a été déterminée après
leur isolation et leur purification opérée par Clau-
de Wischnik dans les années 1980. Ils sont à base de
protéine tau, une protéine absolument essentielle
pour la forme des neurones et le transport «cargo»
le long des axones connectant les réseaux nerveux
et le cerveau. Toute accumulation anormale de pro-
téine tau dans les neurones est étroitement liée aux
signes cliniques de démence et à la dégénérescence
neuronale.
L‘évolution de la pathologie tau (tauopathie) suit un
schéma caractéristique dans la durée, qui a été dé-
couvert et décrit pour la première fois en 1991 par les
neuropathologues allemands, Heiko et Eva Braak,
et qui est depuis communément appelé stades de
Braak. La tauopathie démarre dans l’hippocampe et
le cortex entorhinal, une région importante pour la
mémoire et l’apprentissage chez les souris et chez
les humains. Avec la progression de la maladie, les
emmêlements s’étendent sur le cortex temporal,
pariétal et frontal. Cette extension caractéristique
de la pathologie d’agrégation tau semble, post-mor-
tem, correspondre étroitement au schéma régional
des déficits cérébraux pouvant être démontrés intra
vitam par des scans fonctionnels du cerveau, mesu-
rant soit la réduction du flux sanguin, soit la réduc-
tion de l’utilisation du glucose (SPECT ou PET). De
tels déficits correspondent à la progression clinique
de l’AD, qui peut être suivie à l’aide de batteries de
tests neuropsychologiques variés.
# 03 | September 2011
Nouvelles percées concernant la maladie
d’Alzheimer avec des souris transgéniques
L’ÉCHO DES SOURIS
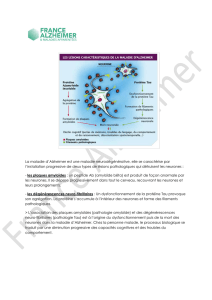
Fig. 1: Représentation schématique de l’évolution de la pathologie tau
neuronale
Nucleus
Emmêlement
Emmêlement
«fantôme»
Plaque nerveuse
Agrégats de
protéine tau
Neurone sain

En 1991, l’équipe de John Hardy à Londres a rapporté
qu’une mutation génétique menait à l’AD chez les
patients ayant des antécédents familiaux de la mala-
die. La mutation touchait une protéine produisant
un fragment d’amyloïde insoluble s’accumulant
sous forme de «plaques» dans le cerveau, en dehors
des neurones, ce qui correspond à l’autre patholo-
gie évidente déjà décrite par Alois Alzheimer. Ceci
a donné naissance à ce qui est appelé l’hypothèse de
la cascade amyloïde, dans laquelle le processus me-
nant à l’accumulation d’amyloïde dans les plaques
a été mis au centre du processus de développement
de la maladie. Cette hypothèse doit toutefois en-
core être confirmée par une étude clinique réussie.
Braak et Braak ont montré que la pathologie amy-
loïde semble être une caractéristique générale du
cerveau vieillissant qui ne suit pas de schéma défini
de progression ou d‘extension. Une relation systé-
matique tout au plus minimale entre la pathologie
amyloïde et la dégénérescence cognitive clinique a
été confirmée depuis. Il est intéressant de noter que
les plaques «névritiques» de l’AD contiennent éga-
lement des terminaisons nerveuses montrant en
abondance les mêmes fibrilles que celles retrouvées
dans les emmêlements
L’agrégation de protéine tau
Pour pouvoir développer des médicaments suscep-
tibles d’arrêter le processus de l’agrégation de
la protéine tau menant aux emmêlements dans
les cerveaux AD, il faut disposer d’un modèle per-
mettant de tester ces médicaments. Wischnik et ses
collaborateurs ont développé de tels modèles afin
de montrer qu’une classe de composés peut inhi-
ber l’agrégation tau dans un tube d’essai, une cel-
lule isolée puis dans un modèle murin. Tant dans
le modèle cellulaire que dans le modèle murin, le
processus de l’agrégation tau a été initié par une
petite semence capturant ensuite la protéine tau
et menant à un complexe stable et insoluble de tau
agrégée. On ne comprend pas encore ce qui lance le
processus dans le cerveau humain, mais il semble
probable qu’il puisse y avoir différents évènements
susceptibles de déclencher ce processus. Dans cer-
tains cas, il s’agit peut-être d’amyloïde anormale ou
de l’accumulation de protéines anormales ou en-
core de «pigment de vieillissement». Une fois initiée,
la capacité d‘autopropagation de la pathologie par
la protéine tau aux dépens de la protéine tau nor-
male a été confirmée dans plusieurs études récen-
tes. Les fibrilles tau agrégées peuvent être absorbées
par des cellules contenant de la protéine tau longue
et transmises aux cellules voisines, propageant ainsi
l’agrégation. La transmission et l’extension de la pa-
thologie tau peuvent être induites de manière simi-
laire dans des modèles murins.
Une fois l’ensemencement initial réalisé, la cas-
cade de l’agrégation tau est autopropagatrice, me-
nant à deux résultats préjudiciables. Elle convertit
d’abord la protéine tau fonctionnelle normale du
neurone en sa forme agrégée retrouvée dans les em-
mêlements. La protéine tau normale est nécessaire à
la stabilisation des microtubules axonaux. Le réseau
microtubulaire contribue à la forme du neurone
avec la longueur d’axone requise pour la connexion
de deux parties distantes du cerveau. Mais le point
le plus important est que les agrégats de tau sont di-
rectement neurotoxiques et entrainent la mort neu-
ronale.
Inhibiteurs de l’agrégation de la protéine tau
Le chlorure de méthylthioninium (MT), communé-
ment appelé bleu de méthylène, a été le premier
inhibiteur de l’agrégation tau rapporté. Les con-
centrations de MT efficaces dans la désorganisati-
on des emmêlements in vitro et dans les modèles
«Toute accumulation anormale de protéine tau dans
les neurones est étroitement liée aux signes cliniques
de démence et à la dégénérescence neuronale.»

cellulaires sont liées aux concentrations inoffensi-
ves chez les humains. Ceci nous mène à la question
d’une possible utilisation de MT sans danger et effi-
cace dans l’AD.
Deux modèles murins ont donc été dévelop-
pés, démontrant en premier lieu que l’agrégation
tau provoque des déficits sur le plan cognitif et
d’apprentissage moteur et, deuxièmement, que la
pathologie tau se développe au sein des neurones,
le processus étant organisé de manière similaire à
la neuropathologie humaine. Ces modèles murins
ont confirmé que le MT: (a) passe la barrière hémato-
encéphalique; (b) entraine une modification du phé-
notype clinique (fonctions cognitives et apprentissa-
ge moteur); (c) réduit la charge de tau oligomérique
dans des régions importantes pour la mémoire.
Génération de souris transgéniques
Des oocytes fertilisés ont été prélevés de souris fe-
melles âgées de quatre semaines. Le vecteur, con-
tenant la séquence de codage de la protéine tau
(ADNc de tau) sous le contrôle d’un promoteur neu-
ronal Thy-1, a été microinjecté dans le pronucléus
mâle des oocytes fertilisés. Après la microinjection,
les oocytes ont été implantés dans l’oviducte de
souris femelles NMRI pseudogestantes âgées de 8 à
10 semaines. Les souris transgéniques ont été iden-
tifiées par génotypage en utilisant la PCR (réaction
de polymérase en chaîne) afin d’identifier la pré-
sence d’ADN de tau inséré spécifiquement humain.
Le nombre de copies d’inserts a été déterminé par
Southern blot. L’expression de l’ARNm de tau par
Northern blot et de protéine tau a ensuite été déter-
minée par immunoblots et une analyse immuno-
histochimique des tissus cérébraux.
Dans le premier modèle transgénique, la souris
«lignée 1» exprime un fragment de tau formant
l’unité centrale au sein des filaments individuels de
l’emmêlement Alzheimer. La conception de la prot-
éine lui permet de se fixer à un endroit de la mem-
brane où elle enclenche un ensemencement de tau
pouvant capturer d’autres protéines tau. Ces souris
récapitulent le phénomène essentiel des stades de
Braak. Chez les souris de moins de 12 mois, la pa-
thologie de tau agrégée est principalement localisée
dans le cortex endorhinal et l’hippocampe. Lorsque
la souris vieillit, la pathologie s’étend aux autres ré-
gions corticales du cerveau. Ces souris de la lignée
1 développent une altération de l’apprentissage
après l’âge de 7 mois, ainsi que montré dans la
tâche du labyrinthe aquatique. L‘acquisition d’un
d’apprentissage donné exige presque le double
du nombre d’essais chez les souris de la lignée 1,
mais l’administration orale de MT inverse ce déficit
d’apprentissage tout en réduisant la charge de tau
oligomérique.
Le MT montre également des effets positifs dans
un deuxième modèle murin («lignée 66»). Chez cette
souris, la protéine tau humaine a été modifiée par
des mutations accélérant l’agrégation tau. Ces mu-
tations se retrouvent en fait dans un autre type de
démence, la démence frontotemporale, où les symp-
tômes primaires concernent plus souvent des chan-
gements du comportement que de la mémoire. Alors
que la souris de la lignée 1 montre une pathologie
tau très modeste, la souris de la lignée 66 montre
une pathologie tau sévère. Les emmêlements de tau
chez les souris de la lignée 66 sont filamentaires et
sont observés dans l’hippocampe, le cortex endorhi-
nal et d’autres régions corticales.
Ovules implantés
Pronuclei d’oocyte
Génération de souris tau transgéniques
ADNc de tau humain injecté
dans le pronucléus d’ovules
fertilisés avant la fusion en
pronuclei mâle/femelle
Expression de tau dans
le cerveau
Souris procréée avec
ADNc de tau
Fig. 2: Génération de souris tau transgéniques
Neurones
tau-positifs
300
200
100
MT
(ng/kg/jour)
45150
Fig. 3: Réduction dose-dépendante de la charge de tau neuronale
chez les souris après l’administration de MT

«Les effets du méthylthioninium chez les
souris tau transgéniques ont eu un rôle décisif
dans l’encouragement de la recherche clinique»
Il serait souhaitable de pouvoir comprendre les mécanismes complexes
de l’organisme sans expérimentation stressante pour les animaux.
Ce n’est malheureusement pas encore le cas aujourd’hui bien que les
chercheurs pratiquent déjà depuis bien des années d’innombrables
expériences sur des cellules et des tissus et, à l’époque de la biologie
des systèmes, acquièrent de plus en plus de connaissances grâce aux
simulations sur ordinateur. Le dilemme persistera encore longtemps:
pratiquer la recherche fondamentale sans essais sur des animaux
signifierait renoncer à tout progrès médical. «L’Écho des souris» veut
expliquer pourquoi et, à cette fin, relate des réussites médicales qui
n’auraient pas été possibles sans l’expérimentation animale.
«L’Écho des souris» est une collaboration avec la «Déclaration de Bâle».
www.basel-declaration.org
IMPRESSUM
Herausgeberin in Cooperation:
www.basel-declaration.org
Münchhaldenstrasse 10
Postfach
8034 Zürich
www.forschung-leben.ch
www.recherche-vie.ch
Autor:
Hans J. Moebius, MD, PhD, ECPM
Redaktion:
Astrid Kugler «Forschung für Leben»
Barbara Moebius «Forschung für Leben»
Les souris de la lignée 66 montrent de sévères anor-
malités de l’apprentissage moteur. L’administration
orale de MT peut inverser ce déficit tout en rédui-
sant la charge de tau.
Le MT peut donc inverser les symptômes et la
pathologie dans deux modèles de souris tau trans-
géniques: un modèle de phénotype cognitif avec
prédominance d’oligomères de tau (lignée 1) et un
phénotype moteur de type frontotemporal avec
abondance de tau filamentaire (lignée 66). Les ef-
fets du MT chez les souris tau transgéniques ont été
décisifs dans l’encouragement de la recherche cli-
nique.
La recherche translationnelle dans la maladie
d‘Alzheimer
Le concept d’inhibition de l’agrégation de tau a été
confirmé par des résultats provenant d’une étude
clinique contrôlée portant sur 321 patients souf-
frant d’AD. Le MT a significativement réduit le taux
de déclin cognitif clinique de 84% sur 50 semaines
lorsque mesuré à l’aide de l’échelle ADAS-cog, un
instrument validé et accepté de l’enregistrement
des changements cognitifs dans l’AD. Le critère
d‘évaluation clinique global coprimaire et les résul-
tats d’une sous-étude SPECT étaient significative-
ment positifs. Ces résultats suggèrent que le MT peut
ralentir la détérioration dans l’AD. L’administration
de MT pourrait donc être particulièrement utile aux
stades précoces de la maladie. Une forme améliorée
de MT doit bientôt être testée dans des études de
phase 3. La confirmation clinique et par imagerie
neurologique de ces conclusions initiales est atten-
due avec impatience, afin de voir si le principe d’une
thérapie ciblant la protéine tau peut offrir un nou-
vel espoir dans le traitement de l’AD.
1
/
4
100%










![Découverte d`une [autre] planète potentiellement «habitable»](http://s1.studylibfr.com/store/data/000497995_1-d61d34a4566713f9044969f5bc070e9b-300x300.png)