Télécharger le diaporama

!"##$%"&$'% ()* +& (',&
&)"%,(-"%&"&$'%
!"##$% $& '()$ *+,-! ./01
!"#$%&'()#(*+,,-./*#0/+.(+%#)1(21
34(3+%2+../1%5(6.71*0/+-' 3+,$)/*#0/+.(81''/+.
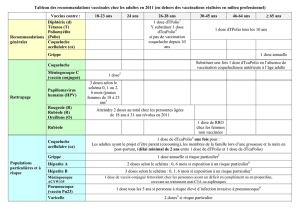
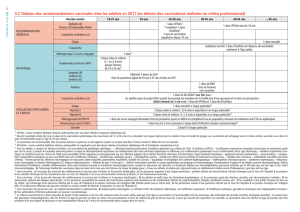
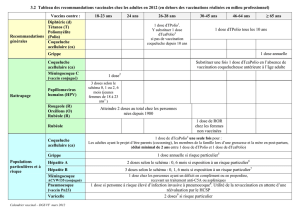
9:;<(=>?@(A==B=@(;#%'(=>?@
CD2/ED($#%()1(!+*01-%(;#F)(G96:H6I(J31.0%1(G+'$/0#)/1%(21(HK+.(8-2(5(HK+.L

!"#$%&'(#)%"
*%+,$-.($%)//0"#.&-.10#)-"#/.#$0"/120"#3/.4
5#$0"/120"#0#)%".&6%$70"-./%2)&-.
57$-88-.&-.+%-22-.4.0'#%9.022%7$-88-
!++'"%&31$-//)%".4.$)/:'-.0(($'.&6)"8-(#)%"/.-#.&6)"8-(#)%"/.
/3;<$-/.0;-(.+)/-.-".=-'.&'.1$%"%/#)(.;)#02
>0(()"0#)%".4.1$3;-"#)%".&-/.)"8-(#)%"/9.1-$+-#.-".(0/.
&6-?1%/)#)%".'"-.&)+)"'#)%".&-.20.$312)(0#)%".-#.&-.20.
&)//3+)"0#)%".&-.2607-"#.)"8-(#)-'?.
@intérêt'particulier'de'la'vaccination'chez'le'transplanté
.
CD2/ED($#%()1(!+*01-%(;#F)(G96:H6I(J31.0%1(G+'$/0#)/1%(21(HK+.(8-2(5(HK+.L

!"#$%&'(#)%"4.
A".(-$#0)"/."%+,$-.&-.:'-/#)%"/.B
!"#-"/)#3C&)+)"'#)%".&-.26)++'"%73")()#3.-".10$#)('2)-$.D.
2%"7.#-$+-9.&)+)"'#)%".&-.26-88)(0()#3.E
F-;-")$.&-.26)++'"%73")()#3.;0(()"02-.1$35
#$0"/120"#0#)%".01$</.20.#$0"/120"#0#)%".E
>0(()"-$.&)883$-++-"#./-2%".20.#$0"/120"#0#)%".E
>0(()"0#)%".1$357$-88-.%'.;0(()"0#)%".&'.&%""-'$.E
!""%(')#3.&-.20.;0(()"0#)%".(G-H.(-/.10#)-"#/.5 $)/:'-.&-.
/'$;-"'-.&-.+020&)-.;0(()"02-.I;0(()"/.;);0"#/J.5 $)/:'-.
&-.$-=-#.E.
2
CD2/ED($#%()1(!+*01-%(;#F)(G96:H6I(J31.0%1(G+'$/0#)/1%(21(HK+.(8-2(5(HK+.L

KL.!++'"%73")()#3 &-.20.$31%"/-.;0(()"02-.
(G-H.2-.#$0"/120"#3
Une'des'difficultés'majeures'est'd’évaluer'l’efficacité'de'la'réponse'
vaccinale'chez'le'transplanté:'
M2)"):'-+-"#.4.F)+)"'#)%".&-.26)"()&-"(-.&6'"-.10#G%2%7)-.)"8-(#)-'/-
N)%2%7):'-+-"#.4 F)883$-"#-/.1%//),)2)#3/.1%'$.-?1$)+-$.2-/.");-0'?.
&6-?1$-//)%".&-.#)#$-.&60"#)(%$1/.-#.2-'$/.8%"(#)%"/.4
5O%P-""-.73%+3#$):'-.&-/.(%"(-"#$0#)%"/.IOQMJ.&60"#)(%$1/
5R'7+-"#0#)%".&-.20.OQM.0;0"#C01$</.SMT
5U.&-.10#)-"#/.-".&-//%'/.&'./-')2.C.V ('#5%88 W.(%""'.(%++-.1$%#-(#-'$.
(G-H.2-/./'=-#/.)++'"/.4.-/#5(-.1$%#-(#-'$.(G-H.2-.10#)-"#.#$0"/120"#3.E
5T-/#/.8%"(#)%""-2/.I%1/%")/0#)%"9.1G07%(P#%/-J
MG$%"%2%7):'-+-"#.4.X'0"&.3;02'-$.20.$31%"/-E.I-".73"3$02.Y5Z.
/-+0)"-/.1%/#5;0(()"0#)%"J
3
CD2/ED($#%()1(!+*01-%(;#F)(G96:H6I(J31.0%1(G+'$/0#)/1%(21(HK+.(8-2(5(HK+.L

Haemophilus,Influenza,N.01$</.RSMT
M0'/-.&-./)"'/)#-/9.,$%"(G)#-/9.1"-'+%")-/9.0//%()3-/.D.&-/.#0'?.
&60"#)(%$1/.0"#)5[\[.,0/.I1$3;02-"(-.;0$)0,2-.&0"/.2-/.10P/.
-'$%13-"/J
>0(()"0#)%".(%"#$-.Haemophilus Influenza,B4
5>0(()".(%"='7'3.].1%2P/0((G0$)&):'-.IN0$$0.-#.02L.K^^_J
5F-'?.&%/-/.8%"#.+)-'?.:'6'"-.IN0$$0.-#.02L.K^^_9.R;0"H0") -#.02L.
K^^ZJ
5T0'?.&-.$31%"/-.4.85%'après'2'doses
5!++'")/0#)%".1$3(%(-.IY.+%)/J.].$-#0$&3-.IK_.+%)/J.I>0"(- K^^`J
1
CD2/ED($#%()1(!+*01-%(;#F)(G96:H6I(J31.0%1(G+'$/0#)/1%(21(HK+.(8-2(5(HK+.L
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%