Anémie infectieuse des équidés: bilan de l`épisode varois de 2009

Le 31 mars 2009,lelaboratoire nationalderéférence(LNR)de
l’anémie infectieuse deséquidés de l’Anses–Laboratoire de pathologie
équine de Dozulé -informaitladirectiongénéraledel’alimentation
de la confirmation d’un cas d’anémie infectieuse deséquidés (AIE)
diagnostiqué sur unejumentmaladeadmisedans uneclinique
vétérinaire desAlpes-Maritimes.Cecas aété àl’originedelamise
en évidencedufoyerleplusimportant identifiédepuisledébut des
années2000.Dans cet articleles résultats obtenussuite auxenquêtes
épidémiologiques réalisées sur le terrainainsi queles données
d’épidémiologiemoléculaire obtenues àpartir dessouches d’AIE isolées
dans cesfoyers sontprésentés.
L’anémie infectieuse
Le virusdel’anémie infectieuse deséquidés (EIAV) est l’agentétiologique
de l’AIE.Ilappartientàlafamille des Retroviridae,genre Lentivirus.La
formeclinique de la maladieaété décrite pour la première fois en
Franceen1843[1] et ce n’est qu’en1904que l’origineinfectieuse de
la maladieaété démontrée.Les signescliniques associésàl’infection
apparaissentaprès unepériode d’incubation variantd’une semaine à
21 joursenfonctiondustatut immunitaire de l’hôte ainsique de la
charge virale lors de l’infection. Ilssecaractérisentprincipalementpar
de la fièvre, de l’anémie,des œdèmesetdifférentssignesd’abattement.
Suiteàl’infection, plusieursformescliniques pouvantsesuccéder,sont
rencontrées: uneforme diteaiguë où l’équidéprésente dessignes
cliniquesgravespouvantconduire àsamort, uneforme chronique
quisecaractérise parune récurrencedes phases cliniques(fièvre,
anémie, abattement…)etenfin uneforme asymptomatique [2,3].
Leséquidés infectés n’éliminentjamais le virusetrestentdonc des
sources de contagionpourleurs congénères même en l’absencede
signescliniques [4]. Lesanimaux en phaseasymptomatiquepeuvent
développer dessignescliniques sous l’effetdustress. La transmission
virale d’un animal àl’autre se produitprincipalementpar le sang,par
l’intermédiairedepiqûres d’insectes ou selon un mode iatrogène lors
de l’utilisation d’aiguillesoudematérieldentaire nonstériles[5,6].
Lesinsectes, essentiellementdes taonsetdes stomoxes, servent de
vecteursmécaniques(le virusnesemultiplie pasdans l’insecte) en
conservant le virusinfectieux dans leurspiècesbuccales pendant
quelques heures après la piqûre.Cemode de transmissionfavorisela
disséminationviraleprincipalementlorsderegroupements de chevaux.
L’AIE est unemaladie réglementéedite«réputéecontagieuse »
(MRC)(1) dontles conséquences économiquesetsanitairespeuvent
s’avérer très préjudiciables pour l’ensembledes professionnelsde
la filièreéquine. Le coût économique liéàl’infectionpar l’AIE est
important et s’expliquepar l’euthanasie desanimaux séropositifs(2) le
nombreimportant d’analyses réaliséessuite àladécouverted’uncas
et àl’annulation desmanifestations hippiques.Par ailleurs, l’AIE est
inscrite sur la listedes vicesrédhibitoires(3).
Le diagnostic sérologique de l’AIE est réalisépar un test d’immuno-
diffusionengélose(IDG) (test de Coggins) [7]. Leséquidés ne subissent
pasdecontrôlesystématiqueaucours de leur vie. En effet, le diagnostic
de l’AIE est réglementairementexigé uniquementlorsdel’importation
ou l’exportation d’un équidéetlorsdes contrôlespourlareproduction
chez lesétalons.C’est pourquoi lesfoyers d’AIE sontsouvent détectés
suiteàladécouvertepar un vétérinaire praticiendesignescliniques
évocateurschez un équidédesaclientèle.Cette suspicioninitiale peut
être àl’originedudépistage d’autres équidés séropositifsàproximité,
qu’ils soient maladesouinfectés asymptomatiques.
Assainissementdes foyers
et enquêtes épidémiologiques:
uneactiond’envergure
Le foyerprimaire de 2009 aété déclaré dans un centre équestre situé
sur la communedeCarcès, dans le départementduVar,aumois
Anémie infectieusedes équidés
:bilan de l’épisode
varois de 2009
Aymeric Hans(1), Élodie Morilland(1),FannyLecouturier(1),Claire Laugier(1), Stephan Zientara(2), Anne Chemel(3),
Éric Coulibaly(4),Nicolas Ponçon (5)
(1)Anses, Laboratoire de pathologie équinedeDozulé
(2)Anses, Laboratoire de santéanimaledeMaisons-Alfort
(3)Directiondépartementaledelaprotectiondes populations du Var
(4)Directiondépartementaledelaprotectiondes populations desAlpes-Maritimes
(5)Directiongénéraledel’alimentation (DGAl), bureau de la santéanimale
Résumé
La confirmation d’un casd’anémie infectieuse deséquidés
sur une jumentprésentantdes signes cliniques en 2009
arévélél’épisodeleplusimportantdepuisledébut des
années2000 en France. Avec trois foyers, 16 équidés
infectés, 83 établissements placés sous surveillance dans
quatre départements du sud-est, environ500 chevaux
dépistéset1500dépistagesréalisés, cet épisodesouligne
lesconséquences importantesenmatière de gestion,
économique et judiciairedecette maladie.
Mots clés
Anémieinfectieuse deséquidés, lentivirus, épidémiologie
Abstract
Equine infectiousanaemia:overviewofthe 2009outbreak
in theVar départementof France
Theinitialconfirmationof acase of equineinfectiousanaemia
in 2009 in amarepresenting with clinical signs of thedisease
brought to lightthe mostsignificant episode of EIAsince the
beginningofthe 21st centuryinFrance.Withthree outbreak
sites, 16 infected equids,83sites placedundersurveillance
in four départementsinthe southwestofFrance,and
approximately 500horsesfound positive outofthe 1,500
tested,thisepisodehas shownthatthisdiseasecan have
seriousrepercussions in termsofmanagement as well as on
an economic andlegal level.
Keywords
Equineinfectiousanaemia,lentivirus, Epidemiology
(1)Coderural et de la pêchemaritime,article D. 223-21.
(2)Arrêtédu23septembre1992fixantles mesures de police sanitaire relativesàl’anémie infectieuse deséquidés.
(3)Coderural et de la pêchemaritime,article R. 213-1.
10 Bulletin épidémiologique, santé animale et alimentationN
o39

de mars 2009 après la confirmation de l’infectiond’une jumentde
ce centre.Cette jument(cas index) âgée de 10 ans présentait les
symptômessuivants:hyperthermie, inappétence, anémie importante
(2 000000 d’hématies/mm3), amaigrissement, et asthénie.Elleaété
transférée, le 20 mars 2009,deCarcèsàlacliniquevétérinaire de
Cagnes-sur-Mer dans lesAlpes-Maritimes où unesuspiciond’infection
parl’EIAVaété établie,puisconfirmée le 31 mars 2009.Lajument
aété isolée puis euthanasiéele9avril2009. S’agissant d’uneMRC,
la gestionsanitaire (tableau1) de l’épisode aété réalisée parles
servicesvétérinaires, en relation avec lesprofessionnelsdelafilière
équine.Conformémentàlaréglementation visant àluttercontrela
disséminationdel’AIE en France, l’action desservicesvétérinairesa
consisté parallèlementi)àassainir le foyermis en évidenceetii) à
mener desenquêtes épidémiologiques en amontetenaval du foyer
afin d’identifier l’originedecelui-ci, et d’identifier leséquidés en lien
épidémiologiqueaveccefoyer.
Dans un premiertemps, un arrêtépréfectoral portantdéclaration
d’infection(APDI)aété publiépourl’établissementdeCarcèsoù
étaitdétenulecas index, lui imposant notammentdes mesures de
restrictiondes mouvements et de dépistage deséquidés présents
in situ.Onzeéquidés sur les49détenus dans le centre équestre ont
ététrouvés séropositifs, soit 22 %del’effectifcontaminé, et ontété
euthanasiésle23avril2009.
Lesenquêtes épidémiologiques se sont focalisées sur i) leséquidés
ayantprésenté un contactdirect avec leséquidés infectés –contacts
au coursdesquelslatransmission vectoriellemécanique aurait pu
avoirlieuii) leséquidés présents dans unezonede2km autour du
foyer. L’ensembledes équidés répertoriésetles centresles hébergeant
ontété placés sous arrêtépréfectoral portant mis sous surveillance
(APMS) et soumis àdes mesures de dépistage et de restrictiondes
mouvements.Ces enquêtes ontpermis d’identifier quatre autres
chevauxséropositifs,unsur la communedeCarcèsettrois sur la
communeduPlan-de-la-Tour.Ces deux nouveauxfoyers présentaient
un lien épidémiologiquedirect avec le foyerinitial de Carcèspar achat/
ventedechevaux et utilisation de pâtures communes ou très proches.
In fine,ces enquêtes ontpermis d’éviter uneplusgrandedissémination
du virusdans la population équinelocale.
Au total,16équidés ontété détectés positifspourl’AIE,répartis en trois
foyers dontlefoyerprimaire de Carcèscomprenant lestroisquarts
deséquidés infectés.Ces trois foyers ontété placés sous APDI et 83
établissements répartis dans le départementduVar,des Bouches-du-
Rhône, de la Drôme et desAlpes-Maritimes ontété placés sous APMS,
dont l’hippodrome de Cagnes-sur-Mer.Plusde1500testsdeCoggins
ontété réalisés sur 500équidés environentre mars et décembre2009.
LestroisAPDIont étélevés respectivementenoctobreetendécembre
2009,après assainissementdes foyers.Les APMS ontété levésaprès
achèvementdes mesures de dépistage.
Malgré desenquêtes épidémiologiques exhaustives, l’originede
l’infectionn’a pasété établie aveccertitude. Dans la mesureoùle
foyerprimaire 2009,situé sur la communedeCarcès, avaitdéjà été
placésous APDI en l’an 2000 suiteaudépistage et àl’euthanasie de 36
chevauxséropositifs, trois hypothèsessontenvisagéespourexpliquer
l’apparitiondecas d’AIE dans ce même centre àneufans d’intervalle:
•1) le foyer 2009 pourrait être unerésurgencedecelui de 2000
quin’auraitpas étééradiquésuite àlasoustraction, volontaire ou
non, de chevauxaux analyses;
•2) le foyer2009seraitunévénementnon liéàcelui de 2000 et aurait
uneorigineindépendante, comme l’introductiondenouveaux
chevauxaprès le foyerde2000 et enfin;
•3) unehypothèse résultant de l’additiondes deux premières.
Tableau 1. Chronologie de l’épisodevarois en 2009
DatesÉpisode
20 mars 2010 Jumentâgéede10ans,malade, transportée de Carcès(Var) àlaClinique vétérinaire de l’hippodrome de Cagnes-sur-Mer
(Alpes-Maritimes). Suspiciond’anémie infectieuse deséquidés.
31 mars 2009 Confirmation par le LNRdel’infectiondelajument. Isolementdelajumentinfectée et euthanasie le 9avril2009.
2avril2009PremierAPDIpubliépourlefoyer primaire de Carcèsconcernant49équidés.
5avril2009Malgrél’APDIlepropriétaireorganiseune compétition équestre regroupantprèsde200 chevaux
6avril2009 APMS de zone (4 communes concernées pour 18 équidés de propriétaire), d’un rayonde2kmautourdufoyer,
et dépistage deséquidés concernéspar l’APMS.
23 avril2009Euthanasie de 11 équidés diagnostiquéspositifs dans le foyer primaire.
Avril, mai,juin
et août2009 Dépistagessérologiquesmensuels deséquidés du foyer primaire placés sous APDI.
Avriletmai 2009 Enquêteépidémiologiqueenaval du foyer primaire :34équidés ayantquittélefoyer primaire depuisl’an2000 sontretrouvés et
testés. Parmiceux-ci,deuxéquidés sontdiagnostiquéspositifs,correspondant àdeuxnouveauxfoyersdans le départementduVar.
4mai 2009 Deuxième et troisième APDI publiéspourles deux foyerssecondaires, concernant 12 équidés àCarcèset6équidés
au Plan-de-la-Tour.
12 mai 2009 Euthanasie de trois équidés diagnostiquéspositifs dans lesfoyerssecondaires:un àCarcèsetdeuxauPlan-de-la-Tour.
Mai àoctobre 2009 Dépistagessérologiquesmensuels deséquidés desdeuxfoyerssecondaires.
12 juin2009Euthanasie d’un troisième équidédiagnostiqué positifdans le foyer secondaire du Plan-de-la-Tour.
Avril, mai et juin2009 Àlasuite de l’enquêteépidémiologique, 83 centreséquestresdans 4départements sontplacéssous APMS,
dontplusdes deux tiersdans le Var.
Avrilàoctobre 2009 Dépistage deséquidés «contacts »hébergés dans lescentres sous APMS.
Octobre2009Levée du dernierAPMSdans le Var.
5octobre 2009 Levéedel’APDIsur lesfoyersprimaire et secondaire de Carcès.
7décembre2009Levée de l’APDI sur le foyer secondaire du Plan-de-la-Tour.
Tableau 2. Pourcentaged’homologie de séquencesur le gène
gag
entreles isolats2009issus destrois foyers varois (sur 1400 nucléotides)
Carcès 1
FRAIE09-
83-01
Carcès 1
FRAIE09-
83-02
Carcès 1
FRAIE09-
83-03
Carcès 1
FRAIE09-
83-04
Carcès 1
FRAIE09-
83-05
Carcès 1
FRAIE09-
83-06
Carcès 1
FRAIE09-
83-07
Carcès 1
FRAIE09-
83-08
Carcès 2
FRAIE09-
83-09
Plan-de-la
-Tour
FRAIE09-
83-10
Plan-de-la
-Tour
FRAIE09-
83-11
Plan-de-la
-Tour
FRAIE09-
83-12
Carcès1
FRAIE09-
83-01 100% 97,8 %97,1% 96,8 %98,6% 98,8% 98,3% 98 %97% 98,6% 97,4 %98,7%
Bulletin épidémiologique, santé animale et alimentationN
o39 11

Génotypage desisolats 2009
Afin de réaliser le génotypagedes souchesd’AIE isoléesdes différents
foyers, le séquençagedugène gag,d’une longueur de 1400 nucléotides
environ, aété entrepris.Sur les16équidés diagnostiquéspositifset
répartis en trois foyers, le gène gag de 12 isolatsvirauxapuêtre
amplifié parPCR (AmplificationenChaînepar Polymérase).L’analyse
du séquençagedugène gag des12isolatsrévèleune homologie de
séquenceentre euxsupérieureà97%(tableau2).Les isolatsviraux
issusdes trois foyersduVar sont donctrèsproches et il est probable
qu’ils aientune seule et même origine. Cesrésultats confirmentles
données obtenues au coursdes enquêtes épidémiologiques réalisées
sur le terrainpar lesservicesvétérinaires. D’autrepart, aucune
différencemajeure n’aété observéedans la séquencenucléotidique
du gène gag,entre lesisolatsprélevéssur leséquidés asymptomatiques
et l’isolat viralissuducas index.
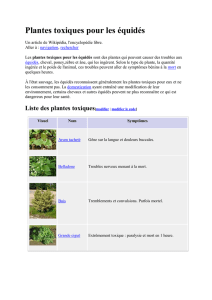
L’analysephylogénétiqueréalisée sur la séquencedugène gag (1 400
pairesdebases)permetdeclasser et de comparer lesisolatsvirauxissus
desfoyers varois2009aux isolatsdécritsdans la littérature (figure1).
Lesisolatsvarois formentunnouvelensembledifférent de ceuxformés
par lessouches nord-américaines et européennesrépertoriéesàce
jour.Les isolatsfrançais 2009 sontnotammentdifférentsdes souches
isoléesenIrlande et en Italie quiont étéresponsables de plusieurs
foyerscliniques en 2006.Cependant,les isolatsvarois semblent
prochesd’une souche roumaine(cloneRom-1)isolée et séquencée en
Italie en 2009.L’AIE est endémique en Roumanie avec 157foyers et
9301 équidés infectés répertoriésen2004. L’hypothèse quelasouche
virale isolée dans le départementduVar en 2009 aitune origineitalo-
roumaine est envisagée, même si aucune investigationréaliséesur
le terrain,àcejour, ne permet de relier lesfoyers du Varen2009
àdes échanges de chevauxavecces deux pays.
Lesconséquencesimportantes
de l’épisodeduVar
Compte tenu du nombredefoyers,d’équidés infectés et d’établis-
sements placés sous surveillance, cet épisode d’AIE aété le plus
importantenFrancedepuisledébut desannées 2000,assorti d’un
impactconséquentauplandelagestionsanitaire et administrative,
et auxplans économique et au plan judiciaire.
En effet, plus de 500équidés ontété soumis àdes mesures de
surveillance incluant desdépistagesetdes restrictions de mouvements
et environ1500dépistagespar la réalisationd’untest de Cogginsont
étéréalisés dans le cadredelapolicesanitaire.
Figure1.Analysephylogénétiquede29souches de virusdel’anémie infectieusedes équidés.
Analyseréalisée sur la séquencecomplètedugène
gag
(1 400nucléotides) des12isolats provenant de l’épisodevarois 2009.
SouchesVar 2009 -
FRANCE
Souchesorigine
USA
Souchesorigine
CANADA
Souchesorigine
EUROPE
(Irlande,Italie)
Souche origine
CHINE
12 Bulletin épidémiologique, santé animale et alimentationN
o39

Malgré leur dimensionnementadaptéaurisqueetleurévolution en
fonction de la situationépidémiologique, lesmesures de gestion, en
particulierles restrictions de mouvements,ont largementperturbé
l’activité desétablissements placés sous APMS.Dans le Var, près
de la moitié descentres équestresdudépartementaété bloquée
pendant cet épisode.Dans lesAlpes-Maritimes, plus de cent trotteurs
s’entraînant sur l’hippodrome de Cagnes-sur-Mer placésous APMS
ne pouvaientplusparticiperàdes compétitions extérieures.L’étroite
collaborationentre la filièreetles servicesvétérinairesapermis
d’adopterdes protocoles alternatifsdesurveillance de cestrotteurs
permettant auxentraineursdepoursuivreleursactivités, tout en
garantissant un niveau de protection sanitaire jugé équivalent.
Enfin, lesresponsables desétablissements dans lesquels lesfoyers de
Carcès(foyerindex et un foyer secondaire)ont étéidentifiés ontété
condamnésrespectivementàquatreettroismois de prison avec sursis
et miseàl’épreuve pendant36mois ainsi qu’à desamendesautitre
desnombreusesinfractions relevées dans l’établissement, allantdela
nonidentification deséquidés et nonisolementd’unanimalatteint
de maladiecontagieuse àlaprovocation ou propagationinvolontaire
d’uneépizootie(àlasuite du non-respectdes prescriptions de l’APDI)
Cetépisodeillustreles conséquences lourdesdans différents domaines
quepeuvent entraîner un foyerd’AIE et l’interconnexion sanitaire des
différentesfilièreséquines (sport/loisir et course dans le cas de cet
épisode).Dans ce cadre, il est primordial de souligner l’importance
du respectdelaréglementation relative àl’identification et la tenue
du registred’élevagequi sontles deux seulsoutilsdetraçabilité
actuellementdisponiblespourlafilière équine en France(hormis
certains outils élaborés par lesfilièrescourses). L’absencedefiabilité
du registred’élevagedans cetépisodead’autantpluscompliquéla
réalisationdes enquêtes épidémiologiques.
Enfin,bienque la prévalencedel’AIE en Francesoit sûrementtrès
faible, son importancenedoit pasêtresous estimée.Dans la mesure
où nombred’équidés infectés sontporteursasymptomatiques,
le dépistage volontaire par lespropriétairesd’équidés resteune
mesureefficace, notammentlorsd’introductiond’équidés dans un
établissement,oulorsdetransaction d’équidés, d’autant plus que
l’AIE est un vice rédhibitoire.Deplusetcompte tenu du tableau
cliniquesouvent fruste et peuévocateur,larecherched’AIE devrait
égalementêtreenvisagée plus systématiquementpar lesvétérinaires
praticiens dans le diagnostic différentiel d’un cheval présentant une
fièvre récurrented’origineinconnueaccompagnéed’anémie et de
thrombocytopénie.
Références bibliographiques
[1]Lignee, M. (1843) Mémoiresetobservations sur unemaladie de sang,
connus sous le nom d’anémie hydrohémie.Cachexieaqueuse de cheval.
Recueil de médecinevétérinaire 20,30.
[2]Hammond SA,LiF,McKeon BM Sr,Cook SJ,Issel CJ,Montelaro RC.
(2000)Immune responsesand viralreplicationinlong-term inapparent
carrierponiesinoculated with equine infectious anemiavirus.J.Virol.
2000 Jul;74(13):5968-81.
[3]LerouxC,CraigoJK, Issel CJ,Montelaro RC.(2001). Equine infectious
anemia virusgenomic evolutioninprogressor andnonprogressor
ponies. JVirol. 2001 May;75(10):4570-83.
[4]Issel CJ,Adams WV Jr,MeekL,Ochoa R. (1982).Transmissionofequine
infectious anemiavirus from horses without clinical signs of disease.J
Am VetMed Assoc.1982Feb 1;180(3):272-5.
[5]Hawkins JA,Adams WV,Cook L, Wilson BH,RothEE. (1973).Role
of horse fly(Tabanus fuscicostatusHine) andstablefly (Stomoxys
calcitrans L.)intransmissionofequineinfectious anemiatoponiesin
Louisiana.AmJVet Res. 1973 Dec;34(12):1583-6.
[6]Foil LD,MeekCL, Adams WV,Issel CJ.(1983). Mechanical transmission
of equine infectious anemiavirus by deer flies(Chrysopsflavidus) and
stableflies (Stomoxyscalcitrans).AmJVet Res. 1983 Jan;44(1):155-6.
[7]CogginsL,NorcrossNL. (1970).Immunodiffusionreactioninequine
infectious anemia. Cornell Vet. 1970 Apr;60(2):330-5
Brève. Émergenced’unvariantmonophasique du sérotype Typhimurium chez
Salmonella
Anne Brisabois
Anses, Laboratoire de sécurité desaliments de Maisons-Alfort
Depuis quelques années, lesdonnées de surveillanceetdecaractérisation desisolatsdeSalmonella montrentune augmentation importante
du sérotypeSI4,[5],12:i:-reconnu comme un variant monophasique du sérotype Typhimurium de formuleantigénique 4,[5],12 :i:1,2. Cette
augmentation marquéedunombre d’isolatsappartenant àcesérotypeest signaléeaussi bienauniveaunationalque dans d’autres pays européens
et auxÉtats-Unis[1].
En France, lesdonnées de surveillancedes souchescliniques collectées parleCentrenationalderéférencedes Salmonella montrentque la
fréquenced’isolementdecesérotypeest passée de la 11epositionen2005àlatroisième positionen2008, justeaprès lessérotypes Typhimurium
et Enteritidis,soit uneaugmentation de plus de 400%.Cependant,lenombre d’isolatsresteassez loin desdeuxprincipaux sérotypes.Demême,
lesoutils biostatistiques mis en placepar le Réseau Salmonella de l’Ansespourlasurveillancedes salmonelles d’originenon humaine et permettant
la détectiond’évènements inhabituels dans le nombred’isolatsfontétatd’unnombre anormalementélevé de souchesappartenant àcesérotype
depuis fin2007. Cettesituation semble stablepuisque le nombredesouches appartenant àcesérotyperecueillies durant 2009 se situe dans les
mêmesvaleursque la totalité de souchescollectéesannuellementaucours des4années précédentes dans lestroisgrandssecteurssurveillés:
Santéetproductionanimales, Hygiène desaliments et Environnement.
En Europe,les donnéesindiquent quelesérotype4,[5],12:i:-trèsrarementidentifiéavant 1990,sesitue actuellementdans les10premiers
sérotypes enregistrés dans différents pays et qu’ilexprime fréquemmentlephénotype de résistanceassocié àl’ampicilline,lastreptomycine,la
tétracycline et auxsulfamides[2].LeréseauEnterNetamontréque ce sérotypeétait identifiéen4ème positionparmi lescas de salmonelloses
humainesconfirmés en 2006.Les cas d’infectionobservésaveccesérotypesontliésàdes sourcesalimentairesvariées, maisles produits d’origine
porcine semblentplussouvent impliqués. En effet, le sérotype4,[5],12:i:-est égalementmentionné parmi les10sérotypes lesplusfréquemment
isolés àlafois de porcetdeviandeporcine d’après lesdonnées européennesde2006(http:/www.efsa.europa.eu/en/scdocs/scdoc/130r.htm).
Compte tenu de cettesituation et suiteàlasaisine de la DGAL surlesujet,ilaété décidéd’inclure dans la réglementation française concernant
le contrôle dessalmonelles en filièreaviaire,ladétection desvariantsdusérotype Typhimurium en plus descinqsérotypes ciblés (Notedeservice
DGAL/SDSSA/N2010-8026du27/01/2010).
Références bibliographiques
[1]Switt Al., SoyerY., WarnickLD.,Wiedmann M. Emergence, distributionand molecular andphenotypic characteristicsofSalmonella enteric
serotype4,5,12:i:-.Foodborne Pathog.Dis. 2009;6(4):407-15
[2]HopkinsK.L., KirchnerM., Guerra B.,GranierS.A.,Lucarelli C.,Porrero M.C.,JakubczakA., Threfall E.J.,MeviusD.J.Multiresistant Salmonella
entericserovar 4,[5],12:i:- in Europe:anew pandemic strain?Eurosurveillance, 15 (22)03 June 2010.
Bulletin épidémiologique, santé animale et alimentationN
o39 13
1
/
4
100%