Atomes de Rydberg et transitions vibroniques

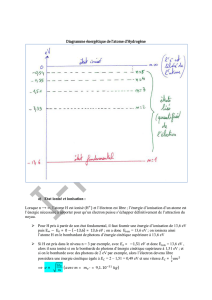
Lorsque l’électron de l’atome d’hydrogène est dans le niveau
d’énergie n, on démontre que sa distance moyenne au proton
vaut an= a0 n2où a0= 0,5 Å = 0,5 x 10–10 m.
Plus n est grand, plus l’électron est loin en moyenne du noyau
atomique. Ce sont des états de Rydberg.
Pour n infini, l’électron n’est plus lié au proton, son énergie est
nulle : l’atome est ionisé.
Atomes de Rydberg

Série de Balmer

Atome H
Rydberg (1889)
Noyau infiniment lourd
Noyau de masse MN
Atome de sodium Na
10 électrons de cœur sur orbitales 1s, 2s, 2p
Excitation 3s!3p n=3, l=1, s=1/2, j= 1/2, 3/2
Raie de résonance (doublet de structure fine)

Lithium Li
Sodium Na
Diagrammes de Grotrian des alcalins
(comparaison avec H)
2S2P2D2F

Sodium Na
Grotrian (suite)
3p
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
1
/
22
100%