Sujet n°2

1
Le pétrole : de sa formation à son exploitation
1) Formation du pétrole
a) Formation et maturation du kérogène
Le pétrole est une ressource énergétique fossile. En effet,
à la mort des organismes, plus de
5
99,9% du carbone qu'ils contiennent sont recyclés dans les chaînes alimentaires, mais les 0,1%
restant en moyenne quittent ce cycle de régénération et sont incorporés dans les sédiments. Ils
y subissent un ensemble de transformations physico-chimiques qui pourront conduire, sous
certaines conditions, à la formation de pétrole.
La matière organique des êtres vivants est pour l'essentiel constituée de protides, de lipides, de
10
glucides et de lignine, contenue dans les végétaux supérieurs. Cependant, la majeure partie des
protides et des glucides est recyclée après la mort des organismes, ce qui conduit à un
enrichissement de la matière organique en lipides et en lignine. Cette matière organique
s’enfouit dans les sédiments et, sous l’effet de l’augmentation de température, due au gradient
géothermique (augmentation de 30°C par kilomètre), et de pression (due à l’enfouissement), la
15
matière organique subit un ensemble de transformations selon trois étapes bien définies : la
diagénèse, la catagénèse et la métagénèse.
La diagénèse peut elle-même se subdiviser en deux étapes : la première est la diagénèse précoce
marquée par une forte activité bactérienne à faible profondeur et à basse température (50-60°C).
La deuxième étape de la diagenèse se caractérise par la rupture de liaisons faibles et par la
20
formation de méthane, de dioxyde de carbone et d'eau. Cette étape se traduit essentiellement
par la décroissance du rapport atomique O/C dans la matière organique. A la fin de cette phase,
les biopolymères ont été entièrement transformés en un géopolymère, le kérogène. Le kérogène
peut être vu comme une macromolécule constituée de chaînes alkyles plus ou moins ramifiées,
de cycles saturés et de cycles aromatiques, enchaînés de manière aléatoire. Cette
25
macromolécule est disséminée dans une roche, appelée roche mère.
La catagenèse constitue la phase de conversion du kérogène : l’enfouissement des sédiments et
l’augmentation de la température provoquent la rupture de liaisons covalentes au sein du
kérogène, ce qui conduit à la production de pétrole (huile et gaz). La température idéale de
maturation se situe entre 60°C et 120°C, ce qui correspond respectivement à 1 200 m et 3 000 m
30
de profondeur : il s’agit de la "fenêtre à huile". La pression varie de 30 à 100 voire 150 MPa
selon la profondeur et la densité des sédiments. Cette étape est également qualifiée de craquage
primaire.
La métagenèse est le stade ultime de transformation. Le kérogène acquiert une structure
hautement aromatique et ne produit plus que du méthane, de l'azote et du sulfure de
35
dihydrogène. La structure du solide résiduel est alors proche du graphite. Ces transformations
débutent lorsque la température atteint 160-180°C, vers 4500-5000 m de profondeur.

2
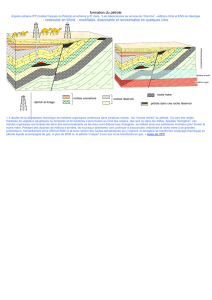
b) Migration vers les réservoirs
Une partie des composés générés lors de la catagenèse peut être expulsée de la roche mère sous
l’effet de la pression croissante des effluents au sein de la roche, vers une roche poreuse et
40
perméable contiguë : il s’agit de la migration primaire. La distance généralement parcourue
durant cette étape est faible : de quelques centimètres à quelques mètres.
Le pétrole expulsé entreprend ensuite une migration, appelée migration secondaire, durant
laquelle la distance parcourue par les hydrocarbures peut atteindre plusieurs centaines de
kilomètres. La migration s’achève si le pétrole rencontre une couche imperméable appelée
45
roche couverture. L’accumulation ou le piégeage de pétrole dans la roche réservoir forme alors
un gisement pétrolier. Dans le cas contraire, le pétrole peut atteindre la surface où il est
biodégradé et "oxydé" en bitume.
Lors de la migration secondaire, les vitesses de déplacement du pétrole sont extrêmement
faibles de sorte que le régime est laminaire et que la loi de Darcy (1) peut s’appliquer. La loi de
50
Darcy lie le débit volumique du fluide à la perméabilité intrinsèque du milieu poreux et à la
différence de pression motrice entre l’entrée et la sortie du milieu de migration.
(1)
Où :
- Q est le débit volumique en m
3
/s
55
- K, la perméabilité intrinsèque du milieu en m²
- A, la section du milieu étudié en m²
-
η
, viscosité dynamique en Pa.s
- L, la longueur du milieu étudié en m
- P*, la pression motrice du fluide en Pa : P* = P+
ρ
gz, avec
ρ
la masse volumique du
60
fluide en kg/m
3
.
La perméabilité intrinsèque est une caractéristique physique du milieu qui représente la facilité
qu’a un matériau à permettre le transfert d’un fluide au travers d’un réseau connecté. La loi de
Darcy a été empiriquement mise en évidence en 1856 et les perméabilités intrinsèques peuvent
être mesurées par l’expérience schématisée sur la figure 1 qui est un perméamètre à charge
65
constante. La couche de milieu poreux, d’épaisseur L, est placée dans la cuve inférieure. Le
niveau d’eau dans la cuve haute est maintenu constant par une alimentation et un bac de
débordement. L’écoulement du liquide dans le milieu poreux s’effectue du bas vers le haut. Le
fluide est évacué par le même principe de débordement qui maintient le niveau d’eau constant
au-dessus du milieu poreux. Les niveaux d’eau amont et aval étant constants, la différence de
70

3
pression
∆
P entre le bas et le haut du milieu poreux est aussi constante. L’écoulement dans le
milieu poreux est produit par la différence de pression motrice
∆
P* entre le bas et le haut :
Cette quantité est directement proportionnelle à la différence de hauteur H entre les niveaux
d’eau dans les deux tubes piézométriques, reliés respectivement à la base et au sommet du
75
milieu poreux :
∆
P*=
ρ
gH
Si H = 0, le fluide est en équilibre hydrostatique et le fluide ne coule pas à travers le milieu
poreux.
Figure 1 : Perméamètre à charge constante
80
La perméabilité intrinsèque de la plupart des roches a été mesurée ; elle s’échelonne de 10
-22
à
10
-12
m². Dans le cas du pétrole, il n’y a généralement pas qu’une seule phase fluide, mais un
mélange de gaz, d’huile et d’eau. Chaque phase ayant une viscosité dynamique différente, les
différentes phases progressent à une vitesse différente, entraînant ainsi une variation de
composition.
85
Milieu poreux
Débordement
débit Q
Section A
L
Evacuation du
trop-plein
Alimentation à
débit constant
z
z
1
z
2
H

4
La loi de Darcy, intégrée dans des modèles globaux de bassins sédimentaires, participe à la
compréhension de l’histoire du gisement, en particulier de son âge et de l’évolution de sa
composition.
2) Réservoirs pétroliers
90
a) Composition et diversité
Il existe une grande diversité dans la composition des pétroles, dont la nature s’échelonne des
condensats, pétroles presque transparents de très faibles densités, aux bruts extra-lourds,
opaques et plus denses que l’eau, mais il est possible néanmoins de dégager de grandes
tendances.
95
De façon générale, un pétrole est constitué de deux familles de composés : les hydrocarbures et
les composés dits polaires.
Les hydrocarbures se subdivisent en deux classes : les hydrocarbures dits saturés ou
aliphatiques comprenant les alcanes linéaires et ramifiés ainsi que les cycloalcanes, et les
hydrocarbures aromatiques incluant les composés purement aromatiques et les cycles soufrés,
100
et dans une moindre mesure les cycles azotés (figure 2).
Les composés dits polaires sont des macromolécules constituées de structures polycycliques
hétéroatomiques (N, S, O) dont les masses molaires peuvent atteindre 10 000 g/mol.
D’un point de vue économique, la classe de composés la plus intéressante est constituée des
hydrocarbures dits saturés, mais leur proportion est très variable selon l’origine du pétrole et
105
les transformations chimiques subies. Ils peuvent atteindre 80% en masse dans les condensats
et seulement 40% dans les huiles dégradées (figure 3).
b) Evolution thermique des pétroles dans les réservoirs géologiques : modélisation
cinétique
110
Le pétrole, une fois piégé dans sa roche-réservoir, subit un craquage thermique dit secondaire
du fait des températures qui règnent dans les réservoirs (jusqu’à 200°C) et des temps de
résidence de plusieurs millions d’années.
115

5
120
125
130
Figure 2 : Exemples d’hydrocarbures contenus dans les pétroles
135
140
145
Figure 3 : Diagramme ternaire montrant la composition massique globale de 636 huiles
HC AROMATIQUES
HC SATURES COMPOSES NSO
RESINES +ASPHALTENES
HUILES LOURDES DEGRADEES
80
60
40
20
20
40
60
80
20
406080
contours isofrequence
HUILES BRUTES
NORMALES
A
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%