SEP : Sclérose en plaques, affection dysimmunitaire

Article de synthèse
RMC-2012 2
1
SEP, la sclérose en plaques :
une affection dysimmunitaire
Docteur Brigitte CAPRON
Service de Neurologie
CHU de Charleroi - site de Vésale
L
a sclérose en plaques (SEP) est une affection dysimmunitaire, caractérisée par une
atteinte inflammatoire démyélinisante multifocale et chronique du système nerveux cen-
tral (SNC), entraînant une atteinte progressive du tissu cérébral, conduisant à un état
neurodégénératif.
La SEP se manifeste quand une lésion inflammatoire focale interrompt des voies nerveu-
ses cliniquement relevantes. La plupart des lésions de SEP sont cliniquement asympto-
matiques, donc, le moment d’apparition des symptômes et le type de symptôme exprimé
au début de la maladie relèvent en partie du hasard. La sévérité de la maladie est ainsi
extrêmement hétérogène et largement imprévisible. C’est la première cause d’handicap,
d’origine non traumatique, chez l’adulte jeune.
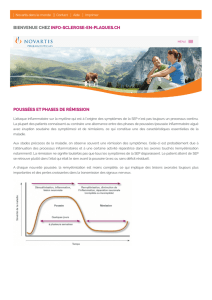
L’évolution clinique naturelle de cette maladie est variable. La SEP peut présenter 3 pat-
terns principaux : une forme évoluant par poussée(s)–rémission(s) (PR), une forme se-
condairement progressive (SP) et une forme primaire progressive (PP).
La majorité des malades (85%) débute avec une forme rémittente (poussée-rémission).
La poussée (déficit neurologique d’apparition aiguë) est associée à un processus in-
flammatoire focal dans le SNC. Ce phénomène semble sensible aux traitements immu-
nomodulateurs (et éventuellement immunosuppresseurs).
La survenue d’une poussée est en général imprévisible et le degré de récupération va-
riable.
Les traitements immunomodulateurs disponibles actuellement réduisent le taux d’exacer-
bation clinique (et radiologique) mais leur influence sur le pronostic à long terme de la
maladie n’est pas encore très clair.
En effet, avec le temps et avec l’âge, le taux de poussée diminue et beaucoup de ces
malades, présentant à l’origine une forme PR évoluent vers une forme secondairement
progressive. Dans celle-ci, le handicap neurologique (touchant plus particulièrement l’au-
tonomie à la marche) s’aggrave progressivement au fil des années, sans qu’il n’y ait plus
nécessairement d’exacerbation clinique aiguë (poussée).
Mots-clés
:
inflammation démyélinisante, système nerveux central, SNC

Article de synthèse
RMC-2012 2
2
Les malades avec une forme primaire progressive de SEP présentent une progression
d’un handicap depuis le début de leur maladie. Ce type d’évolution est, quant à elle, plu-
tôt associée à un processus de neurodégénérescence, sur lequel les traitements ac-
tuellement disponibles (immunomodulateurs et immunosuppresseurs) n’agissent pas.
Les mécanismes moléculaires sous-jacents à la progression de la maladie ne sont pas
bien connus.
La sévérité de la SEP varie considérablement d’un patient à l’autre, pouvant aller de for-
mes agressives, entraînant un handicap sévère en quelques années à peine, jusqu’aux
formes bénignes, avec un handicap mineur après une longue durée d’évolution.
Cette hétérogénéité de la sévérité de la SEP pourrait refléter la diversité des processus
biologiques impliqués dans les lésions de la gaine de myéline (neuro-inflammation), dans
les lésions axonales (neuro-dégénération), voire dans la réparation (remyélinisation,
croissance axonale et plasticité cérébrale).
Il semble toutefois que ces 3 formes évolutives (PR, SP et PP) représentent un phénoty-
pe continu d’une même maladie dans laquelle des facteurs familiaux (génétiques et/ou
environnementaux) influencent l’équilibre relatif entre la neurodégénérescence
(progression) et la neuroinflammation (poussées).
Figure 1
Les mécanismes responsables de l’apparition de cette maladie acquise sont difficiles à
établir car elle est probablement d’origine plurifactorielle, mais différents arguments lais-
sent supposer une intrication complexe de susceptibilité génétique individuelle et de fac-
teurs environnementaux.
Nous allons discuter ci-après des différents facteurs pouvant favoriser l’établissement
d’une SEP et ceux pouvant influencer l’évolution de la maladie.

Article de synthèse
RMC-2012 2
3
OBSERVATIONS ÉPIDÉMIOLOGIQUES GÉNÉRALES
La sclérose en plaque est une maladie de l’adulte jeune (pic d’incidence vers 30 ans),
deux fois plus fréquente chez la femme que chez l’homme, avec une répartition géogra-
phique inégale. La prévalence dans nos régions se situe aux alentours de 1/1000.
Figure 2
Il semble exister deux facteurs de risque principaux pour la sclérose en plaques, généti-
ques et environnementaux.
Figure 3

Article de synthèse
RMC-2012 2
4
SUSCEPTIBILITÉ GÉNÉTIQUE
Bien que la prévalence actuelle dans nos régions soit de 1/1000, le risque semble
majoré chez les personnes ayant un membre de leur famille atteint de la maladie. Si l’un
des parents est atteint de SEP le risque est de 4-5%, si les deux parents sont atteints, le
risque s’élève à 15%. Dans les familles de jumeaux monozygotes, si l’un des jumeaux
est atteint, le risque de l’autre s’élève à 30%.
Les études épidémiologiques sur les différents groupes ethniques d’une même ré-
gion montrent que les évolutions cliniques sont souvent différentes. Par exemple, les
Afro-américains ont un début plus tardif de la maladie, une forme plutôt optico-spinale
(névrite optique et atteinte médullaire) et un décours plus agressif que les Américains
caucasiens d’une même région des USA.
En France, il a été démontré que les patients d’origine nord-africaine ont une maladie
plus progressive, des poussées plus sévères et une rapide accumulation de handicap
que les patients d’origine européenne, et ce indépendamment du fait qu’ils soient immi-
grés ou nés en Europe. Ceci est un argument supplémentaire en faveur de l’hypothèse
d’une influence génétique sur l’expression clinique de la SEP et sa progression.
I
l n’existe sans doute pas un gène unique responsable du développement de la scléro-
se en plaques, mais plutôt une susceptibilité conférée par l’interaction de différents gènes
entre eux et/ou avec des facteurs environnementaux.
Depuis les années ’70, où une association entre le type d’allèle HLA exprimé et le risque
de SEP a été identifié, plusieurs études génétiques (GWAS ou Genome Wide Associa-
tion Studies) ont été entreprises et différents gènes ont été clairement associés avec une
susceptibilité pour la SEP.
Ces différentes variations génétiques pourraient non seulement influencer le risque de
développer la SEP, mais également jouer un rôle dans l’hétérogénéité de l’évolution clini-
que.
ARGUMENTS EN FAVEUR D’UNE INFLUENCE GÉNÉTIQUE

Article de synthèse
RMC-2012 2
5
P
our comprendre le rôle des différents gènes étudiés, il faut revenir à la physiopatho-
logie de la maladie…
La phase initiale de la lésion de démyélinisation est caractérisée par une rupture de la
barrière hémato-encéphalique et par une infiltration des lymphocytes et des monocytes
activés d’origine sanguine. Le primum novens de la maladie ne se situe donc pas au ni-
veau du système nerveux central mais bien au niveau systémique.
Dans le répertoire immunitaire du sujet normal, il existe un petit nombre de clones lym-
phocytaires T, inactifs ou dormants, dirigés contre des épitopes de diverses protéines de
la myéline, comme la protéine basique de la myéline (MBP), la myelin-associated glyco-
protein (MAG) …
D
es facteurs génétiques probables (déficience de l’immunorégulation) et environne-
mentaux conduisent à l’activation et à la prolifération de ces clones auto-réactifs, ainsi
qu’à leur passage dans le SNC au travers de la BHE.
Ainsi, dans le compartiment périphérique, les lymphoctes T CD4 + (LT CD4) myélino-
réactifs (faisant partie du répertoire immunologique normal), sont stimulés par la présen-
tation d’un exo-antigène (par exemple d’origine virale) dont la structure est proche d’un
auto-antigène de la myéline (mimétisme moléculaire).
C
ette présentation est réalisée par une cellule dendritique, ou cellule présentatrice
d’antigène, par le biais d’un complexe majeur d’histocompatibilité de type II (CMH II).
Il en résulte ensuite une activation et une prolifération de ces LT CD4 naïf (Th0).
Ceux-ci peuvent potentiellement se différencier en LTh1 (responsables de l’immunité cel-
lulaire), en LTh2 (responsable de l’immunité humorale), en LTh17 (qui sont des cellules
pro-inflammatoires) ou en LT reg (qui sont des cellules régulatrices).
PHYSIOPATHOLOGIE DE LA MALADIE
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
1
/
23
100%