TG4010, une approche personnalisée pour le traitement du cancer

> Quels sont ces « tests compagnons » ?
Nous développons ces tests « compagnons »
en partenariat avec des sociétés spécialistes
du diagnostic in vitro. Les deux biomarqueurs
sur lesquels nous travaillons ont des objectifs
complémentaires :
• l’un vise à mesurer si les cellules tumorales
d’un patient expriment la protéine MUC1. En
effet, notre vaccin a pour objectif d’induire
chez les patients une réponse immune
spécifiquement dirigée contre cette protéine.
Ce test immuno-histochimique, développé en
collaboration avec la société Ventana, Inc. a
été validé en 2011 ;
• l’autre vise à mesurer le taux de cellules dites
« Natural Killer » activées dans le sang des
patients. En effet, nous avons mis en évidence
dans l’étude clinique précédente réalisée dans
le cancer du poumon « non à petites cellules »
que le pourcentage de cellules Natural Killer
était potentiellement un biomarqueur de
l’efficacité et de la sécurité du traitement avec
le vaccin TG4010. Ce test fait l’objet d’un accord
de collaboration avec LabCorp, Inc. le deuxième
laboratoire de référence en biologie clinique
des États-Unis.
Nous travaillons main dans la main avec ces
sociétés, pour lesquelles le développement
de tests compagnons représente un axe
stratégique majeur. C’est un facteur de succès
pour ce type d’approche « théranostique »
associant diagnostic et thérapie. Là encore,
nous sommes au cœur d’une vaccination
thérapeutique ciblée en fonction des données
propres à chaque patient, un gage de meilleure
efficacité.
> Les résultats de phase II ont répondu
à vos attentes, quelles ont été les
avancées en 2011 ?
TG4010 est l’un des produits de notre
portefeuille les plus avancés dans son déve-
loppement et présente des perspectives très
prometteuses. Les résultats de la précédente
étude clinique de phase II ont d’ailleurs fait
l’objet d’une publication en 2011 dans la revue
scientifique de référence The Lancet Oncology.
Forts de ces résultats, l’année 2011 nous a
permis d’avancer et de finaliser le protocole
de l’étude clinique de phase IIb/III (étude TIME)
et de préparer cette étude à grande échelle.
Cela représente un travail considérable, tant
en interne, qu’en gestion de la sous-traitance
(une dizaine de sous-traitants et près de 200
contrats à signer) et au niveau des discussions
à mener avec des autorités réglementaires et
commissions variées (Autorités de santé,
Comités d’Ethique, Ministères de l’Environne-
ment…) en vue d’obtenir les autorisations de
réaliser l’étude dans une dizaine de pays !
Les discussions menées avec la FDA notamment,
se sont avérées très constructives et nous
avons ajusté notre protocole clinique suite à
« TG4010,
une approche personnalisée
pour le traitement du
cancer du poumon »
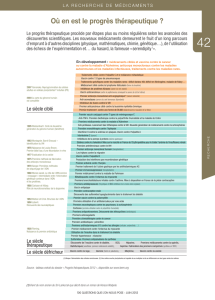
> En quoi le vaccin thérapeutique de Transgene est-il original ?
L’approche adoptée avec TG4010 se différencie
de celle de nos concurrents par le fait que nous
associons au développement de notre vaccin
thérapeutique deux biomarqueurs permettant
de sélectionner les patients pour lesquels le
traitement avec le vaccin sera potentiellement
bénéfique. Ces biomarqueurs sont mesurés par
des tests dits « compagnons » car associés
à l’approche thérapeutique avec le TG4010.
Après avoir démontré leur efficacité lors des
essais cliniques, ces tests compagnons seront
enregistrés concomitamment avec notre vaccin.
Nous sommes au cœur de la médecine
personnalisée, une médecine d’anticipation
qui apporte des réponses adaptées au profil
biologique de chaque patient.
Les tests compagnons ont en effet pour
objectif d’identifier les malades susceptibles de
répondre favorablement au traitement et/ou
d’écarter ceux qui pourraient développer des
effets secondaires indésirables. Ce nouveau type
d’approches ciblées améliore significativement
la prise en charge des patients et l’efficacité
des traitements. De plus, dans un contexte de
plus grande maîtrise des dépenses de santé, ces
enjeux sont importants au plan économique.
CANCERS
1
/
1
100%