Notes de cours section 1.4

Les substances pures
Notes sections 1.4

Substance pure
•Est composée d’un seul type de particule.
•Chaque substance pure possède son
propre type de particule qui diffère des
particules d’autres substances pures.
•Une substance pure a toujours les mêmes
propriétés.
–Elles sont utilisées pour l’identification.

Substance HOMOGÈNE!
Substance Pure!
Élement OU Composé
-oxygène -dioxyde de carbone

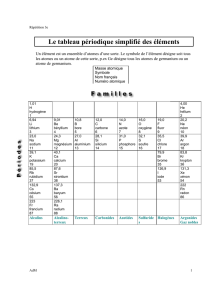
Types de substances pures
Les substances pures sont groupées selon leur
décomposition lors d’une transformation
CHIMIQUE.
1. ÉLÉMENT: substance pure qui NE se
décompose PAS en autres substances pures.
–p.c.q. il contient seulement un seul type d’atome.
–Oxygène (02) , Hélium (He)…
2. COMPOSÉ: substance pure formée de 2 ou
plusieurs éléments combinés chimiquement
–Forme une molécule distincte de rapport fixe
d’au moins 2 éléments.
–VA se DÉCOMPOSER dans ses éléments avec
l’application d’une transformation chimique.
–Eau (H20), dioxyde de carbone(C02)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%