La lettre mensuelle en PDF

Lettre d’information et d’analyse sur l’actualité bioéthique
°165 : M 2014
G. : Sur quel plan se situe votre opposi-
tion à la recherche sur l’embryon humain :
éthique ou scientique ?
Pr Alain Privat : Les deux. La mission du
médecin est de soigner, de son mieux, en
gardant à l’esprit un garde-fou absolu : le
respect de la vie humaine. La recherche qui
utilise l’embryon humain en promettant
des solutions thérapeutiques potentielles
a déjà, sur le plan éthique, franchi la ligne
jaune mais en plus, elle se fourvoie en
investissant temps et argent précieux dans
un axe qui conduit à des impasses cliniques
depuis deux décennies.
G. : Comprenons bien, comment aujourd’hui
est utilisé l’embryon humain?
Pr Alain Privat : Potentiellement, il existe
trois axes : les recherches fondamentales
sur le développement de l’embryon, l’uti-
lisation d’embryons pour la modélisation
des pathologies et le criblage de molé-
cules, utiles à l’industrie pharmaceutique
et les recherches, à visée directement thé-
rapeutique (la thérapie cellulaire qui est un
volet de la médecine régénérative). Disons
d’emblée que les premières, ce que l’on
appelle l’embryologie, sont conduites dans
leur majorité, pour ne pas dire leur tota-
lité aujourd’hui sur des modèles animaux
(de la mouche au primate, en passant par
le poisson, le poulet, le rat et la souris).
S’agissant de l’industrie pharmaceutique le
débat est aujourd’hui clos, même pour les
promoteurs de la recherche sur l’embryon
humain : pour cette utilisation, les cellules
iPS (induced pluripotent stem cells ou cel-
lules adultes inductibles), qui ont valu le
prix Nobel au Pr Yamanaka(1), présentent les
mêmes propriétés que les cellules souches
embryonnaires humaines (CSEh). Elles sont
faciles d’utilisation, développables dans
de très grandes quantités et sans barrière
éthique. Reste sans doute leur prix et c’est
un vrai problème: elles sont plus chères que
les cellules souches extraites d’embryons
humains, eux-mêmes… gratuits. Si le prag-
matisme scientique va aux iPS, le pragma-
tisme économique (à court terme) hésite :
la mise au point d’un médicament, quelle
qu’en soit la nature, nécessite aujourd’hui
une dizaine d’années de recherches, im-
pliquant notamment de longs et onéreux
essais sur des modèles animaux avant de
passer à l’étape des essais cliniques sur le
patient. L’utilisation en grand nombre de
cellules issues d’embryons humains per-
mettrait à l’industrie pharmaceutique de
tester à grande échelle de futurs médica-
ments, à un coût moins élevé que sur des
modèles animaux, ou sur des cellules iPS.
C’est l’un des objets des contrats passés
entre le groupe suisse Roche, et le labora-
toire ISTEM, créé dans ce but par l’AFM.
Pour ce qui est de la médecine régénérative,
le débat scientique reste ouvert alors que
de mon point de vue, la situation est encore
plus claire. Enn ce dernier point est évi-
demment la vitrine qui permet de tout faire
miroiter en termes de soin et de justier des
moyens employés (détruire des embryons)
pour aboutir à des ns attendues (soigner
des patients grâce aux cellules souches
extraites des embryons).
G. : Sur ce dernier axe et avant de rentrer
dans le détail, pouvez-vous rappeler ce
qu’est la médecine régénérative dont on
entend tant parler ?
Pr A.P. : Il s’agit de remplacer des cellules
décientes, comme celles qui produisent
l’insuline dans le pancréas, décientes
dans le diabète, ou de leur fournir des fac-
teurs de croissance ou de survie.
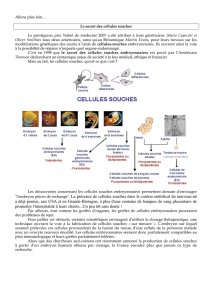
Ces recherches font appel à des thérapies
cellulaires et tissulaires (grees) à base
de cellules souches. Ces cellules indié-
renciées sont présentes en grand nombre
chez l’embryon, mais aussi, quoique
plus rarement, dans la plupart des tissus
adultes.
Les cellules souches ont deux caractéris-
tiques exclusives : Elles peuvent se multi-
plier quasiment à l’inni, et elles peuvent
également se diérencier dans tous les
types cellulaires de l’organisme adulte.
Promoteurs de la recherche sur l’embryon humain devenus prudents, adversaires de ces recherches surpris par les avancées des
équipes qui utilisent des embryons, publications contradictoires en série : l’état des lieux de la course scientique pour l’utilisation
thérapeutique de cellules souches est aujourd’hui dicile à établir pour un non initié. Qui, des équipes travaillant sur les cellules
souches adultes, les cellules iPS ou les cellules souches embryonnaires avance le plus ecacement vers les traitements ?
Gènéthique vous propose ce mois-ci l’analyse du Pr Alain Privat, neurobiologiste, membre correspondant de l’Académie de Médecine, ainsi
qu’une plongée dans deux cas particuliers qui ont animé l’actualité scientique des semaines passées : la thérapie cellulaire du cœur et le
clonage dit «thérapeutique ».
La recherche biomédicale et la médecine clinique
qui en est le résultat progressent sans faire appel
à l’embryon humain Par le Pr Alain Privat
(1) Le Pr Yamanaka montra que l’introduction de quatre gènes dans des cellules adultes de souris les transformait en cellules souches. Un an plus tard, il reproduisait cette expérience sur des cellules humaines.
Auditionné par la Commission des Aaires Sociales et de la Santé lors du débat qui a conduit en juillet 2013 à la libéralisation de la recherche
sur l’embryon en France, et, plus récemment, par la Commission européenne en tant qu’expert scientique dans le cadre de l’initiative One of
us/ Un de nous, le Pr Alain Privat est constant : la médecine n’a pas besoin des embryons humains pour soigner les patients. Explications.

(1) Karantalis V, 2014, Nasseri BA, 2014, Heldman AW, 2014, Hare JM, 2012 (Etude Poseidon)
(2) Fisher SA, Brunskill SJ, Doree C, Mathur A, Taggart DP, Martin-Rendon E., Stem cell therapy for chronic ischaemic heart disease and congestive heart failure,Cochrane Database Syst Rev. 2014 Apr 29;4:CD007888.
doi: 10.1002/14651858.CD007888.pub2.
(3) Nowbar AN, Mielewczik M, Karavassilis M, Dehbi HM, Shun-Shin MJ, Jones S, Howard JP, Cole GD, Francis DP; DAMASCENE writing group, Discrepancies in autologous bone marrow stem cell trials and enhan-
cement of ejection fraction (DAMASCENE): weighted regression and meta-analysis.,m BMJ. 2014 Apr 28;348:g2688. doi: 10.1136/bmj.g2688.
Thérapie cellulaire du cœur :
beaucoup de bruit…
Le cœur, comme le cerveau, attisent sans
surprise l’intérêt des équipes scientiques.
Récemment la perspective de soigner des
cœurs fatigués, victimes d’un infarctus via
des injections de cellules souches a trouvé
un nouvel écho. A l’origine deux publica-
tions quasi simultanées publiées dans la
revue scientique Nature.
La première souligne le fait que les publi-
cations scientiques sur la thérapie cellu-
laire du cœur dont le protocole se base sur
des cellules souches adultes ne présente-
raient pas de bénéce et que si bénéce il
y avait, il serait dû à un biais dans l’étude.
La seconde publication semble présenter a
priori un progrès dans l’utilisation des cel-
lules souches embryonnaires pour soigner
les fatigues du cœur : et plus particulière-
ment le risque lié au développement de tu-
meurs après injection de ces cellules, risque
le plus répandu dans l’utilisation de cellules
souches embryonnaires, semble pouvoir
être contenu. Peut-on en déduire que les
cellules souches adultes, jusqu’alors bien
plus avancées que celles embryonnaires
dans la thérapie du cœur seraient battues
en brèche ? En réalité, non.
L’utilisation des cellules souches adultes
(hématopoïétiques et mésenchymateuses,
donc non-embryonnaires) pour la régé-
nération myocardique après infarctus a
été pratiquée depuis déjà longtemps.
Une amélioration dans la fonction ventri-
culaire, faible, mais réelle, a toujours été
notée après injection de cellules souches
mésenchymateuses dérivées de la moelle
osseuse. Cet eet positif post infarctus -
augmentation de l’éjection ventriculaire,
diminution de la mortalité, et améliora-
tion globale un an après le traitement - est
bien démontré dans les études les plus
récentes(1) et (2).
Les mises en causes des eets des cel-
lules souches adultes sont discutables.
L’article de Nowbar AN et al.(3) qui jette le
doute sur les cellules souches adultes, ne
porte pas sur l’eet de ces cellules dans
le traitement de l’infarctus du myocarde,
chez l’homme, mais sur les inexactitudes
rencontrées dans certains rapports. Face à
des eets, certes modérés, mais réels, pré-
sentés dans le paragraphe précédant, les
conclusions de cet article sont à relativiser.
Deux cas particuliers ont récemment donné lieu à plusieurs publications qui semblent brouiller les cartes en matière d’utilisation de cellules
souches à des ns thérapeutiques : la thérapie cellulaire du cœur et le clonage dit « thérapeutique ». Gènéthique vous propose une plongée
dans ces publications scientiques pour démêler les avancées concrètes des eets d’annonce.
Thérapie cellulaire du cœur & clonage thérapeutique:
l’embryonnaire reviendrait-il dans la course
aux cellules souches ?
G. : Revenons-en à votre position sur la thé-
rapie cellulaire : quels éléments vous per-
mettent d’être aussi catégorique ?
Pr A. P. : D’une part, les médecins utilisent
depuis longtemps des cellules souches hu-
maines adultes, en particulier celles issues
de la moelle osseuse, qui contribuent à des
thérapies ecaces dans certaines maladies
hématologiques, mais aussi dans d’autres
pathologies. Les cellules souches issues
du cordon ombilical constituent également
une source précieuse. D’autre part, les
chercheurs disposent maintenant, depuis
8 ans d’un outil exceptionnel dont je parlais
à l’instant : les iPS. Ces cellules peuvent
être cultivées, multipliées, et utilisées pour
toutes sortes de recherches et de réelles
perspectives thérapeutiques. En particulier,
elles présentent l’avantage décisif sur les
cellules souches embryonnaires d’ouvrir la
porte à la médecine personnalisée. Préle-
vées sur des patients sourant de maladies
génétiques, elles peuvent être utilisées
pour analyser les détails de la pathologie
propre à ce patient et pour élaborer des
thérapies adaptées, pharmacologiques,
cellulaires ou moléculaires. Ceci est évidem-
ment impossible avec des cellules souches
embryonnaires provenant par dénition
d’un individu diérent. Parmi les objections
formulées à l’encontre des cellules IPS, les
plus fréquentes concernaient les risques
de tumorisation, et les risques inhérents à
l’utilisation de virus pour la transformation
de ces cellules.
Dans les derniers travaux publiés, les virus
ont été remplacés par des agents chimiques
sans danger. Par ailleurs, les risques de
tumorisation peuvent être éliminés par des
techniques de tri cellulaire.
En somme, les critiques à l’encontre des
iPS de première génération sont écartées
par la seconde génération de ces cellules.
D’ailleurs, si en France le débat est cade-
nassé, nombres d’équipes scientiques
ne s’y trompent pas: depuis 2006, près de
3000 articles scientiques concernant les
cellules iPS ont été publiés dans des revues
spécialisées. Au cours des trois derniers
mois, les pathologies étudiées vont de la
maladie de Parkinson (Doi et coll., Stem
Cell reports, 2014) au diabète (Holdich et
coll., Transl. Med., 2014), en passant par l‘X-
fragile (Doers et coll., Cell.Dev., 2014) et la
maladie de Pompe (Higuchi et coll., Genet.
Metab., 2014). Par ailleurs, des travaux de
recherche fondamentale concernant par
exemple l’évolution ont pu être conduits sur
des cellules iPS de primates comparées à
des cellules humaines (Wunderlich et coll.,
Stem Cell res., 2014). Enn, des essais
cliniques sont d’ores et déjà en cours au
Japon, concernant une maladie grave de la
vision, la Dégénérescence Maculaire liée à
l’Age (DMLA).
En revanche, depuis vingt ans, aucune ten-
tative thérapeutique utilisant des cellules
souches embryonnaires humaines n’a été
couronnée de succès. L’une des plus ré-
centes, conduite aux Etats-Unis par la socié-
té Geron, a été interrompue après quelques
mois, faute de résultats probants.

Lettre mensuelle gratuite, publiée par la Fondation Jérôme Lejeune - 37 rue des Volontaires 75725 Paris cedex 15
C : cont[email protected]g - T. : 01 44 49 73 39 - S : www.genethique.org - S : 31 rue Galande 75005 Paris
D : Jean-Marie Le Méné - Rédacteur en chef : Guenièvre Mouchet - I : PRD S.A.R.L. - N° ISSN 1627.498
(4) Chong JJ, Yang X, Don CW, Minami E, Liu YW, Weyers JJ, Mahoney WM, Van Biber B, Palpant NJ, Gantz JA, Fugate JA, Muskheli V, Gough GM, Vogel KW, Astley CA, Hotchkiss CE, Baldessari A, Pabon L, Reinecke
H, Gill EA, Nelson V, Kiem HP, Laflamme MA, Murry CE. Human embryonic-stem-cell-derived cardiomyocytes regenerate non-human primate hearts, Nature. 2014 Apr 30. doi: 10.1038/nature13233. [Epub ahead
of print]
(5) Irrégularités du rythme cardiaque
(6) Wang G, McCain ML, Yang L, He A, Pasqualini FS, Agarwal A, Yuan H, Jiang D, Zhang D, Zangi L, Geva J, Roberts AE, Ma Q, Ding J, Chen J, Wang DZ, Li K, Wang J, Wanders RJ, Kulik W, Vaz FM, Laflamme MA, Murry
CE, Chien KR, Kelley RI, Church GM, Parker KK, Pu WT., Modeling the mitochondrial cardiomyopathy of Barth syndrome with induced pluripotent stem cell and heart-on-chip technologies, Nature Medicine, 2014
May 11. doi: 10.1038/nm.3545
(7) 2013 par M.Tachibana, S.Mitalipov et ses collègues de l’Oregon National Primate Research Center (USA), de la réussite du clonage thérapeutique sur des cellules humaines, suivie ce mois-ci de deux annonces
identiques par deux équipes diérentes, l’une Coréenne (Young Gie Chung et Dong Ryul Lee de l’Université CHA de Séoul), l’autre américaine (Dieter Egli et collaborateurs, au New York Stem Cell Foundation
Research Institute).
L’article qui présente des avancées via
les cellules souches embryonnaires n’ap-
porte guère de nouveauté, dans un do-
maine où ce qui compte maintenant,
ce sont les résultats chez les patients.
Certes, il(4) présente la régénération par
les cardiomyocytes dérivés de cellules
souches embryonnaires du cœur de pri-
mates. Jusqu’alors cela n’avait été réalisé
que sur la souris : le passage au macaque
n’est pas anodin. Mais il met en garde vis-
à-vis des complications possibles d’une
telle opération, en particulier les aryth-
mies(5). Comme les cardiomyocytes dérivés
des cellules souches embryonnaires ne
peuvent être injectés aux patients, sous
peine de rejet immunologique, l’étude ne
fait pas prévoir de grands changements
dans ce domaine de la régénération myo-
cardique, chez les patients, par cellules
souches, à moins qu’un institut ne décide
de faire une épreuve clinique sous immu-
nosuppresseurs avec ces cardiomyocytes,
ce qui, d’un point de vue règlementaire,
est loin d’être réalisable.
La récente interview dans le Figaro Santé
du Pr Menasché (5 mai), ardent avocat
de l’utilisation des cellules souches
embryonnaires humaines en thérapie
cardiaque, se termine d’ailleurs par un
constat pour le moins prudent quant à
l’utilisation thérapeutique de ces cellules.
La vraie question demeure : pourquoi les
recherches dans le domaine sur des iPS
n’avancent-elle pas plus vite ? En eet,
la thérapie par cellules souches pluripo-
tentes chez l’homme est bien plus condi-
tionnée par la question du rejet immuno-
logique que par les éventuelles tumeurs
qui pourraient se développer. Par consé-
quent, logiquement le traitement par iPS
dérivées du malade lui-même devrait
prévaloir. Une publication parue mi mai
dans Nature Medecine(6) pourrait d’ail-
leurs ouvrir de nouvelles perspectives :
des équipes d’Harvard associent iPS,
thérapie génique et ingénierie cellulaire
pour restaurer du myocarde chez des
personnes atteintes d’une maladie géné-
tique qui conduit à des insusances car-
diaques. A suivre de près.
Clonage thérapeutique : le retour ?
Plusieurs annonces récentes viennent
de démontrer que le clonage thérapeu-
tique chez l’homme est possible. L’écho
rencontré dans la presse se comprend
en partie par le contraste avec le silence
qui entoure cette recherche depuis le
scandale du professeur coréen Hwang
en 2005(7). Est-ce à dire pour autant que
le clonage thérapeutique pourrait de
nouveau concurrencer les autres moyens
d’obtention des cellules souches pluri-
potentes (notamment les iPS) ? Pour rap-
pel, la technique du clonage consiste à
extraire le noyau cellulaire d’un ovocyte,
à le remplacer par le noyau d’une cel-
lule prélevée directement sur le patient
en attente de traitement. La division de
l’ovocyte est lancée pour aboutir à un
embryon au stade précoce duquel sont
extraites des cellules souches.
L’objectif est de produire un tissu géné-
tiquement identique au patient ce qui
permettrait d’éviter les rejets observés
avec des cellules souches embryonnaires
«classiques».
Une entreprise qui demeure insoutenable
sur le plan éthique, coûteuse, et limitée sur
le plan de son application. Ces diérents tra-
vaux récents montrent certes que le clonage
thérapeutique est possible chez l’homme.
Cependant les obstacles sont nombreux.
D’abord cette technique consiste à créer des
embryons, donc des êtres humains pour la
recherche, ce qui éthiquement est indéfen-
dable.
Ensuite les conditions sont très précises, et
avec une ecacité limitée. Cette réussite a
un intérêt théorique, mais n’a guère d’appli-
cabilité pratique, en particulier pour une mé-
decine régénérative. La disponibilité réduite
d’ovocytes humains, les questions éthiques
soulevées par la rémunération des femmes
qui donnent leurs ovocytes d’une part et
par l’enjeu de société abyssal que repré-
sente le clonage humain, la basse ecacité
de la procédure de transfert nucléaire et le
long temps nécessaire pour obtenir le dou-
blage de la population de cellules souches
embryonnaires humaines, font qu’une telle
technique peinera à devenir une procédure
de routine dans le domaine clinique.
On sait que les publications en la matière
sont systématiquement accompagnées
d’une grande couverture médiatique.
Cependant cela est loin de prouver que ce
clonage dit «thérapeutique» soit devenu
une alternative crédible à l’usage des cel-
lules iPS, plus discrètes, mais déjà répan-
dues et très utiles dans les laboratoires.
1
/
3
100%