Quand les questions bioéthiques de début et de fin de vie

Quand les questions bioéthiques
de début et de fin de vie
interrogent la vie religieuse
Rueil-Malmaison, 28 janvier 2012

2
Introduction
- Définition de la bioéthique :
La bioéthique s’intéresse à la mise en œuvre des soins du malade ainsi qu’aux
recherches et aux techniques biomédicales impliquant l’utilisation des éléments du
corps humain.
Elle cherche à répondre le mieux possible aux questions soulevées par le progrès
scientifique et technique, au regard des valeurs de notre société pour le respect de la
dignité humaine du début à la fin de l’existence.
A partir des questionnements bioéthiques devraient naître des lois justes, au sens où
ces lois préservent la dignité de la personne humaine en toute situation, et notamment
dans celles où la personne apparaît le plus vulnérable. Mais les lois et les institutions
tiennent-elles promesse ?
- Problématique :
Il s’agit donc de nous exercer à un regard critique à partir de notre place en société en
tant que religieux et religieuses. La vie religieuse, comme mode de vie croyant, a-t-
elle quelque chose à dire sur les grandes questions de bioéthique ? Quelle société se
dessine, par rapport à « la justice du Royaume » ? Que devient la personne humaine
aujourd'hui, créée « à l’image et à la ressemblance de Dieu » ? D’un autre côté, ces
questionnements ont-ils quelque chose à nous dire sur notre manière d’être au monde
aujourd’hui en tant que consacré(e)s ?
- Présentation :
Nous aborderons ces interrogations à travers cinq thèmes de bioéthique choisis : 1/ le
diagnostic prénatal, 2/ la recherche sur les cellules souches, 3/ l’assistance médicale à
la procréation, 4/ l’autonomie décisionnelle du patient, et 5/ la demande de mort en fin
de vie.

3
1. Diagnostic Pré Natal
- Qu’est-ce que le DPN ?
La loi relative à la bioéthique du 6 août 2004 dit que « le diagnostic prénatal s’entend des
pratiques médicales ayant pour but de détecter in utero chez l’embryon ou le fœtus une
affection d’une particulière gravité.» Art. 23
Mais qu’appelle-t-on une « affection d’une particulière gravité » ? La loi ne précise pas.
- Comment se fait le DPN ?
On retient trois types de techniques pour identifier une anomalie chez le fœtus
- Des échographies chez la femme enceinte. Cet examen d’imagerie permet d’explorer
la morphologie du fœtus.
- Des prélèvements de liquide amniotique (amniocentèse), de cellules placentaires
(biopsie de trophoblaste), ou de sang fœtal (ponction de sang fœtal) pour faire des
études biologiques (recherches génétiques en particulier).
- Des prélèvements de sang maternel permettront probablement dans le futur
d’identifier des anomalies fœtales avec une moindre agressivité.
Le DPN permet de détecter en pratique, surtout par l’échographie et l’amniocentèse, de
nombreuses pathologies :
- atrophie d’un membre
- grave lésion neurocérébrale : anencéphalie, spina bifida
- handicap mental sévère : trisomie 21
- maladie gravement invalidante : myopathie, mucoviscidose
Le bien de l’enfant à naître justifie amplement l’usage de l’échographie qui peut permettre des
traitements voire une intervention chirurgicale précoce. De même, une prise de sang maternel
peut déboucher sur des examens plus précis de l’enfant. Ainsi, la toxoplasmose détectée dans
le sang maternel peut entraîner une cécité chez l’enfant à naître, voire sa mort. Il est important
de détecter cette infection le plus tôt possible et de la traiter par voie médicamenteuse.
Le DPN a donc toute sa légitimité.
- Cependant, il convient de distinguer les examens de diagnostic proprement dit des
examens de dépistage.
Diagnostiquer, c’est affirmer la présence d’une anomalie. Dépister, c’est repérer un risque
d’anomalie dans une population donnée.
Le dépistage de la trisomie 21 est un exemple paradigmatique du glissement en France du
DPN au dépistage
Le DPN de la trisomie 21 avait essentiellement pour but, à ses débuts, de rassurer des couples
qui avaient déjà donné naissance à un enfant trisomique. Puis un glissement s’est opéré : on
est passé d’un diagnostic de T21 dans les populations à risque à un dépistage systématique
chez toutes les femmes enceintes.
Aujourd'hui, un test est obligatoirement proposé par le médecin à toute femme enceinte pour
dépister, non une trisomie 21, mais une probabilité augmentée que l’enfant soit porteur d’une
trisomie 21. L’analyse de sang, qui s’appelle le dosage des marqueurs sériques, est couplée à
une échographie sur laquelle on va rechercher une clarté nucale. Le résultat est donné en
risque : si, au vu des ces examens, le risque pour le fœtus d’être porteur de l’anomalie est

4
supérieur ou égal à 1 sur 250, on propose une amniocentèse pour établir un caryotype.
L’amniocentèse consiste à prélever du liquide amniotique grâce à une aiguille introduite à
travers l’abdomen de la mère. Ce n’est pas un geste anodin puisqu’il peut provoquer une
fausse couche dans un cas sur 100.
Les limites de ces tests de dépistage sont réelles:
- Ce n’est pas un diagnostic mais un calcul statistique de risque. Il entraîne la pratique
d’une amniocentèse avec risque de fausse couche, alors que dans 98% des cas, le
caryotype du fœtus est normal.
- Ce calcul statistique est anxiogène pour la femme enceinte quand le risque est élevé
(alors que l’enfant sera normal).
- Il n’y a pas de geste thérapeutique possible : la trisomie 21 ne peut se guérir.
Ce genre de test débouche donc sur deux attitudes :
- Soit se préparer à accueillir un enfant trisomique.
- Soit décider une IMG, interruption de grossesse pratiquée pour un motif médical.
L’avortement est le choix de 90% des couples concernés par un diagnostic prénatal de
trisomie 21.
- En conclusion : attention à la dérive eugéniste
Derrière DPN, on peut entendre : tri, sélection… Il faut donc être attentif à la capacité de la
société à accepter des enfants handicapés. Moins la société est accueillante, plus l’exigence
d’une normalité sera revendiquée.
Certains pensent que l’on peut appliquer le principe de précaution à la naissance d’un enfant
(ne prendre aucun risque d’écart par rapport à ce qui est considéré comme la norme ou
l’idéal : l’enfant « zéro défaut ») Mais que penser d’une société qui ne supporte plus le doute
ou le divers ?
ALTERNATIVES : encourager la recherche sur les maladies concernées plutôt que
l’éradication des malades.
Annexe 1
La France au risque de l’eugénisme
Le Monde, 03/02/07 Didier Sicard, président du Comité consultatif national d’éthique.
Propos recueillis par Michel Alberganti et Jean-Yves Nau.
« Il me paraît hautement préoccupant que l’on passe d’un dépistage généralisé à une forme
d’éradication sociale.
Le cas des trisomies 21 et 18 en sont un exemple paradigmatique. Tout s’est passé comme si,
à un moment donné, la science avait cédé à la société le droit d’établir que la venue au monde
de certains enfants était devenue collectivement non souhaitée, non souhaitable. Et les parents
qui désireraient la naissance de ces enfants doivent, outre la souffrance associée à ce
handicap, s’exposer au regard de la communauté et à une forme de cruauté sociale née du fait
qu’ils n’ont pas accepté la proposition faite par la science et entérinée par la loi.
En France la généralisation du dépistage est, certes, fondée sur la notion de proposition, mais
dans la pratique il est, de fait, devenu quasi obligatoire. Le dépistage de la trisomie concerne
désormais en France, gratuitement, la quasi-totalité des grossesses. Osons le dire : la France
construit pas à pas une politique de santé qui flirte de plus en plus avec l’eugénisme. »

5
2. Recherche sur cellules souches
Grâce aux progrès de la médecine, dans un pays développé comme la France, la longévité
augmente, et, avec elle, des maladies dites dégénératives liées au vieillissement cellulaire. Un
exemple typique est la maladie d’Alzheimer, entraînant des handicaps importants, tant
intellectuels que physiques. Les recherches sur les cellules souches et embryonnaires tentent
de traiter ces maladies en remplaçant les cellules abîmées – c’est ce qu’on peut appeler une
thérapie cellulaire ou « médecine régénératrice » (Pierre d’Ornellas, « Bioéthique – Propos
pour un dialogue », Lethielleux, Paris, 2009).
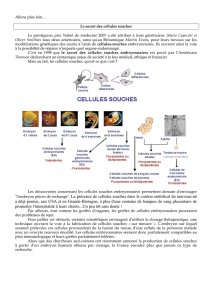
- Que sont les cellules souches ?
Les cellules souches sont des cellules très jeunes dont on distingue trois types :
- Les cellules souches adultes, qui sont différenciées en type d’organe (sang, peau par
exemple).
- Les cellules souches pluripotentes, qui sont des cellules souches adultes mais qui ont
subi une modification pour les rendre indifférenciées et donner donc différents types
de tissus.
- Les cellules souches embryonnaires, provenant des embryons et qui sont
indifférenciées et donc également aptes à produire différents tissus. Ces embryons
pourraient être produits par génie génétique. C’est ce qu’on appelle le « clonage », car
de fait, les embryons produits et le sujet à traiter ont les mêmes gènes. L’intérêt des
cellules indifférenciées est qu’elles pourraient remplacer les cellules de plusieurs
organes, voire n’importe quel organe.
Alors que la thérapie cellulaire à partir des cellules souches adultes a déjà quelques
applications (maladies sanguines, greffe de peau), il n’y a pas pour le moment de possibilités
réelles de traitement avec des cellules souches pluripotentes ou embryonnaires car le risque de
provoquer des cancers est grand.
- Problématique du statut de l’embryon :
Il y a une première problématique concernant la recherche sur les cellules embryonnaires qui
affecte l’intégrité de l’embryon: les prélèvements de cellules pour recherche entraînent sa
destruction. Si on considère, à l’instar de l’Eglise, que l’embryon dès sa conception est un être
humain, une telle attitude non seulement serait :
- une transgression de l’interdit de meurtre,
- mais serait également une atteinte de la dignité humaine, l’embryon n’étant plus
considéré comme une personne mais comme un objet.
- Problématique du rapport au traitement hautement technique :
La question de l’embryon ne se pose pas lorsqu’il s’agit de cellules souches adultes, et on peut
se réjouir des recherches à partir de telles cellules qui peuvent apporter un progrès dans le
traitement des maladies. Mais on peut s’interroger sur le rapport que l’on peut avoir par
rapport à ces éventuels traitements de pointe :
- tous ne pourront y avoir accès, à cause du coût ;
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%