Le cycle de l`acide citrique

Le cycle de l’acide citrique
• Synonymes
– cycle d!’acide tricarboxylique
– cycle de TCA
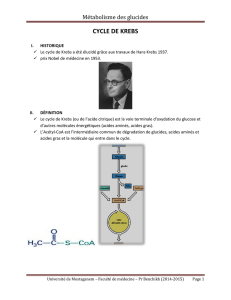
– cycle de Krebs
• Fonction: conversion de pyruvate en
CO2 et H2O via des intermédiaires du
cycle
• Plaque tournante du métabolisme
aérobie
– cycle amphibolique
• Cataboliques: Oxidations des glucides,
des graisses, des acides aminés
• Anaboliques: Matériaux de départ pour
de nombreuses voies biosynthétiques
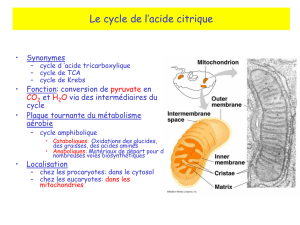
• Localisation
– chez les procaryotes: dans le cytosol
– chez les eucaryotes: dans les
mitochondries



Le cycle du citrate se passe dans les mitochondries

Entrée du pyruvate dans la mitochondrie
• Membrane externe: porine
(10,000)
• Membrane interne: pyruvate
translocase symport pyruvate
+ H+
• Entrée du pyruvate dans le
cycle du citrate
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
1
/
30
100%