epreuve theorique : corrige

22èmes Olympiades de la Chimie. Académie de Lille. Sujet théorique. Corrigé
1
OLYMPIADES DE LA CHIMIE 2006
Concours régional de l’Académie de Lille
EPREUVE THEORIQUE : CORRIGE
Durée : 2 h Calculatrice autorisée
mots-clés : chlorure de vinyle ; PVC ; plastifiant ; phtalate ; alumine ; aluminium ;
procédé Bayer ; électrolyse de l’alumine ; anodisation de l’aluminium
LE P.V.C. ET L’ALUMINIUM COMME MATERIAUX DE
CONSTRUCTION : FABRICATION ET PROPRIÉTÉS
De nombreux matériaux sont utilisés dans l’habitat. Parmi ceux-ci nous nous intéresserons
plus particulièrement au polychlorure de vinyle (P.V.C.) et à l’aluminium. Le P.V.C.
représente 39 % des matières plastiques utilisées dans l’habitat. Le P.V.C et l’aluminium
servent notamment pour réaliser des portes, des plinthes, des fenêtres et des volets. 46 % des
fenêtres posées sont en PVC et 33 % en aluminium.
1. Le P.V.C.
Le marché intérieur de la menuiserie en matières plastiques est évalué à près de
350 000 tonnes par an.
Le PVC, comme les autres matières plastiques, est un produit dérivé du pétrole. Dans cette
partie nous allons étudier les différentes étapes de fabrication du P.V.C.
1.1. Synthèse du P.V.C.
L’éthylène (ou éthène) est le premier produit de base de la chimie organique tant par son
volume de production que par son nombre de dérivés : 30 % des produits de la pétroléochimie
en dérivent. Il intervient en particulier dans la synthèse de nombreuses matières plastiques
telles que le polyéthylène (PE), le polystyrène (PS), le polychlorure de vinyle (PVC) etc.
On se propose dans un premier temps de synthétiser l’éthylène, puis le chlorure de vinyle et
enfin de polymériser le chlorure de vinyle pour obtenir le P.V.C.

22èmes Olympiades de la Chimie. Académie de Lille. Sujet théorique. Corrigé
2
1.1.1. Synthèse de l’éthylène par différentes méthodes
Près de 80 millions de tonnes d’éthylène sont produites industriellement chaque année dans le
monde.
La déshydratation de l’éthanol d’origine agricole chauffé en présence d’un catalyseur acide
peut constituer une façon de fabriquer de l’éthylène au laboratoire.
1. Ecrire l’équation de cette réaction :
CH3-CH2OH = CH2=CH2 + H2O
2. Qu’est-ce qu’un catalyseur ?
Un catalyseur est une espèce chimique qui accélère une réaction chimique
Dans l’industrie on peut produire l’éthylène par déshydrogénation de l’éthane.
3. Ecrire l’équation de cette réaction :
CH3-CH3 = CH2=CH2 + H2
En réalité c’est un mélange d’hydrocarbures saturés qui est soumis à déshydrogénation. On
récupère l’éthylène à partir du mélange réactionnel.
1.1.2. Synthèse du chlorure de vinyle
Chaque année, on fabrique dans le monde 20 millions de tonnes de chlorure de vinyle.
Dans une première étape on effectue la chloration de l’éthylène en phase liquide à 60°C en
présence d’un catalyseur
4. Ecrire l’équation de la réaction (R1) entre l’éthylène et le dichlore sachant que l’on
obtient un produit dichloré symétrique :
CH2=CH2 + Cl2 = CH2Cl-CH2Cl
5. Quel est le nom de la molécule (A) ainsi obtenue ?
1,2-dichloroéthane
La seconde étape consiste à éliminer le chlorure d’hydrogène du composé (A) à 500°C sous
une pression de 12 bars, par un mécanisme radicalaire, pour obtenir le chlorure de vinyle ou
chloroéthène.
6. Ecrire l’équation de cette réaction (R2) :
CH2Cl-CH2Cl = CH2=CHCl + HCl
La molécule (A) peut également être obtenue industriellement par une réaction, appelée
oxychloration, effectuée à 230°C sous une pression de 5 bars et dont l’équation est :
CH2=CH2 + 2 HCl + ½ O2 = CH2Cl-CH2Cl + H2O (R3)
Cette réaction utilise donc le chlorure d’hydrogène fabriqué précédemment.

22èmes Olympiades de la Chimie. Académie de Lille. Sujet théorique. Corrigé
3
La production industrielle du chlorure de vinyle utilise ces trois dernières réactions
7. Ecrire le bilan global de la réaction (R) de synthèse du chlorure de vinyle :
(R) = (R1) + 2(R2) + (R3)
2 CH2=CH2 + Cl2 + ½ O2 = 2 CH2=CHCl + H2O
8. Quel est l’avantage pour l’industrie de combiner ces trois réactions dans une
production automatisée ?
Pas de chlorure d’hydrogène dans les produits
1.1.3. Synthèse du P.V.C
9. Représenter la structure du polychlorure de vinyle (PVC) :
CH
2
CH
Cl n
Les spécialistes ont montré qu’il était facile d’obtenir des macromolécules de PVC
constituées par l’association d’environ 10 000 molécules de chlorure de vinyle.
10. Déterminer la masse molaire moyenne de ce PVC :
M = [2*M(C)+3*M(H)+M(Cl)]*10 000 = 625 000 g/mol
1.2. Propriétés du P.V.C.
Le PVC obtenu est très dur et cassant, ce qui constitue un handicap pour son utilisation à
grande échelle.
L’amélioration de ses propriétés d’usage passe par l’ajout d’additifs (en moyenne 10% en
masse) qui rendent possibles de nombreuses applications.
1.2.1. Ajout de plastifiants
Pour obtenir des feuilles de plastique souples il est nécessaire d’ajouter au PVC des
plastifiants.
Les phtalates sont des plastifiants très répandus. Ce sont des diesters qu’on peut obtenir par
réaction entre l’anhydride phtalique et un alcool en excès.
11. Compléter l’équation ci-dessous de formation d’un phtalate en précisant sa structure :
O
O
O
C
8
H
17
OH
+2
O
O
O
O
C
8
H
17
C
8
H
17
+H
2
O
structure phtalate et eau

22èmes Olympiades de la Chimie. Académie de Lille. Sujet théorique. Corrigé
4
12. Calculer la masse molaire M’ du phtalate formé :
M’= 390 g/mol
13. Comparer la taille des molécules de plastifiant à celle des molécules de PVC.
M’<<M : les molécules de plastifiant sont très petites devant les molécules de PVC.
Les tuyaux souples transparents utilisés au laboratoire peuvent être en PVC. Après plusieurs
mois d’utilisation on constate que le PVC perd sa souplesse et qu’il se casse par endroits si
l’on veut changer sa forme.
14. Proposez une explication à ce phénomène de vieillissement :
Le PVC devient de nouveau cassant car le plastifiant est expulsé aux endroits soumis à des
contraintes mécaniques.
1.2.2. Ajout de charges
Pour obtenir des matériaux tels que les portes ou les fenêtres il faut diminuer l’effet plastique
des matériaux. On modifie les propriétés mécaniques en ajoutant des « charges » minérales
telles que le carbonate de calcium, le dioxyde de titane…Les matériaux contenant ces charges
sont blancs.
Pour obtenir une autre couleur il suffit d’ajouter au mélange en fusion des pigments colorés :
le matériau est ainsi coloré dans la masse.
Le carbonate de calcium est bon marché : son ajout influe sur le prix des matériaux finis.
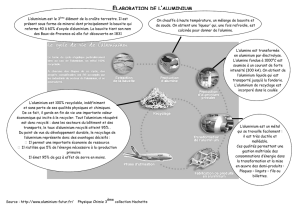
2. Elaboration de l’aluminium
L’aluminium est l’élément métallique le plus répandu sur notre planète. Il représente 8 % de
la masse totale de l’écorce terrestre et se trouve sous forme d’alumine de formule chimique
Al2O3 ou d’autres formes oxydées de l’aluminium. L’élément aluminium est présent dans des
silicoaluminates (argiles, schistes…) contenant 18 à 38 % d’alumine, mais il est plus
économique de récupérer l’aluminium à partir des bauxites.
La bauxite est constituée essentiellement de :
- 40 à 60 % en masse d’hydrargillite (ou hydroxyde d’aluminium), de formule Al(OH)3,
ou de böhmite, de formule AlO(OH), composés insolubles dans l’eau
- 10 à 20 % d’oxyde de fer : la gœthite de formule FeO(OH)
- 5 % de silice
2.1. Obtention de l’alumine
Les composés de l’aluminium contenus dans la bauxite étant insolubles dans l’eau, il est
nécessaire de les transformer en espèces solubles pour pouvoir les séparer de la gœthite et de
la silice qui restent solides et peuvent ainsi être éliminés par filtration.
Dans un deuxième temps les dérivés de l’aluminium sont à nouveau transformés en solide et
filtrés.
Ceci constitue le principe du procédé Bayer élaboré en 1887.

22èmes Olympiades de la Chimie. Académie de Lille. Sujet théorique. Corrigé
5
Dans ses recherches Bayer a observé qu’il pouvait solubiliser les dérivés de l’aluminium
contenus dans la bauxite :
• Soit par une attaque à l’acide conduisant au cation aluminium Al3+
15. Ecrire l’équation de la réaction donnant Al3+ à partir de Al(OH)3 :
Al(OH)3 + 3 H+ = Al3+ + 3 H2O
16. Quel est le rôle de Al(OH)3 dans cette réaction ? Justifier.
Al(OH)3 joue le rôle d’une base de Brønsted
car il capte des ions H+
• Soit par une attaque basique fournissant l’ion aluminate AlO2-
17. Ecrire l’équation de la réaction donnant AlO2- à partir de Al(OH)3 :
Al(OH)3 = AlO2- + H2O + H+
18. Quel est le rôle de Al(OH)3 dans cette réaction ? Justifier.
Al(OH)3 joue le rôle d’un acide de Brønsted
car il cède un ion H+
19. On dit que l’hydroxyde d’aluminium est amphotère. Expliquer :
Une espèce amphotère est à la fois un acide et une base. On vient de voir que c’est le cas de
Al(OH)3.
20. Porter sur une échelle de pH les domaines de prédominance de ces différentes espèces
de l’aluminium
Dans le procédé Bayer, la bauxite est attaquée par une solution concentrée d’hydroxyde de
sodium à 220°C dans des autoclaves sous une pression de 20 bars (étape 1). La solution ainsi
obtenue est alors filtrée pour la débarrasser des « boues rouges » (étape 2) puis on fait
précipiter l’hydroxyde d’aluminium en diluant et en refroidissant la solution filtrée (étape 3).
Enfin l’alumine est obtenue par calcination de l’hydroxyde d’aluminium, c'est-à-dire par
chauffage à plus de 1200°C.
21. Pourquoi l’attaque basique de la bauxite est-elle réalisée à haute température ?
Pour que la vitesse de réaction soit plus grande (cinétique)
22. Ecrire l’équation chimique de la réaction de calcination de l’hydroxyde d’aluminium.
2 Al(OH)3 = Al2O3 + 3 H2O
pH Al(OH)3 Al3+ AlO2-
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%