Introduction au métabolisme

Introduction au métabolisme
Toute cellule a des besoins en énergie :
- Travail mécanique
- Contractions musculaires
- Mouvements cellulaires
- Transport actif de molécules, d’ions
- Synthèse de macromolécules à partir de précurseurs simples
- Production de chaleur
- Production d’électricité
- … Figures tirées de
Copyright © 2004 by W. H. Freeman & Company
Lehninger Principles of Biochemistry
Fourth Edition
Chap I.
I. Introduction

Origine de l’énergie
- Ni crée, ni détruite mais TRANSFÉRÉE
- Environnement
- Radiations lumineuses (soleil) / organisme phototrophes
(plantes vertes, bactéries photosynthétiques)
- Substances organiques / organismes chimiotrophes
(herbivores, carnivores)
Energie lumineuse
+ CO2 + NH3 + H2O
Energie chimique
glucides, lipides,
Protéines, …
Energie chimique
(organique)
Energie chimique
(organique)

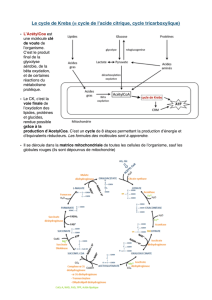
Métabolisme (de tous les êtres vivants) =
Transformation de l’énergie chimique
en d’autres formes d’énergies
Nutriments fournissant
de l’énergie
Glucides, graisses,
protéines
Catabolisme
Produits terminaux pauvres
en énergie
CO2, H2O, NH3
Anabolisme
ADP + Pi
NAD+
FAD
ATP
NADH + H+
FADH2
Macromolécules
cellulaires
Protéines, polysaccharides,
lipides, acides nucléiques
Energie
chimique
Précurseurs
Acides aminés, sucres,
acides gras, bases azotées

Métabolisme
Ensemble hautement intégré de réactions chimiques
Structure cohérente contenant de nombreux éléments
communs
Nombre de réactions très grand
Ex : Escherichia coli : plus de 1000 réactions
Nombre de types de réactions limité
Mécanismes très simples
Molécules clés avec rôles centraux
Régulations par mécanismes communs

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%