Mini-revue Apport des modèles animaux d`inflammation intestinale

Mini-revue
Apport des modèles animaux
d’inflammation intestinale
dans les maladies
inflammatoires chroniques
de l’intestin
Stéphane Nancey
1,2
, Fériel Hacini
2
, Pierre-Yves Durand
2
,
Nadège Milhau
2
, Dominique Kaiserlian
2
, Bernard Flourié
1
1
Service d’Hépato-Gastroentérologie, Centre Hospitalier Lyon-Sud, 69495 Pierre-Bénite
2
Inserm U851, IFR 128 Biosciences Lyon-Gerland, 21 avenue Tony Garnier,
69365 Lyon Cedex 7
De nombreux modèles animaux d’inflammation intestinale ont été
développés ces vingt dernières années. Leur nombre et la diversité
des mécanismes à l’origine d’une inflammation intestinale illustrent
la complexité du système immunitaire associé à l’intestin et de ses
facteurs de régulation. Tous ces modèles ont permis d’améliorer nos
connaissances sur l’immunité et les interactions entre la flore et
l’hôte dans des conditions normales et inflammatoires. La compré-
hension de la pathogénie des maladies inflammatoires chroniques
de l’intestin (MICI) chez l’homme a largement bénéficié de toutes
ces avancées. Les modèles animaux permettent aussi d’identifier de
nouvelles cibles thérapeutiques et constituent des outils indispensa-
bles pour tester l’efficacité et la toxicité de thérapeutiques anti-
inflammatoires et immuno-modulatrices innovantes.
Mots clés : colite expérimentale, modèle animal, haptène, MICI, inflammation
intestinale, cytokine
La détection de l’inflammation et des lésions intestinales et la
quantification de leur sévérité sont appréciées à l’aide de différents
critères. Les plus classiques sont la mortalité, l’importance de la
perte de poids de l’animal, la longueur du côlon qui se rétracte en cas de
colite sévère, son poids et son aspect macroscopique, l’intensité des
lésions histologiques (érosions, ulcérations, œdèmes, intensité de l’infiltrat
inflammatoire) et l’élévation de marqueurs biochimiques corrélés à
l’importance de l’infiltrat à polynucléaires neutrophiles dans l’intestin
comme l’activité myéloperoxydase (MPO), la lactoferrine, la calprotectine
fécale. Enfin, la quantification des cytokines proinflammatoires (TNFa,
interleukine (IL)-1b) dans l’intestin permet d’apprécier globalement l’inten-
sité de la réaction inflammatoire. Récemment, des progrès technologiques
de miniaturisation ont permis la visualisation dans le côlon de l’animal de
lésions macroscopiques à l’aide de mini-endoscopes adaptés.
Hépato-Gastro, vol. 15, n°1, janvier-février 2008
Tirés à part : S. Nancey
33
doi: 10.1684/hpg.2008.0182
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Mécanismes lésionnels
et modèles animaux
Même si de nombreuses espèces animales sont concer-
nées, la majorité des modèles d’inflammation intesti-
nale ont été développés chez la souris en raison de la
disponibilité, du coût, de la maniabilité de ces modèles
et des nombreux outils disponibles dans cette espèce
(invalidation ou surexpression de gènes par exemple).
Nous nous limiterons dans cette mini-revue aux princi-
paux modèles murins. Dans la plupart de ces modèles,
l’inflammation intestinale affecte exclusivement le
côlon, plus rarement l’iléon, parfois les deux.
On distingue classiquement les modèles d’inflamma-
tion spontanée et les modèles d’inflammation induite.
Les modèles d’inflammation intestinale
spontanée
Ceux-ci regroupent essentiellement les souris mutantes
(souches SAMP1/Yit, C3H/HeJ) et les souris généti-
quement modifiées chez lesquelles la colite survient
dans des conditions de surexpression d’un gène (souris
transgénique « knock-in ») impliqué dans l’inflamma-
tion (souris IL-7 transgénique ou TNF
DARE
par exemple).
Une colite peut aussi être observée chez des animaux
invalidés pour un gène (souris « knock-out ») affectant :
la fonction du lymphocyte T (souris déficiente pour la
molécule de classe II du complexe majeur d’histocom-
patibilité (CMH) ou déficiente pour le récepteur T des
lymphocytes), une cytokine anti-inflammatoire (IL-10
-/-
,
TGFb
-/-
) ou certains constituants nécessaires au main-
tien de l’intégrité de la barrière intestinale (souris
dominant négative pour la protéine de jonction inter-
cellulaire N-cadhérine qui remplace la E-cadhérine)
[1].
La souris mutante SAMP1/Yit est un modèle intéressant
à plusieurs titres : elle dérive d’une souris appelée AKR
(60-70 % d’homologies de séquences) et a été déve-
loppée initialement comme un modèle de vieillissement
accéléré. Cette souris mutante présente progressive-
ment autour de 15 semaines d’âge une iléite sponta-
née, parfois associée à une colite proximale [2]. Les
lésions inflammatoires intestinales présentent des simi-
litudes anatomocliniques importantes avec celles
observées dans la maladie de Crohn (MC) puisque
l’atteinte est transmurale, segmentaire et affecte électi-
Lumière intestinale
Mécanisme toxique
Inflammation
lésions
Recrutement
secondaire
Lymphocytes
Macrophages
Polynucléaires
Sang
Immunisation Colite
Révélation
Mécanisme d’hypersensibilité
retardée colique
DSS
Ganglions mésentériques
Antigène
Inflammation, lésions
Lumière intestinale
B
A
Flore
Cellule
dendritique
Cellule
épithéliale
intestinale
Cellule
dendritique
Infiltrat
Inflammatoire
1
2
LT
LT
3
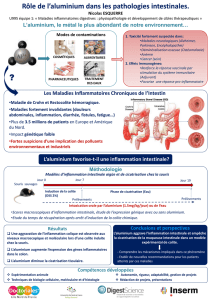
Figure 1.Colite induite par un mécanisme toxique (A) ou colite « immunologique » induite par une hypersensibilité retardée colique aux
haptènes (1) phase d’immunisation : l’haptène est pris en charge par les CPA qui migrent et le présentent aux LT naïfs dans les ganglions ; 2)
phase de révélation : les LT effecteurs migrent dans le côlon lors du second contact avec l’antigène et initient l’inflammation et les lésions de
l’épithélium intestinal ; 3) recrutement secondaire de cellules inflammatoires qui amplifient et perpétuent la maladie).
Mini-revue
Hépato-Gastro, vol. 15, n°1, janvier-février 2008
34
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

vement la région iléo-cæcale. Parfois, la présence de
granulomes épithélioïdes, caractéristiques de la MC, a
été décrite. De plus, des lésions fistulisantes anales ont
aussi été récemment mises en évidence dans ce modèle
animal qui est celui qui présente le plus grand nombre
de similitudes avec la MC.
Les modèles d’inflammation intestinale
induite
• Les modèles « toxiques »
Une colite peut être déclenchée par l’administration
d’un composé chimique toxique qui lèse la paroi intes-
tinale. Plusieurs voies d’administration du toxique sont
décrites, notamment le lavement (éthanol concentré,
acide acétique ou formaline) et la prise orale (sulfate
de dextrane sodique (DSS) dans l’eau de boisson). La
colite de mécanisme « toxique » apparaît rapidement
après l’administration du composé et conduit à des
lésions souvent sévères par altération de la barrière
intestinale qui met en contact la flore et l’immunité
intestinale sous-jacente. L’activation du système immu-
nitaire intestinal et le recrutement dans l’intestin de
cellules inflammatoires concourent à entretenir l’inflam-
mation et les lésions intestinales [1] (figure 1). Ces
modèles ont ainsi démontré l’importance de l’intégrité
de la barrière intestinale dans le maintien de l’homéos-
tasie intestinale.
• Les modèles « immunologiques »
Ces modèles reposent sur l’utilisation de molécules
chimiques de faible poids moléculaire non immunogè-
nes par elles-mêmes, appelées haptènes, comme
l’acide 2,4,6 trinitrobenzène sulfonique (TNBS) ou
l’acide 2,4 dinitrobenzène sulfonique (DNBS). L’admi-
nistration d’une faible dose non toxique d’un haptène
dans le côlon entraîne la formation d’un complexe
entre l’haptène et certains acides aminés constituant
des protéines du contenu et des parois coliques (par
exemple les résidus lysines qui forment ainsi un com-
plexe ayant des propriétés antigéniques) à l’origine de
l’induction d’une réponse immunitaire. Cette réponse,
localisée dans les ganglions mésentériques, se carac-
térise par l’activation, l’expansion et la différenciation
de lymphocytes T (LT) spécifiques d’antigène en cellules
effectrices et est complètement asymptomatique (phase
de sensibilisation). L’inflammation colique survient lors
d’un second contact de la muqueuse colique avec
l’haptène (phase de révélation) et résulte du recrute-
ment des LT effecteurs dans l’intestin. Ces effecteurs
spécifiques de l’antigène initient la réaction inflamma-
toire et les lésions intestinales qui sont amplifiées et
perpétuées par le recrutement d’autres cellules inflam-
matoires non spécifiques (macrophages, polynucléai-
res, lymphocytes, mastocytes).
Le mécanisme impliqué dans ces modèles « immunolo-
giques » est une hypersensibilité retardée (HSR type IV)
colique médiée par les LT CD4
+
ou LT CD8
+
spécifiques,
cytotoxiques et produisant des cytokines (figure 1)
. Ces
modèles s’accompagnent d’une inflammation récidi-
vante de l’intestin ; ceci supporte l’hypothèse qu’un
composant du contenu intestinal est à l’origine des
poussées récurrentes observées au cours des MICI.
• Les modèles de transfert
à des souris immunodéprimées
Le dernier modèle largement utilisé est représenté par
le transfert d’une population particulière de LT CD4
+
dits « naïfs », exprimant les molécules CD45RB
hi
, à des
animaux immunodéprimés (souris Nude ou RAG
-/-
dépourvues de LT ou SCID pour severe combined
immunocompromised deficiency dépourvues de LT et
de lymphocytes B). Ces animaux reconstitués avec
cette sous-population lymphocytaire T particulière
développent progressivement un infiltrat inflammatoire
puis des lésions coliques qui surviennent dans les
3-10 semaines suivant le transfert [3]. Ce modèle a
permis d’identifier, chez la souris, une sous-population
de LT CD4
+
« mémoires » (exprimant la molécule
CD45RB
low
) ayant des propriétés régulatrices. Le
co-transfert de ces LT et des LTCD4
+
naïfs CD45RB
hi
aux
animaux immunodéprimés prévient ainsi le développe-
ment de la colite [4]. Ces expériences ont aussi permis
de mettre en évidence le rôle du TGFbet d’une molé-
Abréviations :
CPA :cellule présentatrice d’antigène ;
CEACAM-1 :carcinoembryonnic antigen-related cell adhesion
molecule -1 ;
CARD15 :caspase activation and recruitment domain ;
CCR-9 :récepteur de chimiokine 9 ;
CMH :complexe majeur d’histocompatibilité ;
CPA :cellule présentatrice d’antigène ;
CTLA4 :cytotoxic T lymphocyte associated molecule-4 ;
DSS :sulfate de dextrane sodique ;
DNBS :dinitrobenzène sullfonate ;
HSR :hypersensibilité retardée colique ;
IL- :interleukine ;
IFNc:interféron c;
LT :lymphocytes T ;
MAPK :protéine kinase activée par les mitogènes ;
MC :maladie de Crohn ;
MICI :maladies inflammatoires chroniques de l’intestin ;
MPO :myelloperoxydase ;
NFjB:nuclear factor jB;
NKT :natural killer T cells ;
NOD2 :nucleotide-binding oligomerization domain ;
PPARc:récepteur activé des proliférateurs des peroxisomes ;
RAG :recombinase activating gene ;
RCH :rectocolite hémorragique ;
SCID :severe combined immunodeficiency ;
TcR :récepteur T du lymphocyte ;
Th :T helper ;
TGFb:transforming growth factor b;
TNBS :trinitrobenzène sulfonate ;
TNFa:tumor necrosis factor
␣
.
Hépato-Gastro, vol. 15, n°1, janvier-février 2008 35
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

cule de co-stimulation (CTLA-4) dans la régulation de
l’inflammation [5]. Néanmoins, les conséquences de
l’expansion clonale des LT transférés chez un receveur
immunologiquement « vide » constituent une limite
significative du modèle.
Une synthèse non exhaustive des principaux modèles
d’inflammation intestinale chez la souris est proposée
dans le tableau 1. La cinétique du développement de
la colite est variable selon les modèles de colite, de
quelques heures pour les inducteurs toxiques à plu-
sieurs semaines chez les animaux génétiquement mani-
pulés. Tous ces modèles ont permis d’étayer le concept
que l’inflammation intestinale pouvait résulter d’un
déséquilibre entre le pool des cellules effectrices et des
cellules régulatrices avec soit un excès d’effecteurs
(comme dans le modèle aux haptènes), soit un défaut
de régulateurs (comme dans le modèle de transfert à
des souris immunodéprimées) (figure 2).
Colites expérimentales,
sécrétion de cytokines
et voie de signalisation NFjB
Deux populations de LT CD4
+
ayant des propriétés
fonctionnelles de sécrétion de cytokines différentes ont
été décrites chez la souris : les T helper 1 (Th1) et les
Th2. Les lymphocytes Th1 activés produisent préféren-
tiellement de l’IL-2, de l’IFNcet du TNFatandis que les
Th2 produisent de l’IL-4, de l’IL-5 et de l’IL-13. La
majorité des modèles animaux d’inflammation intesti-
nale spontanée ou induite sont associés à un micro-
environnement riche en IL-12 et caractérisés par un
profil Th1 (figure 3). Les caractéristiques anatomo-
cliniques de ces modèles animaux Th1 se rapprochent
de la MC. Dans ces modèles, l’intensité de l’inflamma-
tion intestinale est réduite par l’utilisation d’un traite-
ment par anticorps anti-IL-12, anti-IFNcet anti-TNFa
mais aussi par l’administration d’IL-10 ou d’IL-4.
D’autres modèles, moins nombreux, sont plutôt Th2 en
raison de la mise en évidence de concentrations éle-
vées d’IL-4, d’IL-5 ou d’IL-13 dans l’intestin (souris
déficiente pour l’IL-2 ou pour la chaîne adu TcR, souris
transgénique pour l’IL-5, colite à l’oxazolone). Ces
modèles de colite, qui reproduisent plutôt l’atteinte
inflammatoire superficielle observée dans la rectocolite
hémorragique, sont améliorés par l’administration
d’anticorps anti-IL-4 (figure 3) [6]. Cette polarisation
fonctionnelle des LT helper 1 et 2 est contrôlée par
certains lymphocytes T régulateurs, dits « Th3 » qui
expriment fortement le marqueur de surface CD25, le
facteur de transcription intracytoplasmique FoxP3 et
produisent en grande quantité les cytokines immuno-
modulatrices IL-10 et/ou TGFb.
Cette dichotomie Th
1
/Th
2
est actuellement nuancée
dans les modèles animaux et chez l’homme puisque
des formes de passage d’un profil à l’autre sont possi-
bles au cours de l’évolution de la maladie. De plus, une
nouvelle famille de lymphocytes T, appelés Th17, a
récemment été identifiée au sein du système immuni-
taire intestinal [7]. Cette population Th17, induite par
l’IL-6 et le TGFbdans la muqueuse intestinale, est
capable de produire de grande quantité d’IL-17 et
d’IL-6, cytokines qui semblent jouer un rôle crucial dans
l’inflammation intestinale [8].
Tableau 1.Principaux modèles murins d’inflammation intestinale.
Colite spontanée Colite induite
Souris
mutantes
Souris
transgéniques
Souris
invalidées
Administration
de toxiques
Haptènes
(HSR)
Transfert à receveurs
immunodéprimés
SAMP1/Yit
C3H/HeJBir
STAT 4
IL-7
IL-12
TNF
DARE
Fonction lymphocyte T
TcRab
−/−
CMH classe II
−/−
Gai2
−/−
Cytokines
IL-10
−/−
IL-2
−/−
IL-2R
−/−
TGFb
−/−
CRFB4
−/−
Barrière intestinale
MDR
1−/−
Trefoil peptide
−/−
N-cadhérine
(dominant négatif)
Voie
intestinale
Formaline
Esters de
phorbols
Capsaïcine
Polysaccharides
sulfatés
Voie orale
Dextrane sodium
sulfate
Indométhacine
Carageenan
Injection
colique
Peptidoglycanes
DNBS
TNBS
Oxazolone
Scid
Nude
RAG
−/−
Lymphocytes T
CD4
+
CD45
+
RB
hi
(naïfs)
Moëlle osseuse
→Tge26
Mini-revue
Hépato-Gastro, vol. 15, n°1, janvier-février 2008
36
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Les modèles animaux ont aussi mis en évidence l’impli-
cation de différentes voies de signalisation intracellu-
laire dans la réaction inflammatoire intestinale, comme
les voies du NFjB ou des MAPkinases. Récemment, un
nouveau modèle de colite survenant chez des souris
invalidées pour un facteur d’activation de la voie NFjB
au niveau de l’intestin (souris NEMO) a été décrit. Ces
données suggèrent que cette voie de transduction,
jusque là considérée comme exclusivement proinflam-
matoire, participe au maintien de l’homéostasie intes-
tinale et au contrôle de l’inflammation locale [9].
L’étude des modèles animaux d’inflammation intesti-
nale a ainsi contribué à disséquer les mécanismes
immunologiques cellulaires mais aussi moléculaires
(voies de signalisation, réseaux de cytokines) impli-
qués dans la réaction inflammatoire intestinale au
cours des MICI.
Apport des modèles animaux
dans la compréhension des rapports
flore intestinale et inflammation
L’ensemble des modèles animaux a contribué à mon-
trer le rôle indispensable de la flore dans le dévelop-
pement de l’inflammation intestinale (figure 4). Ainsi,
l’atteinte inflammatoire intestinale prédomine dans la
majorité des modèles au niveau du côlon, site où la
flore intestinale est la plus abondante. De plus, la flore
intestinale est indispensable au développement de
l’inflammation intestinale puisqu’aucune inflammation
ou une inflammation intestinale réduite est observée
dans la quasi-totalité des modèles lorsque les animaux
sont élevés dans des conditions stériles (Germ-free).
L’inflammation intestinale apparaît secondairement ou
s’aggrave chez ces animaux lorsqu’ils sont exposés à
un environnement conventionnel. Dans le modèle de la
colite spontanée chez la souris C3H/HeJBir, la tolé-
rance immunitaire à la flore est anormale. En effet, la
stimulation des lymphocytes T isolés du côlon de cette
souris par un lysat de sa propre flore bactérienne
fécale active anormalement ces cellules avec produc-
tion de cytokines Th1[10].
L’injection transmurale dans la paroi colique de com-
posants bactériens (peptidoglycanes), reconnus par les
récepteurs NOD2/CARD15, est responsable d’une
colite granulomateuse chez le rat Lewis, suggérant qu’il
n’existe pas de spécificité bactérienne de la flore pour
induire l’inflammation intestinale. Néanmoins, la capa-
Cellules
régulatrices
Homéostasie intestinale
Cellules
effectrices
Th1 Th2
Cellules
régulatrices
Tr1 Th3
Cellules
régulatrices
Cellules
effectrices
Cellules
effectrices
InflammationInflammation
Excès
d’effecteurs
Défaut
de régulateurs
Homéostasie
intestinale
Figure 2.L’inflammation intestinale peut être consécutive à un excès de cellules effectrices ou à un déficit relatif de cellules régulatrices.
Hépato-Gastro, vol. 15, n°1, janvier-février 2008 37
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%