VIGI-PHARMA Bulletin d`informations

VIGI-PHARMA, N°12, Avril 2009, Page 1
M
ME
ED
DI
IC
CA
AM
ME
EN
NT
TS
S
R
RE
EC
CE
EN
NT
TS
S
:
:
D
DE
ES
S
E
EF
FF
FE
ET
TS
S
I
IN
ND
DE
ES
SI
IR
RA
AB
BL
LE
ES
S
A
A
S
SU
UR
RV
VE
EI
IL
LL
LE
ER
R
D
DE
E
P
PR
RE
ES
S
.
.
A
A
p
pr
ro
op
po
os
s
d
de
e
2
2
p
pr
ro
od
du
ui
it
ts
s
d
do
on
nt
t
l
le
es
s
c
co
on
ns
so
om
mm
ma
at
ti
io
on
ns
s
s
su
ui
iv
ve
en
nt
t
d
de
es
s
p
pe
en
nt
te
es
s
a
as
sc
ce
en
nd
da
an
nt
te
es
s…
…
L
L
Y
YR
RI
IC
CA
A
*
*
(
(P
Pr
ré
ég
ga
ab
ba
al
li
in
ne
e)
)
Sur le marché depuis 2004, la prégabaline, proche de la Gabapentine (
NEURONTIN
*), est un analogue du GABA qui fut
d’abord utilisé dans
l’épilepsie partielle et les douleurs neuropathiques, puis qui a vu ses indications s’élargir au traitement de l’anxiété généralisée depuis 2007. Les
effets indésirables notifiés sont : des troubles neurologiq
ues (somnolence, confusion mentale, sensations vertigineuses, tremblements), des
œdèmes généralisés associés à des troubles rénaux, respiratoires ou cardiaques graves et des prises de poids pouvant aller jusqu’à 20 kg, des effets
indésirables cutanés dont des œdèmes de Quincke, des neutropénies et thrombopénies, des atteintes du champ visuel pouvant être irréversibles
.
Un syndrome de sevrage est aussi décrit à l’arrêt du traitement.
C
YMBALTA
* (Duloxétine)
VIGI-PHARMA n°10 vous avait déjà fait part des nombr
euses interactions médicamenteuses auquel ce médicament exposait. Alors que son
efficacité reste incertaine, ses effets indésirables sont nombreux et parfois graves
: troubles neuropsychiques, digestifs, urinaires, sexuels,
augmentation dose-dépendante de la pression artérielle (d’où une contre-
indication chez le patient hypertendu), atteintes hépatiques (hépatites
cytolytiques et cholestatiques), des hémorragies parfois mortelles, des troubles de la natrémie à l’origine de chutes et pertes de conscience.
Avec tout ça, on se demande si le
CYMBALTA
* peut être un traitement de 1
ère
intention d’un épisode dépressif caractérisé ?
Prescrire, 2006, n°274, p 486 (1-
6) et Prescrire, 2007, n°279, p56
Prescrire, 2008, n°301, p 833 et Prescrire 2009, 303, p 9
V
VI
IG
GI
I-
-P
PH
HA
AR
RM
MA
A Bulletin d’informations pharmaceutiques
Service Pharmacie
N° 12 / Avril 2009 Centre Hospitalier Spécialisé du Jura
Rédacteurs : Christel Chalmendrier (Poste 1284) et Guy Martin (Poste 1397)
E
ED
DI
IT
TO
OR
RI
IA
AL
L
Plus de 6 mois sans nouvelles
de
VIGI
-
PHARMA
,
vous
deviez trouver le temps long,
non ?!
Heureusement, ce nouveau
VIGI
-
PHARMA
sort des
corbeilles en même temps
que les premières fleurs
printanières ! Nous espérons
que vous y trouverez des
sujets intéressant votre
pratique quotidienne, peut
être aussi que certains faits
titilleront votre esprit
critique, dans tous les cas,
c’est fait pour !
N’oubliez pas de rester
vigilants et de nous déclarer
les évènements iatrogènes
graves ou inattendus !
Nous restons à votre
disposition,
LES REDACTEURS
.
BREVES DE L
’
AFSSAPS
-
ACOMPLIA
* (Rimonabant)
AMM suspendue.
ACOMPLIA
*, premier médicament antagoniste des récepteurs CB1 aux
cannabinoïdes avait été promu en 2006 dans le traitement des sujets obèses ou en surpoids
avec des facteurs de risque associés (
Diabète de type 2, dyslipidémie
) conjointement à un
régime hypocalorique et à l’exercice physique. Dès le départ, troubles de l’humeur,
dépressions et troubles du sommeil ont été notifiés (dont 125 cas graves de troubles
dépressifs rapportés en France) ce qui avait conduit à une modification du RCP en 2007 et
2008. Fin 2008, le nombre de dépressions et de suicides causés par le rimonabant est
devenu si important que l’Agence européenne a (enfin !) suspendu l’AMM.
-
EQUANIL
* (Méprobamate) 400 mg/5 ml solution injectable IM
Restriction de l’indication. Désormais il ne s’agit plus que d’un traitement de deuxième
intention dans les états aigus d’anxiété ou d’agitation sur une période la plus brève possible
(max : 3 jours). Il est bon de rappeler que le méprobamate est responsable d’accidents
hématologiques et de réactions cutanées et d’hypersensibilité.
-
CONTRE
-
INDICATION DES ANTIHYPERTENSEURS ANTAGONISTES DES
RECEPTEURS DE L
’
ANGIOTENSINE
II
(
ALIAS SARTANS
)
ET DES INHIBITEURS DE
L
’
ENZYME DE CONVERSION
(IEC)
AU COURS DES
2
E ET
3
E TRIMESTRES DE LA
GROSSESSE
et leur utilisation déconseillée lors du 1
er
trimestre. (rappels)
Malgré l’information diffusée en 2003, des effets indésirables graves voire mortels
consécutifs à une telle exposition continuent d’être rapportés au réseau français de
pharmacovigilance, il s’agit d’insuffisances rénales fœtales et/ou néonatales parfois
compliquées d’anomalies des membres, de la voûte du crâne, voire de mort in utero.
-
PERFALGAN
*
(Paracétamol) sol 10 mg/ml (Flacons de 1G) pour injection IV
Le risque d’hépatotoxicité du paracétamol, en particulier par voie IV, est majoré en cas :
d’insuffisance hépatocellulaire, d’insuffisance rénale sévère, de malnutrition chronique,
d’alcoolisme chronique et de déshydratation : la dose maximale journalière ne devra pas
dépasser 3 g chez ces patients. En cas de surdosage, le risque d’atteinte hépatique est
particulièrement à craindre chez : les sujets âgés, les jeunes enfants, les patients ayant déjà
une atteinte hépatique, en cas d’alcoolisme chronique, de malnutrition chronique et chez les
patients recevant des médicaments inducteurs enzymatiques.
Lettres aux prescripteurs, Afssaps, http://www.afssaps.sante.fr

VIGI-PHARMA, N°12, Avril 2009, Page 2
H
HY
YP
PO
ON
NA
AT
TR
RE
EM
MI
IE
E
M
ME
ED
DI
IC
CA
AM
ME
EN
NT
TE
EU
US
SE
E
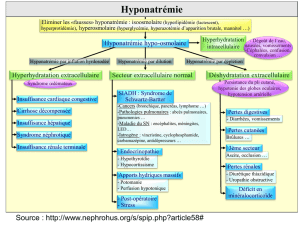
L’hyponatrémie se définit par une natrémie <135 mmol/l.
Les conséquences cliniques d’une hyponatrémie due à une déplétion en sodium
(conséquence de pertes rénales ou digestives) associée à une contraction
volémique sont une hypotension artérielle.
Une hyponatrémie de dilution (conséquence d’une polydipsie ou d’une
diminution de l’élimination de l’eau) est parfois asymptomatique ou entraîne
céphalées, confusion, nausées, vomissements, somnolence et faiblesse voire
quand ell
e est sévère, œdème cérébral avec convulsions, coma puis arrêt
respiratoire.
Une hyponatrémie est observée en cas d’insuffisance cardiaque, de cirrhose,
d’insuffisance surrénalienne ou encore en cas d’hyperglycémie.
Les médicaments hyponatrémiants sont essentiellement
: tous les diurétiques, la
desmopressine (
MINIRIN
*), les antidépresseurs inhibiteurs de la recapture de la
sérotonine, les antidépresseurs inhibiteurs de la recapture de la sérotonine et de
la noradrénaline, les antiépileptiques tels que la carbamazépine (
TEGRETOL
*),
l’oxcarbazépine (
TRILEPTAL
*), lamotrigine (
LAMICTAL
*), les sulfamides
hypoglycémiants.
Sont plus rarement cités
: des antidépresseurs imipraminiques, des
neuroleptiques, des inhibiteurs de la pompe à protons, des IEC, des AINS,
l’acide valproïque (
DEPAKINE
*).
La surveillance de la natrémie est d’autant plus importante que des facteurs de
risque sont présents. Une hyponatrémie est un effet indésirable d’installation
progressive, facilement décelable par un dosage biologique. Il vau
t mieux
informer le patient et assurer une surveillance de la natrémie en cas d’association
de médicaments hyponatrémiants, même si le rythme optimal de cette
surveillance n’est pas établi.
Prescrire, 2008, n°302 (Suppl Intercctions médicamenteuses), p 279
L
L’
’
U
UT
TI
IL
LI
IS
SA
AT
TI
IO
ON
N
C
CH
HR
RO
ON
NI
IQ
QU
UE
E
D
D
’
’
I
IN
NH
HI
IB
BI
IT
TE
EU
UR
RS
S
D
DE
E
L
LA
A
P
PO
OM
MP
PE
E
A
A
P
PR
RO
OT
TO
ON
NS
S
(
(I
IP
PP
P)
)
M
MA
AJ
JO
OR
RE
E
-
-
T
T
-
-
E
EL
LL
LE
E
L
LE
E
R
RI
IS
SQ
QU
UE
E
D
DE
E
F
FR
RA
AC
CT
TU
UR
RE
E
?
?
Une étude cas-témoin canadienne (CMJ 2008)
suggère une majoration de 92% du risque de fractures ostéoporotiques après 7
ans ou plus d’utilisation d’un IPP, valeur du même ordre que les autres facteurs de risques de telles fractures
: tabac, alcool,
élévation de l’IMC.
Le mécanisme de cet effet indésirable serait en rapport avec la réduction de la sécrétion d’acide
chlorhydrique, facteur important de l’a
bsorption du calcium dans le grêle. Les auteurs rappellent que face à l’utilisation
croissante des IPP, il convient de bien vérifier à chaque fois la réalité de l’indication. Et ne pas hésiter à réévaluer les prescriptions ….
Bulletin d’information de Pharmacologie, BIP31fr 2008, 15(3), p 18
R
RE
EF
FL
LE
EX
XI
IO
ON
N
C
CE
E
Q
QU
UE
E
D
DI
IS
SA
AI
IT
T
Z
ZA
AR
RI
IF
FI
IA
AN
N
“
“I
Il
l
n
n’
’e
ex
xi
is
st
te
e
p
pa
as
s
e
en
n
F
Fr
ra
an
nc
ce
e,
,
n
ni
i
a
ai
il
ll
le
eu
ur
rs
s,
,
d
de
e
p
ph
ha
ar
rm
ma
ac
co
ov
vi
ig
gi
il
la
an
nc
ce
e
q
qu
ui
i
s
so
oi
it
t
s
sp
pé
éc
ci
if
fi
iq
qu
ue
e
a
au
ux
x
e
ef
ff
fe
et
ts
s
p
ps
sy
yc
ch
hi
iq
qu
ue
es
s
d
de
es
s
p
ps
sy
yc
ch
ho
ot
tr
ro
op
pe
es
s.
.
O
Or
r
l
le
es
s
t
tr
ra
ai
it
te
em
me
en
nt
ts
s
p
pa
ar
r
l
le
es
s
p
ps
sy
yc
ch
ho
ot
tr
ro
op
pe
es
s
c
co
on
nn
na
ai
is
ss
se
en
nt
t
à
à
p
pr
ré
és
se
en
nt
t
d
de
es
s
p
pr
ro
ol
lo
on
ng
ga
at
ti
io
on
ns
s
i
in
nf
fi
in
ni
ie
es
s.
.
O
On
n
e
es
st
t
t
tr
rè
ès
s
l
lo
oi
in
n
d
de
es
s
é
év
va
al
lu
ua
at
ti
io
on
ns
s
q
qu
ue
e
l
l’
’o
on
n
t
tr
ro
ou
uv
ve
e
d
da
an
ns
s
l
le
es
s
d
do
os
ss
si
ie
er
rs
s
d
d’
’A
AM
MM
M
e
et
t
q
qu
ui
i
r
re
ep
po
os
se
en
nt
t
s
su
ur
r
d
de
es
s
e
es
ss
sa
ai
is
s
m
me
en
né
és
s
p
pe
en
nd
da
an
nt
t
s
si
ix
x
s
se
em
ma
ai
in
ne
es
s
d
de
e
t
tr
ra
ai
it
te
em
me
en
nt
t.
.
S
Si
ix
x
s
se
em
ma
ai
in
ne
es
s,
,
c
c’
’e
es
st
t
b
bi
ie
en
n
p
pe
eu
u.
.
Q
Qu
ue
e
s
sa
ai
it
t-
-o
on
n
d
de
es
s
e
ef
ff
fe
et
ts
s
p
ps
sy
yc
ch
hi
iq
qu
ue
es
s
i
ia
at
tr
ro
og
gè
èn
ne
es
s
s
su
ur
r
l
le
e
l
lo
on
ng
g
t
te
er
rm
me
e
?
?
A
Au
u
b
bo
ou
ut
t
d
de
e
d
di
ix
x
a
an
ns
s
d
de
e
n
ne
eu
ur
ro
ol
le
ep
pt
ti
iq
qu
ue
es
s
o
ou
u
d
de
e
b
be
en
nz
zo
od
di
ia
az
zé
ép
pi
in
ne
es
s,
,
a
au
u
b
bo
ou
ut
t
d
de
e
p
pl
lu
us
si
ie
eu
ur
rs
s
a
an
nn
né
ée
es
s
d
d’
’a
an
nt
ti
id
dé
ép
pr
re
es
ss
se
eu
ur
rs
s,
,
a
a-
-t
t-
-o
on
n
t
tr
ra
ai
it
té
é
s
se
eu
ul
le
em
me
en
nt
t
d
de
es
s
s
sy
ym
mp
pt
tô
ôm
me
es
s
p
pa
at
th
ho
ol
lo
og
gi
iq
qu
ue
es
s
o
ou
u
a
a-
-t
t-
-o
on
n
m
mo
od
di
if
fi
ié
é
d
de
e
f
fa
aç
ço
on
n
p
pe
eu
ut
t-
-ê
êt
tr
re
e
d
dé
éf
fi
in
ni
it
ti
iv
ve
e
l
le
e
p
ps
sy
yc
ch
hi
is
sm
me
e
d
d’
’u
un
n
ê
êt
tr
re
e
h
hu
um
ma
ai
in
n
?
?
»
»
In :
Le Prix du Bien Etre.
Psychotropes et So
ciété
. 1996
A
A
N
NT
TI
ID
DE
EP
PR
RE
ES
SS
SE
EU
UR
RS
S
I
IR
RS
S
E
ET
T
V
VI
IO
OL
LE
EN
NC
CE
E
Les antidépresseurs IRS ont été, depuis le début des années 2000, reconnus à l’origine de comportements suicidaires chez les
enfants d’abord, puis chez les adultes jeunes. C’est en 2004 que les premières mentions en rapport avec une hétéroagressivité
ont commencé à apparaître dans certains résumés des caractéristiques (RCP) des IRS ; il est ainsi mentionné : anxiété,
agitation, attaques de panique, insomnie, irritabilité, hostilité, agressivité, impulsivité, akathisie, hypomanie et manie chez les
enfants et les adultes. Le rôle des IRS dans des agressions et des homicides a été évoqué. Déjà les essais cliniques de la
paroxétine et de la sertraline avaient mis en évidence une plus grande fréquence de manifestations « d’hostilité » que sous
placebo. Le terme hostilité recouvrait notamment violence et agressivité. (Le fait de rassembler divers termes sous un même
codage fait perdre de l’information d’une part et d’autre part à la première lecture on ne trouve aucune observation de
violence ou d’agression). Ainsi les données concernant « l’hostilité » devenaient d’autant plus préoccupantes dès lors que l’on
savait ce qui y était rangé. Après une émission sur la paroxétine en 2002, la télévision britannique a reçu plus de 1000
courriers de patients ou de leur entourage : 13 décès par suicide décrits comme surprenants par l’entourage, 47 tentatives de
suicide, 92 cas d’accès de violence contre soi-même ou contre autrui ont été recensés. Certains patients n’avaient aucun
antécédent de comportements violents. Ces comportements semblaient survenir assez souvent soit en début de traitement,
soit lors d’un changement de dose soit lors du sevrage. Des affaires sont traitées en justice.
Ces faisceaux de données convergent pour imputer à des antidépresseurs IRS des troubles émotionnels affectant certains
patients et conduisant à des actes de violence dirigés contre le patient lui-même ou son entourage. Si ces évènements sont
rares, les conséquences peuvent être dramatiques. Les patients exposés sont à suivre de près !
Prescrire, 2008, n°296, p 431-432
1
/
2
100%